
- •1 Вопрос
- •11 Вопрос
- •12 Вопрос
- •13 Вопрос (н.Ц.)
- •14 Вопрос (н.Ц.)
- •15 Вопрос
- •21 Вопрос
- •22 Вопрос
- •24 Вопрос
- •25 Вопрос
- •26 Вопрос
- •34 Вопрос
- •35 Вопрос
- •36 Вопрос
- •37 Вопрос
- •38 Вопрос (н.Ц.)
- •39 Вопрос
- •40 Вопрос
- •41 Вопрос
- •42 Вопрос (н.Ц.)
- •43 Вопрос
- •44 Вопрос
- •45 Вопрос
- •46 Вопрос
- •52 Вопрос
- •53 Вопрос
- •54 Вопрос (н.Ц применение диодов, принцип действия триода)
- •55 Вопрос (н.Ц.)
1 Вопрос
Основные положения МКТ и их опытное обоснование.
Основные положения молекулярно-кинетической теории (МКТ):
-все тела состоят из частиц,
-все частицы находятся в постоянном движении,
-все частицы взаимодействуют между собой;
Опытные обоснования:
Диффузия – взаимное проникновение молекул одного вещества между молекулами другого (вода-краска),
Броуновское движение – хаотичное тепловое движение частиц, в результате которого приходят в движение взвешенные (?) частицы.
2 Вопрос
Скорость движения молекул и ее измерение. Опыт Штерна.
Между частицами действуют силы притяжения и отталкивания, Для определения скорости движения молекул в 1920 году немецкий физик Штерн провел опыт по измерению скорости молекул. Скорость молекул в веществе распределяется от 1500 м/с до 380 м/с.
3 Вопрос
Идеальный газ.
Идеальный газ – газ, соответствующий следующим условиям:
-объёмом всех молекул можно пренебречь, по сравнению с объемом сосуда,
-время столкновения молекул друг с другом пренебрежимо мало,
-молекулы взаимодействуют между собой только при непосредственном соприкосновении,
-силы притяжения между молекулами ничтожно малы, либо ими можно пренебречь.
4 Вопрос
Масса и размеры молекул. Количество вещества. Постоянная Авогадро.
Кол-во вещества (v) определяет относительное число молекул в теле.
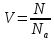
Na - Постоянная Авогадро
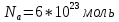
N - Число молекул в теле\веществе
Масса одной молекулы определяется по формуле:
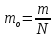
m - масса вещества
5 Вопрос (н.ц.)
Основное уравнение МКТ.
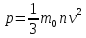
Где:
p – давление
n – концентрация газа
m0 -масса молекулы
v – средняя скорость молекул
6 Вопрос
Уравнение Менделеева-Клапейрона.
p*Vм = R*T
p - Давление
Vм - Молярный объём
R - Универсальная газовая постоянная
Т – абсолютная температура [K]
7 Вопрос
Изопроцессы и их графики.
Изопроцессы – процессы, происходящие в газах, при условии, что меняются лишь два из пяти параметров вещества.
m-масса
T-температура
V-объем
P-?
1.Изотермический процесс m-const
T-const
Изохорный процесс
m-const
v-const
Изобарный процесс
m-const
p-const
*графики*
8 Вопрос
Термодинамическая шкала температур.
В термодинамике, температура измеряется в Кельвинах [К]. T = t+273
9 Вопрос
Внутренняя энергия газа.
Внутренняя энергия газа (термодинамика) – часть полной энергии, которая определяется собственными параметрами системы. ВЭГ складывается из кинетической энергии хаотичного теплового движения частиц и потенциальной энергии их взаимодействия.
10 Вопрос
Первое начало термодинамики, его применение к изопроцессам.
Закон сохранения энергии (основа первого закона термодинамики) – энергия системы не исчезает бесследно и не возникает из ничего. Она только передается от одного тела к другому или превращается из одной формы в другую (кинетическая\внутренняя).
Первый закон термодинамики – изменение внутренней энергии термодинамической системы зависит от количества теплоты, переданной данной системе и работы внешних сил.
Изотермический процесс
V-const
Q=0
∆U=A’
Изохорный
P*∆V – работа газа
A=0
∆U=Q
Изобарный
p-const
A=0
∆U=Q
Адиабатный (?)
∆Q=0
∆U=A
11 Вопрос
Второе начало термодинамики.
Второй закон термодинамики – количество теплоты, полученное системой извне, не может быть целиком преобразовано в механическую энергию тепловой машиной, действующей циклически.
