
Lektsia_8
.docЛекция № 8
УГЛЕВОДЫ
|
Генетический ряд D – сахаров
|
|
|
Лекция № 8
I. Реакции по карбонильной группе
1. СИНТЕЗ ФИШЕРА – КИЛЛИАНИ
(Переход от низших моносахаридов к высшим)
Например:

D-эритроза два диастереоизомера, т.к. две диастереоизомерные
возникает новый асиммет- альдоновые кислоты
рический центр при С2

-лактоны D-арабиноза D-рибоза
(две диастереоизомерные пентозы)
-
МЕТОДЫ УКОРОЧЕНИЯ
УГЛЕРОДНОЙ ЦЕПИ МОНОСАХАРИДОВ
(превращение D-галактозы (альдогексозы) в D-ликсозу (альдопентозу)
а) Метод Руффа:

D-галактоза D-ликсоза
Лекция № 8
б) Метод Воля:

D-галактоза D-ликсоза
в) Метод Вермана:

D-галактоза

D-ликсоза
Лекция № 8
3. ЭПИМЕРИЗАЦИЯ МОНОЗ.
В слабощелочной среде наблюдается эпимеризация – взаимные превращения моносахаридов, различающихся конфигурацией при первых двух атомах углерода (реакция Лобри де Брюина – Альберда ван Экенштейна).
ОБРАЗУЮТСЯ ЭПИМЕРЫ

4. ПОЛУЧЕНИЕ ОЗАЗОНОВ. Реакция с фенилгидразином
При образовании озазонов в результате реакции моноз с избытком фенилгидразина исчезают отличия в строении и конфигурации эпимеров у первых двух С-атомов. Таким образом, эпимеры образуют одинаковые озазоны.

Лекция № 8
5. Реакции окисления
а) со слабыми окислителями такими как, например,
реактив Толленса ([Ag(NH3)2]OH),
жидкостью Фелинга (Cu(OH)2/соль винной кислоты).
Реакция идет только по карбонильной группе (альдегидная (кетонная) группа окислится до карбоксильной) в результате образуются окси-кислоты (см. таблицу 8.1.)
б) с сильными окислителями такими как, например, концентрированная азотная кислота (HNO3).
Сильные окислители окисляют, кроме карбонильной группы, еще и первичную спиртовую. При этом образуются сахарные кислоты (см. таблицу 8.1.).
6. Реакции восстановления
Оксо-группа (карбонильная группа) восстанавливается до гидроксильной амальгамой натрия (Na/Hg), алюмогидридом лития LiAlH4, боргидридом натрия (NaBH4), а также при взаимодействии с водородом в присутствии Ni-катализатора. (см. таблицу 8.1.).
II. Реакции по гидроксильным группам
1. Дегидратация
При нагревании с разбавленной Н2SO4 альдозы отщепляют воду. При этом все пентозы превращаются в фурфурол.
|
|
Отщепление воды – единственная реакция по гидроксильным группам, в которую монозы вступают в альдегидной форме. Обычно все реакции по OH – группе вступают циклические формы.
2. Алкилирование
(См. таблицу 8.1., циклические формы). При взаимодействии углевода со спиртом в присутствии соляной кислоты, водород при гликозидном (полуацетальном) гидроксиле замещается на алкил.
Для алкилирования остальных ОН-групп могут применятся, например иодоформ СH3I, (СН3О)2SO4 и др. реактивы
Лекция № 8
3. Ацилирование
|
Введение ацила |
|
|
Таблицу 8.1 |
|
ХИМИЧЕСКИЕ РЕАКЦИИ МОНОСАХАРИДОВ


Лекция № 8
ВАЖНЕЙШИЕ ДИСАХАРИДЫ (БИОЗЫ)

мальтоза (солодовый сахар) лактоза (молочный сахар)

целлобиоза (древесный сахар) сахароза (тростниковый сахар)
Лекция № 8
КОЛЬЧАТО-ЦЕПНАЯ ТАУТОМЕРИЯ
Явление существования динамического равновесия между незамкнутой оксо-формой и циклическими пяти- и шестичленными полуацетальными формами (фуранозами, пиранозами) для γ- и δ-окси-оксосоединений (моносахаридов, восстанавливающих дисахаридов и др.)
б) для моносахаров

.D-глюкопираноза .D-глюкопираноза

аль-D-глюкоза
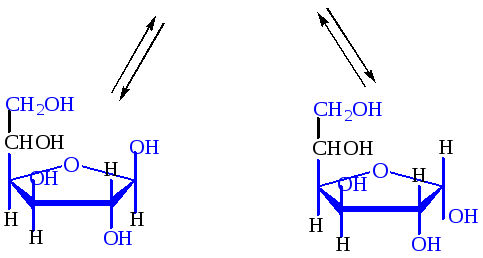
.D-глюкофураноза .D-глюкофураноза
б) для дисахаров

-лактоза -лактоза
 аль-лактоза
аль-лактоза
Лекция № 8
РЕАКЦИИ ЛАКТОЗЫ (МОЛОЧНОГО САХАРА)

-лактоза -лактоза
 аль-лактоза
аль-лактоза

-лактоза ,D-галактопираноз ,В-глюкопираноза
аль-лактоза

лактобионовая кислота ,D-галактопираноза D-глюконовая
кислота
-лактоза

октаметиллактоза

2,3,4,6-тетра-О-метил-,D- 2,3,6-три-О-метил-,D-
-галактопираноза -глюкопираноза


