
- •Министерство образования и науки рф
- •Введение
- •Раздел I. Основы химической термодинамики
- •1.1 Основные понятия, используемые в химической термодинамике
- •1.2 Первый закон термодинамики
- •1.3 Термохимия
- •1.3.1 Закон Гесса и следствия из него. Расчет тепловых эффектов
- •1.3.2 Понятие о теплоемкости веществ
- •1.3.3 Влияние температуры на тепловой эффект
- •1.4 Второй закон термодинамики. Энтропия
- •1.4.1 Процессы самопроизвольные и несамопроизвольные,
- •1.4.2 Формулировки и математическое выражение
- •II закона термодинамики
- •1.4.3 Изменение энтропии – критерий направления
- •1.4.4 Статистическая интерпретация энтропии
- •1.4.5 Расчет изменения энтропии при протекании
- •1.4.6 Абсолютные значения энтропии твердых, жидких
- •1. Абсолютное значение энтропии твердых кристаллических тел.
- •2. Абсолютное значение энтропии жидкости.
- •3. Абсолютное значение энтропии газа.
- •1.5 Термодинамические потенциалы
- •Критерии оценки направления самопроизвольного протекания процессов
- •Раздел II. Растворы и гетерогенные равновесия
- •2.1 Основные понятия и определения
- •2.2 Химический потенциал
- •Условие термодинамического равновесия в растворе
- •2.4 Условие равновесия в гетерогенной системе
- •2.5 Правило фаз Гиббса
- •2.6 Равновесие в однокомпонентной двухфазной системе.
- •2.7 Применение правила фаз Гиббса к анализу диаграммы
- •2.8 Равновесие в гетерогенных системах, состоящих
- •2.8.1 Равновесие жидкость – пар. Закон Рауля
- •2.8.2 Коллигативные свойства растворов
- •2.8.3 Равновесие жидкость-жидкость. Распределение вещества
- •Раздел III. Химическое равновесие
- •3.1 Уравнение изотермы химической реакции
- •3.2 Влияние внешних условий на протекание химической реакции
- •Раздел IV. Электрохимия
- •4.1 Равновесие в растворах слабых электролитов
- •4.2 Термодинамика растворов сильных электролитов
- •4.3 Электрическая проводимость растворов электролитов
- •4.4 Электродвижущие силы и электродные потенциалы
- •Механизм возникновения электродных потенциалов и их расчет
- •Термодинамика гальванического элемента
- •Основные типы электродов и расчет их потенциала
- •Раздел V. Химическая кинетика и катализ
- •5.1 Основной закон химической кинетики.
- •5.2 Основы формальной кинетики кинетика необратимых реакций
- •5.3 Методы определения порядка реакции
- •3. Метод Вант-Гоффа.
- •5.4 Влияние температуры на скорость реакции
- •5.5 Основные понятия катализа
5.3 Методы определения порядка реакции
Из предыдущего раздела следует, что для создания математической модели химической реакции необходимо знать ее порядок.
Существует несколько методов определения порядка реакции.
1. Метод подстановки. Сущность метода заключается в эмпирическом подборе такого кинетического уравнения, которое лучшим образом описывает результаты эксперимента. Существует два варианта реализации метода подстановки.
1) Аналитический метод, заключающийся в том, что для описания экспериментальных данных используются уравнения для реакций различных порядков и выбирается то уравнение, которое наилучшим образом описывает результаты эксперимента. Для этого по опытным значениям концентраций в различные моменты времени рассчитывают константу скорости реакции первого, второго и т.д. порядка. Уравнение удовлетворительно описывает процесс, если рассчитанные по нему значения констант колеблются около какой-либо средней величины и отклонения от среднего лежат в пределах погрешности определения.
2) Графический метод. Зависимость концентрации во времени для реакций различных порядков может быть выражена прямой линией, если подобрать соответствующую систему координат. Так для реакции нулевого порядка зависимость концентрации реагирующего вещества от времени имеет линейный вид:
![]()

Для реакции 1-го порядка прямая получается в системе координат lnС = f():
![]()

![]()
Для реакции 2-го
порядка при
![]() линейная зависимость в координатах1/С = f():
линейная зависимость в координатах1/С = f():
![]() ;
;
![]()

Подбирается случай, когда зависимость в соответствующих координатах прямолинейная. По тангенсу угла наклона можно определить значение константы скорости.
Недостаток метода подстановки заключается в его трудоемкости.
2. Графический метод. Запишем кинетическое уравнение в виде:
![]()
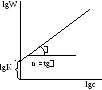 ,
,
прологарифмируем
![]() .
.
Полученное уравнение является линейным, поэтому порядок реакции n будет равен тангенсу угла наклона прямой.
Недостаток метода заключается в необходимости определения абсолютной скорости реакции, что может привести к ошибкам.
3. Метод Вант-Гоффа.
О снован
на определении абсолютной скорости
реакции в начальный момент времени при
двух различных концентрациях реагирующего
вещества:
снован
на определении абсолютной скорости
реакции в начальный момент времени при
двух различных концентрациях реагирующего
вещества:![]() .
Тогда:
.
Тогда:
 ,
,
где ω0 - скорость реакции при исходной концентрации реагирующего вещества с2;
ω0 - скорость реакции при исходной концентрации реагирующего вещества с1.
Логарифмируя уравнения, почленно вычитая их друг из друга и решая относительно n, получим:
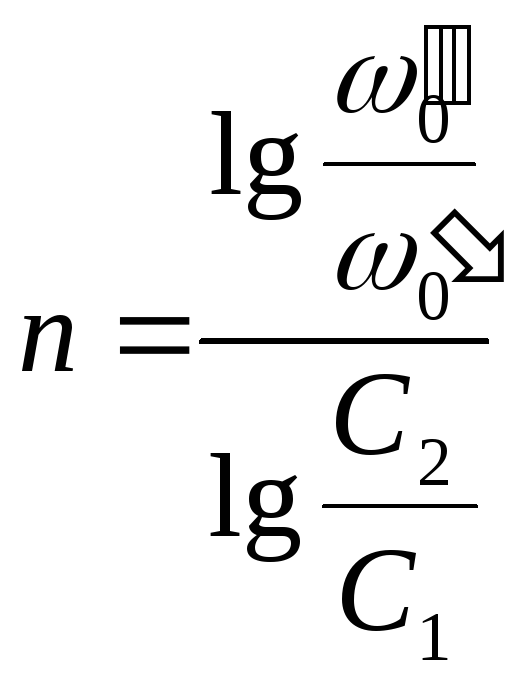
Метод Вант-Гоффа достаточно точен.
5. Метод избыточных концентраций (Оствальда). Основан на исследовании зависимости скорости реакции от начальной концентрации какого-либо одного реагента. Для этого в опытах меняется начальная концентрация одного реагента, а другие исходные вещества берутся в большом избытке – тогда концентрации этих веществ можно принять постоянными. Порядок по первому реагенту определяется по одному из вышеуказанных методов. Затем проводят аналогичные опыты с переменной начальной концентрацией другого исходного вещества в избытке остальных. Общий порядок реакции равен сумме порядков по отдельным компонентам.
