
- •Введение
- •Предельные углеводороды (алканы и циклоалканы)
- •Способы получения
- •Углеводороды с двойными связями алкены
- •Диеновые углеводороды
- •Понятие об ароматичности
- •Функциональные производные
- •Галогенопроизводные
- •Физические свойства
- •Кислородсодержащие функциональные производные
- •Одноатомные спирты
- •Физические свойства
- •Применение.
- •Многоатомные спирты
- •Физические свойства
- •Применение.
- •Фенолы, нафтолы
- •Физические свойства
- •Оксосоединения. Альдегиды и кетоны.
- •Физические свойства
- •Применение.
- •Карбоновые кислоты
- •Одноосновные кислоты (насыщенные и ароматические)
- •Способы получения
- •Одноосновные ненасыщенные кислоты
- •Физические свойства.
- •Применение.
- •Двухосновные кислоты
- •Применение.
- •Функциональные производные карбоновых кислот
- •Гидроксикислоты
- •Углеводы. Определение, строение, нахождение в природе.
- •Физические свойства
- •Физические свойства
- •Азотсодержащие соединения
- •Нитросоединения
- •Физические свойства
- •Применение.
- •Диазо- и азосоединения
- •Физические свойства
- •Применение.
- •Аминокислоты
- •Классификация, изомерия
- •Химические свойства
- •Значение аминокислот
- •Пептиды
- •Гетероциклические соединения
Физические свойства
Физические свойства галогенопроизводных зависят от строения углеводородного радикала, вида галогена и числа галогенов. С увеличением молекулярной массы и переходом от F к I плотность и температура кипения увеличиваются для моногалогенопроизводных. Дигалогенопроизводные – тяжелые масла или твердые вещества. Все галогенопроизводные нерастворимы в воде, растворяются в органических растворителях. Токсичны, большинство имеют специфический резкий запах. Некоторые обладают анестезирующим действием (CH2Cl2, CHCl3) или антисептическим (CHI3).
ХИМИЧЕСКИЕ СВОЙСТВА
Т.к. в молекуле галогенопроизводных σ-связь сильно поляризована из-за большей электроотрицательности атома галогена, электронная плотность у атома углерода понижается, поэтому он легко атакуется нуклеофильными частицами (т.е. молекулами или ионами, способными предоставлять свою электронную пару (НО-, NO2-, CN-, I-, NH3, Н2О и др).
Галогенопроизводные – очень реакционноспособные вещества, легко вступают в реакции замещения (SN1, SN2) и отщепления (EN1, EN2), протекающие по нуклеофильным механизмам, а также в реакции восстановления.
1) Восстановление галогенопроизводных может быть проведено водородом в присутствии катализаторов, либо водородом в момент выделения:
![]()
2) Реакции отщепления галогена (элиминирования) протекают по механизмам EN1 и EN2 под действием спиртовых растворов щелочей. Механизм EN2 характерен для первичных галогенопроизводных
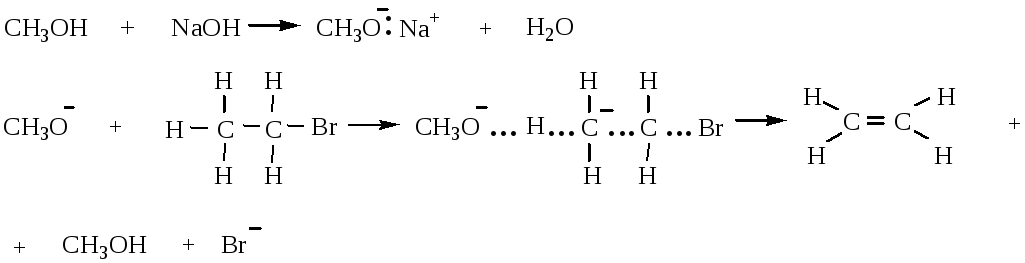
Третичные галогенопроизводные реагируют по механизму EN1:
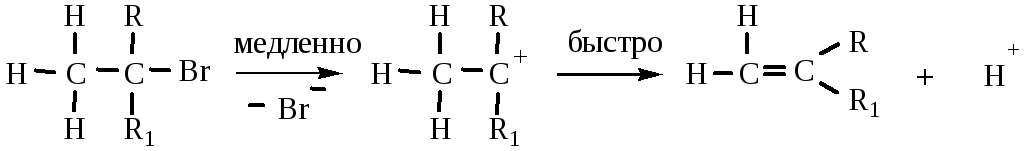
Легкость отщепления
галогена в SN-реакциях
убывает в ряду ![]() .
.
3) Реакции замещения протекают по двум механизмам: SN2 – характерен для первичных галогенопроизводных, описывается кинетическим уравнением второго порядка, т.е. скорость реакции зависит от концентрации обоих компонентов. Реакционная способность убывает в ряду: метиленовые галогенопроизводные > первичные > вторичные > третичные.
Вначале нуклеофильная частица ОН¯ подходит к атому углерода, связанному с галогеном, находящимся в sp3-гибридизованном состоянии.
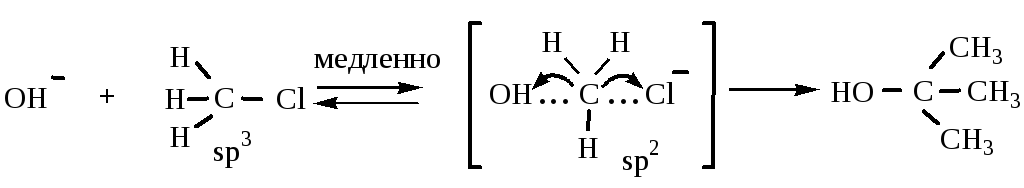
Образуется активированный неустойчивый комплекс; по мере приближения аниона ОН¯ к атому углерода он отталкивает атомы водорода, которые располагаются под углом 120о. При этом связи С–Н лежат в одной плоскости, то есть углерод переходит в sp2-гибридное состояние. Затем происходит вытеснение Cl¯ и углерод снова становится sp3-гибридизованным.
SN1 – механизм, который характерен для третичных галогенопроизводных.
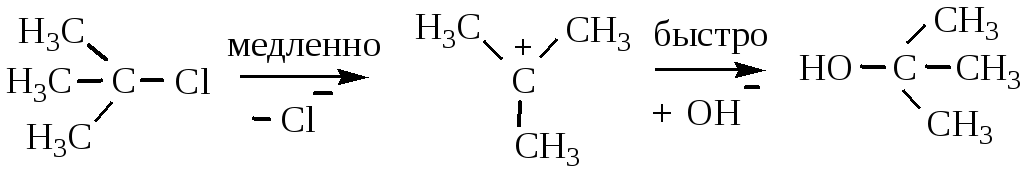
Вначале происходит диссоциация галогенопроизводного на ионы, затем образующийся при этом карбкатион атакуется нуклеофильной частицей. При этом скорость процесса зависит только от концентрации галогенопроизводных и определяется кинетическим уравнением первого порядка. Вторичные галогенопроизводные вступают в реакции замещения по смешанному механизму.
При замещении галогена на нуклеофилы могут быть получены разнообразные классы органических соединений:
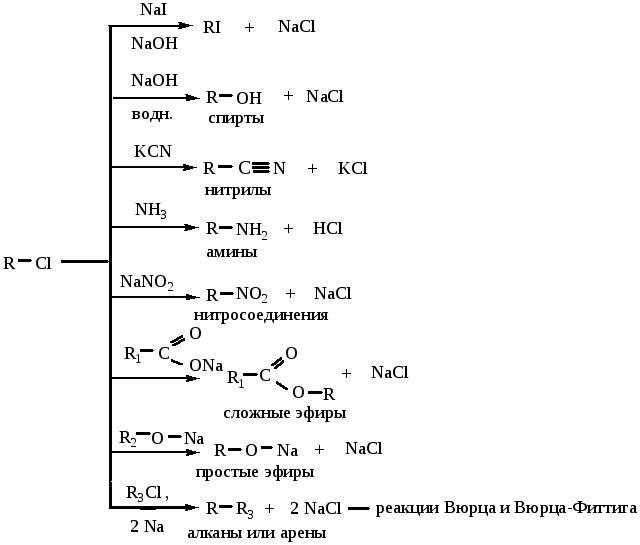
4) Образование магнийорганических соединений (реактивов Гриньяра) происходит при действии Mg на галогенопроизводные в среде абсолютного эфира.
![]()
ФТОРПРОИЗВОДНЫЕ
По способу получения и по химическим свойствам фторпроизводные резко отличаются от других галогенопроизводных. Из-за химической активности фтора прямое фторирование затруднено, поэтому фторпроизводные могут быть получены следующими способами:
1. Действием AgF на Br-, Cl- и I-производные, т.е. заменой галогена на галоген
![]()
2. Фторирование алканов в среде азота
![]()
Химические свойства фторпроизводных также отличаются рядом особенностей. Монофторгалогенопроизводные легко восстанавливаются:
![]()
Дифторгалогенопроизводные – более устойчивы, полностью фторгалогенопроизводные исключительно химически и термически устойчивы, не разлагаются при температуре 500 оС, стойки к кислотам и щелочам, не токсичны. Используются для производства инертных растворителей, смазывающих масел и пластмасс.
