
- •Глава 3. Функциональные производные алканов
- •3.1. ОбщноСть Химических свойств
- •3.1.1. Реакции нуклеофильного замещения
- •3.1.2. Реакции отщепления (элиминирования)
- •3.2. Галогеналканы
- •3.2.1. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •3.2.3. Способы получения
- •3.2.4. Полигалогеналканы
- •3.2.5. Физиологическая роль и Важнейшие представители
- •3.3. Насыщенные спирты
- •3.3.1. Классификация, номенклатура, изомерия
- •3.3.2. Строение и физические свойства
- •3.3.3. Химические свойства
- •3.3.4. Способы получения
- •3.3.5. Многоатомные спирты
- •3.3.6. Физиологическое действие
- •3.3.7. Важнейшие представители
- •3.4. Простые насыщенные эфиры
- •3.4.1. Номенклатура и изомерия
- •3.4.2. Физические и химические свойства
- •3.4.3. Способы получения
- •3.4.4. Циклические простые эфиры
- •3.4.5. Физиологическая роль и Важнейшие представители
- •3.5. Эфиры минеральных кислот
- •3.5.1. Эфиры серной кислоты
- •3.5.2. Эфиры фосфорной кислоты
- •3.6. Тиоспирты и тиоэфиры
- •3.7. Насыщенные амины
- •3.7.1. Классификация, номенклатура, изомерия
- •3.7.2. Физические свойства
- •3.7.3. Строение и химические свойства
- •3.7.4. Способы получения
- •3.7.5. Физиологическая роль и Важнейшие представители
- •3.8. Нитроалканы
- •3.8.1. Строение
- •3.8.2. Свойства
- •3.8.3. Способы получения
- •3.8.4. Физиологическое действие и Важнейшие представители
- •3.9. Кремний-, фосфор- и мышьякорганические соединения
- •3.9.1. Кремнийорганические соединения
- •3.9.2. Фосфорорганические соединения
- •3.9.3. Мышьякорганические соединения
- •Вопросы и упражнения
3.2.3. Способы получения
1. Одним из способов получения галогеналканов является прямое галогенирование предельных углеводородов, например:
R-H + Br2 R-Br + HBr
Закономерности протекания этих реакций были рассмотрены в свойствах алканов (гл. 2.4.1).
2. галогеналканы могут быть получены из спиртов и других галогеналканов с помощью реакции замещения, например:
R-Х + НBr R-Br + HX
Эти реакции, относящиеся к нуклеофильному замещению в спиртах и галогеналканах, рассмотрены в главе 3.1.1. К эффективным реагентам для получения галогеналканов относятся PCl3, POCl3, PCl5, PBr3, PBr5, PI3, SOCl2.
3. Может быть использовано галогенирование и гидрогалогенирование алкенов и алкинов, например:
СН2=СН2 + Br2 СН2Br-СН2Br
СН2=СН2 + HBr СН3-СН2Br
СНСН + 2HCl СН3-СНCl2
Подробнее эти реакции будут рассмотрены в свойствах соответствующих углеводородов (гл. 4.2.3, 4.4.2).
4. Галогеналканы могут быть получены из альдегидов, кетонов и карбоновых кислот действием PCl5, PBr3 или SF4 при нагревании. Эти реакции относятся к химическим свойствам соответствующих карбонильных соединений и будут рассмотрены позже (гл. 6.1.4.1, 6.4.4.2).
3.2.4. Полигалогеналканы
Это производные предельных углеводородов, в молекулы которых входят два или несколько атомов галогена (одинаковых или разных). Закономерности строения, физических и химических свойств, способов получения, являющиеся общими с моногалогеналканами, рассмотрены выше.
К особенностям физических свойств, химического поведения и способов получения соединений с несколькими атомами галогена можно отнести следующее.
Необычными физическими свойствами обладают полифторированные алканы. Температуры кипения соединений состава CnF2n+2 близки температурам кипения алканов с таким же числом атомов углерода, хотя молекулярная масса их существенно больше. Это объясняется незначительными ван-дер-ваальсовыми силами во фторорганических соединениях из-за их малой поляризуемости. Поэтому такие полифтороуглеводороды (точнее, фтороуглероды), как полимер тефлон (-CF2-CF2-)n, обладают высокой химической устойчивостью и низкой адгезией.
Реакционная способность геминальных полихлороалканов в SN-реакциях, как правило, ниже, чем монохлороалканов из-за меньшей полярности связей C–Cl. Но в сильнокислой среде реакционная способность таких соединений может быть повышена, так как избыточная концентрация катионов Н+ способствует протонированию хлора и увеличению полярности связи C–Cl.
Геминальные ди- и тригалогенопроизводные при гидролизе образуют альдегиды, кетоны, карбоновые кислоты:
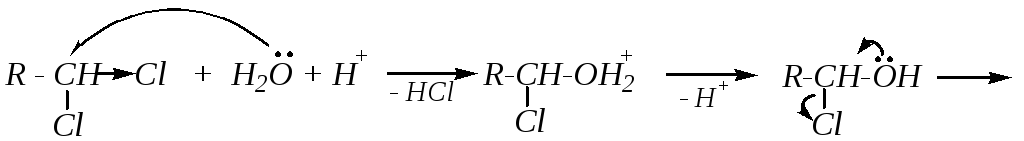
![]()
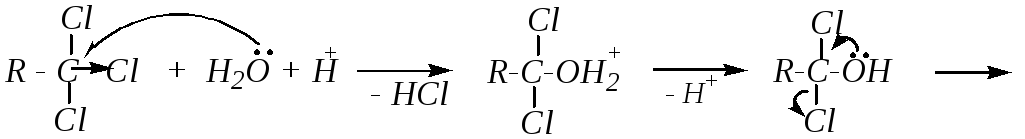

Щелочной гидролиз в этих случаях менее предпочтителен, так как затруднён подход нуклеофила к реакционному центру из-за его экранирования атомами галогена. Наиболее вероятный механизм реакции здесь — SN2.
4. Геминальные дигалогеналканы (дихлороалканы) могут быть получены из карбонильных соединений действием на них таких хлорирующих агентов, как PCl5, SOCl2 :
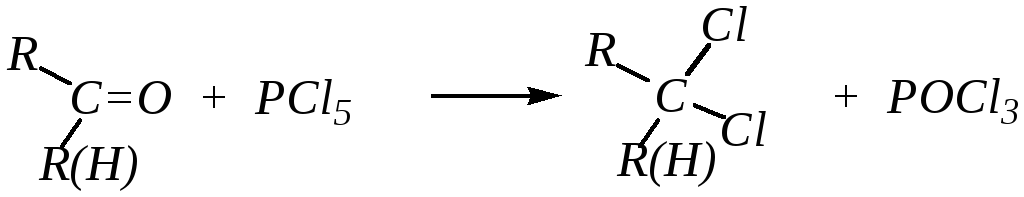
5. Накопление у атома углерода атомов галогена приводит к повышению полярности связи C–H, что способствует отрыву протона от атома углерода и в конечном итоге приводит к образованию дихлоркарбена:
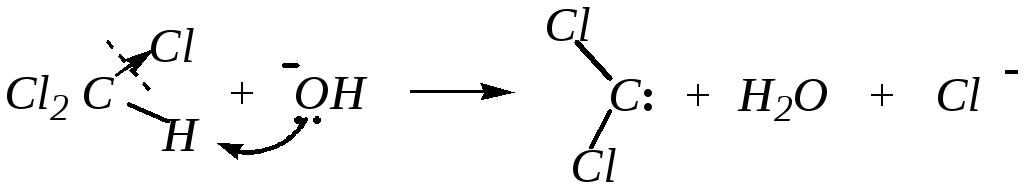
дихлоркарбен
В дихлоркарбене у атома углерода имеются два электрона, которые теоретически могут располагаться либо на двух орбиталях одинаковой энергии (триплетная форма), либо на одной орбитали (синглетная форма). Основным состоянием дигалокарбенов :CHal2 является синглетное (как и для других карбенов с заместителями, содержащими неподелённую электронную пару), хотя энергия синглет-триплетного перехода для дихлоркарбена невелика и составляет 56.5 кДж/моль. Дихлоркарбен за счёт вакантной орбитали синглетной формы легко присоединяет воду:
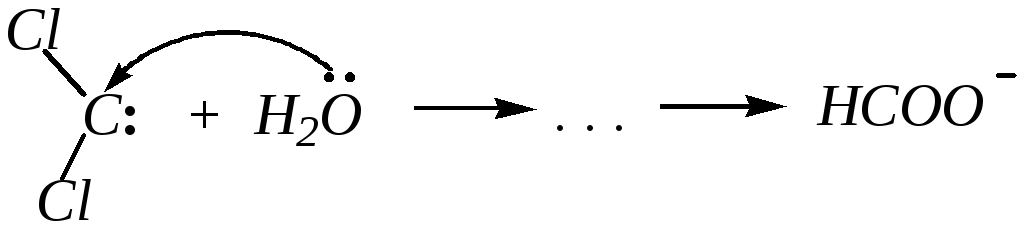
Вицинальные дигалогеналканы под действием цинковой пыли подвергаются дегалогенированию:
R-CНBr-CН2Br + Zn R-CН=CН2 + ZnBr2
Эта реакция часто служит одним из способов получения алкенов.
