
- •Глава 3. Функциональные производные алканов
- •3.1. ОбщноСть Химических свойств
- •3.1.1. Реакции нуклеофильного замещения
- •3.1.2. Реакции отщепления (элиминирования)
- •3.2. Галогеналканы
- •3.2.1. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •3.2.3. Способы получения
- •3.2.4. Полигалогеналканы
- •3.2.5. Физиологическая роль и Важнейшие представители
- •3.3. Насыщенные спирты
- •3.3.1. Классификация, номенклатура, изомерия
- •3.3.2. Строение и физические свойства
- •3.3.3. Химические свойства
- •3.3.4. Способы получения
- •3.3.5. Многоатомные спирты
- •3.3.6. Физиологическое действие
- •3.3.7. Важнейшие представители
- •3.4. Простые насыщенные эфиры
- •3.4.1. Номенклатура и изомерия
- •3.4.2. Физические и химические свойства
- •3.4.3. Способы получения
- •3.4.4. Циклические простые эфиры
- •3.4.5. Физиологическая роль и Важнейшие представители
- •3.5. Эфиры минеральных кислот
- •3.5.1. Эфиры серной кислоты
- •3.5.2. Эфиры фосфорной кислоты
- •3.6. Тиоспирты и тиоэфиры
- •3.7. Насыщенные амины
- •3.7.1. Классификация, номенклатура, изомерия
- •3.7.2. Физические свойства
- •3.7.3. Строение и химические свойства
- •3.7.4. Способы получения
- •3.7.5. Физиологическая роль и Важнейшие представители
- •3.8. Нитроалканы
- •3.8.1. Строение
- •3.8.2. Свойства
- •3.8.3. Способы получения
- •3.8.4. Физиологическое действие и Важнейшие представители
- •3.9. Кремний-, фосфор- и мышьякорганические соединения
- •3.9.1. Кремнийорганические соединения
- •3.9.2. Фосфорорганические соединения
- •3.9.3. Мышьякорганические соединения
- •Вопросы и упражнения
3.7.4. Способы получения
Распространённым способом получения аминов является аммонолиз галогеналканов и, как продолжение его, алкилирование аминов по Гофману — эти реакции рассмотрены в химических свойствах (гл. 3.2.2.1 и 3.7.3.3). Однако данным способом обычно получается смесь первичных, вторичных и третичных аминов.
Амины могут быть получены и при алкилировании аммиака спиртами — эта реакция также рассмотрена в химических свойствах (гл. 3.3.3.1). Она лежит в основе промышленного метода получения аминов.
Одним из способов получения насыщенных аминов является полное восстановление нитросоединений (или других азотсодержащих соединений) по схеме:
R-NO2 R-NH2
R-CH=NH R-CH2-NH2
R-NH-OH R-NH2
R-CN R-CH2-NH2
R-CO-NH2 R-CH2-NH2
Однако такой способ пригоден только для получения первичных аминов, но образующиеся амины всегда загрязнены продуктами неполного восстановления нитросоединений (оксимы, азо- и гидразосоединения и др.).
4. Другим способом получения чистых первичных аминов является синтез Габриэля:
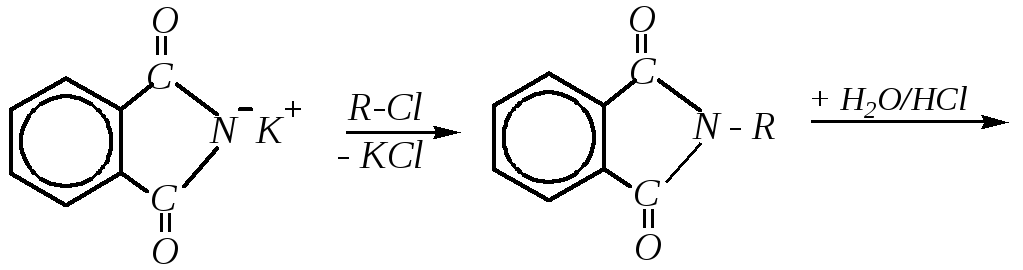
фталимид калия N-алкилфталимид
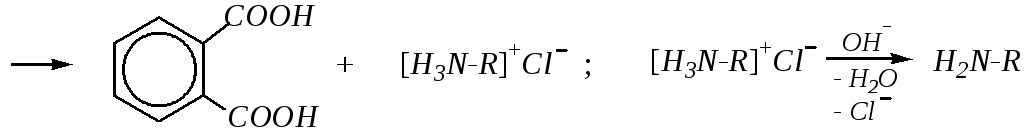
фталевая кислота
Первая стадия здесь — взаимодействие галогеналкана с фталимидом калия, являющимся нуклеофилом, — типичная реакция SN в ряду галогеналканов. За ней следует гидролиз образовавшегося N-алкилфталимида, который обычно проводят в солянокислой среде. Подробнее о закономерностях протекания таких реакций — см. в свойствах карбоновых кислот и их производных (гл. 6.4.4.2, 10.9.3.2).
5. Ещё одним способом получения чистых первичных аминов является перегруппировка Гофмана:
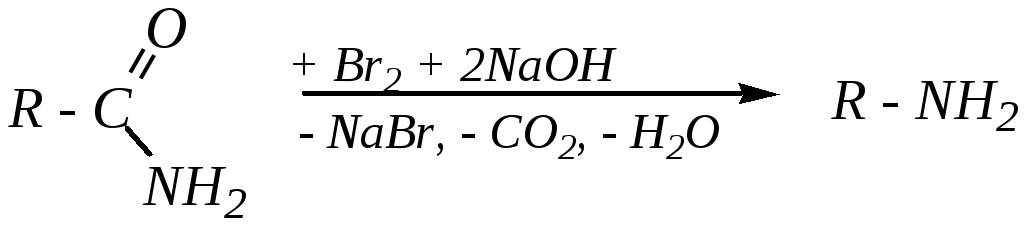
Механизм этой реакции, относящейся к свойствам амидов карбоновых кислот, рассмотрен в главе 6.4.4.5.
6. Один из способов получения чистых вторичных аминов из первичных включает в себя несколько стадий. Первая из них — нуклеофильная атака амина по атому серы сульфохлоридной группы аренсульфохлорида (гл. 10.3.5.1):
![]()
где Ar – ароматический углеводородный радикал
Вторая стадия — образование сульфамидом соли при взаимодействии со щёлочью:
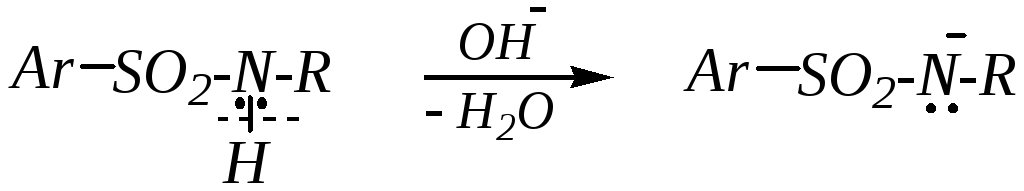
И затем — алкилирование этого сульфамид-аниона галогеналканом (например, бромоалканом), то есть нуклеофильное замещение атома галогена в галогеналкане сульфамидной группой:

И, наконец, кислотный гидролиз образовавшегося диалкилсульфамида:
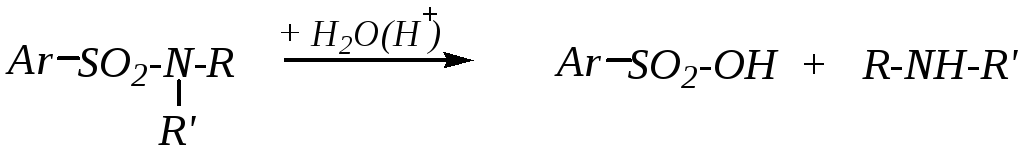
3.7.5. Физиологическая роль и Важнейшие представители
Среди алифатических аминов особое значение для медицинской практики имеют производные бис-(-хлорэтил)-амина, которые применяются в качестве противоопухолевых веществ. Злокачественные опухоли — это заболевания, связанные с усиленным размножением клеток, приводящим к быстрому росту новообразованной опухолевой ткани, которая давит на соседние органы, прорастая сквозь ткани и дезорганизуя работу организма. Большую роль в возникновении злокачественных опухолей играет нарушение обмена нуклеиновых кислот. Различные производные бис-(-хлорэтил)-амина оказывают тормозящее действие на размножение клеток, блокируя их митотическое деление. Механизм действия лекарственных веществ этой группы основан на их алкилирующем действии и способности легко реагировать с нуклеиновыми кислотами, белками и ферментами. Эти вещества также легко взаимодействуют с нуклеопротеидами (белок и нуклеиновая кислота) клеточных ядер кроветворных тканей. Высокой чувствительностью к производным бис-(-хлорэтил)-амина обладают ядра клеток опухолевой ткани. Таким образом, вещества этой группы, с одной стороны, способны тормозить рост опухолевой ткани, с другой — угнетают процесс кроветворения и являются токсичными веществами.
Метиламин — бесцветный газ с острым запахом, подобным запаху аммиака. Хорошо растворяется в воде.
Хлорид метиламмония образует бесцветные кристаллы с температурой плавления 498 К.
В промышленности метиламин получают каталитическим гидрированием циановодорода или при взаимодействии метанола и аммиака над катализатором при повышенной температуре.
Метиламин применяется в органическом синтезе для получения лекарственных веществ, красителей и поверхностно-активных веществ.
Диметиламин — газ с неприятным запахом, хорошо растворимый в воде.
Хлорид диметиламмония — бесцветное кристаллическое вещество с температурой плавления 444 К.
Диметиламин получают каталитическим алкилированием аммиака метанолом. Его используют в синтезе лекарственных веществ и растворителей.
Триэтиламин — бесцветная жидкость с характерным запахом аминов. В промышленности его получают каталитическим алкилированием аммиака этанолом.
Триэтиламин используют в органическом синтезе в качестве исходного вещества, растворителя и оснóвного катализатора.
Этилендиамин — бесцветная жидкость с запахом аммиака, хорошо растворяется в воде.
Его получают из дихлорэтана и аммиака.
Этилендиамин является важным исходным веществом для синтеза аналитических реагентов (комплексонов) и фунгицидов. Соли этилендиамина с высшими карбоновыми кислотами применяются в текстильной промышленности в качестве мягчителей.
Тетраметилендиамин (путресцин) — кристаллическое вещество с температурой плавления 300—301 К и пентаметилендиамин (кадаверин) — жидкость с температурой кипения 451 К. Растворимы в воде. Образуются при гнилостном разложении трупов. Относятся к группе трупных ядов.
Гексаметилендиамин — бесцветное кристаллическое вещество с температурой плавления 315 К и температурой кипения 477 К. Растворим в воде.
В промышленности получают из динитрила адипиновой кислоты NC-(CH2)4-CN.
Используют для получения полиамидов и синтетического волокна (найлон).
Этаноламины H2NCH2CH2ОH, HN(CH2CH2ОH)2, N(CH2CH2ОH)3 — бесцветные вязкие жидкости, при низких температурах — кристаллические вещества, хорошо растворимые в воде.
Этаноламины используют в органическом синтезе для получения эмульгаторов, моющих средств и косметических препаратов как адсорбенты кислых газов и как ингибиторы коррозии.
Холин [(CH3)3N+CH2CH2ОH]ОH¯ — бесцветное гигроскопичное кристаллическое вещество. По свойствам ему более соответствует строение внутренней соли (CH3)3N+CH2CH2О¯ H2О.
Холин широко распространён в животных и растительных тканях, высоко его содержание в нервной ткани. Холин играет важную роль в обмене веществ, входит в состав фосфолипидов. См. также далее, гл. 6.4.7.
