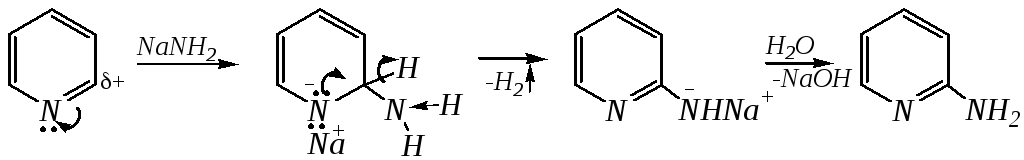- •Глава 12. Гетероциклические соединения
- •12.1. Классификация и номенклатура
- •12.2. Пятичленные гетероциклические
- •12.2.1. Номенклатура пиррола, фурана и тиофена и их производных
- •12.2.2. Строение пиррола, фурана и тиофена
- •12.2.3. Физические и химические свойства пиррола, фурана и тиофена
- •12.2.4. Особенности индола
- •12.2.5. Способы получения пиррола, фурана, тиофена, индола
- •12.2.6. Важнейшие представители и медико-биологическое значение
- •12.3. Пятичленные гетероциклические
- •12.3.1. Номенклатура имидазола и пиразола
- •12.3.2. Строение имидазола и пиразола
- •12.3.3. Физические и химические свойства имидазола и пиразола
- •12.3.4. Способы получения
- •12.3.5. Важнейшие представители и медико-биологическое значение
- •12.4. Шестичленные гетероциклические
- •12.4.1. Номенклатура пиридина и его производных
- •12.4.2. Строение пиридина
- •12.4.3. Химические свойства пиридина
- •Но если оба -положения заняты, то замещается водород в-положении. При нагревании с избытком амида натрия можно получить 2,6-диаминопиридин.
- •12.4.4. Особенности химического поведения пиколинов и функциональных производных пиридина
- •12.4.5. Хинолин и изохинолин
- •12.4.6. -Пиран и -пиран и их производные
- •12.4.7. Способы получения
- •Реакция аналогична получению бензола, протекает при высоких температурах, но представляет только теоретический интерес.
- •12.4.8. Важнейшие представители и медико-биологическое значение
- •12.5. Шестичленные гетероциклические
- •12.5.1. Строение и свойства диазинов
- •12.5.2. Пурин
- •12.5.3. Способы получения
- •12.5.4. Важнейшие представители и медико-биологическое значение
- •12.5.5. Нуклеозиды, нуклеотиды и нуклеиновые кислоты
- •12.6. Алкалоиды
- •Вопросы и упражнения
12.4. Шестичленные гетероциклические
соединения с одним гетероатомом
Шестичленные гетероциклические соединения также могут содержать атомы азота, кислорода и серы. Но наиболее важны в практическом отношении азотосодержащие гетероциклы — пиридин, его производные и конденсированные соединения на их основе. Широко распространены также гетероциклические соединения на основе пиранов — циклов, содержащих атом кислорода.
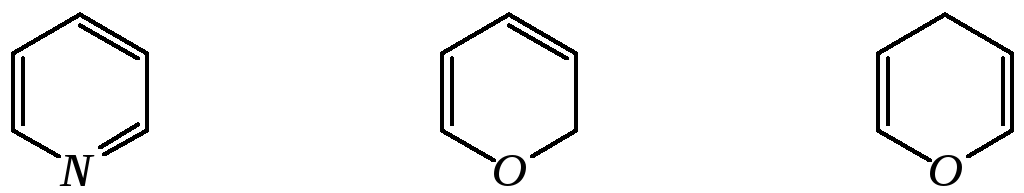
пиридин -пиран-пиран
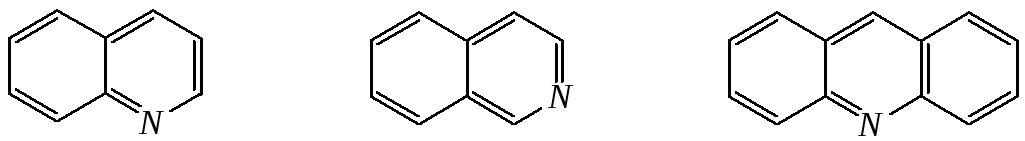
хинолин изохинолин акридин
12.4.1. Номенклатура пиридина и его производных
Систематическое название пиридина — азин (гл. 12.1). Однако как для самого гетероцикла, так и для его производных почти всегда используется тривиальное название «пиридин».
Атомы цикла могут быть обозначены цифровыми локантами или же греческими буквами. Соответственно, возможны три радикала пиридина:
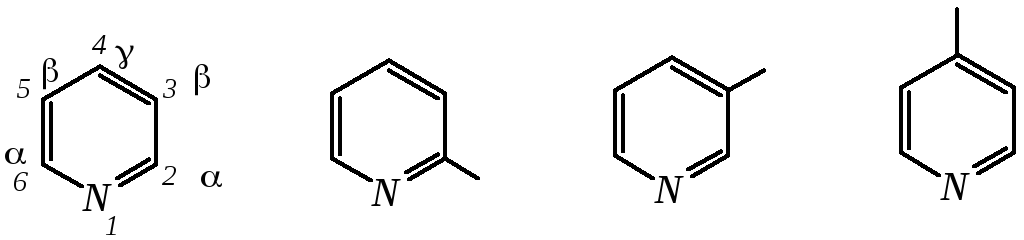
-пиридил-пиридил-пиридил
(пиридил-2) (пиридил-3) (пиридил-4)
Метилпроизводные пиридина имеют тривиальное название «пиколины», диметилпроизводные — «лутидины», например:
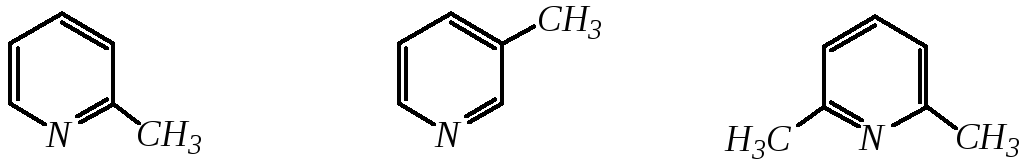
-пиколин-пиколин 2,6-лутидин
(2-метилпиридин) (3-метилпиридин) (2,6-диметилпиридин)
-, - и -пиридинкарбоновые кислоты имеют каждая своё тривиальное название:
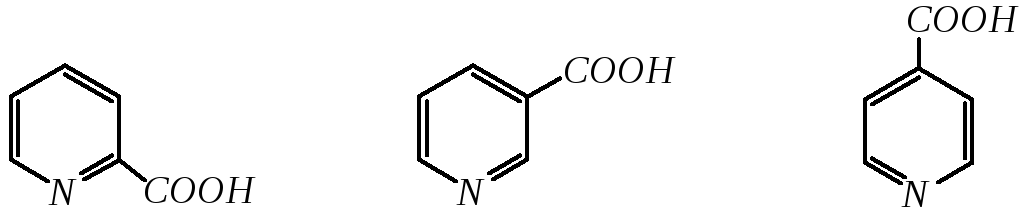
пиколиновая кислота никотиновая кислота изоникотиновая кислота
(пиридин-2-карбоновая (пиридин-3-карбоновая (пиридин-4-карбоновая
кислота) кислота) кислота)
12.4.2. Строение пиридина
Молекула пиридина, как и молекула бензола, представляет собой плоский шестиугольник, содержащий сопряжённую -электронную систему, удовлетворяющую всем критериям ароматичности, в том числе и правилу Хюккеля (6 -электронов). Однако пиридиновый цикл содержит атом азота вместо одного из атомов углерода бензольного кольца. Ввиду большей электроотрицательности азота по сравнению с углеродом валентные углы и длины связей в молекуле пиридина несколько искажены по сравнению с бензолом. Энергия делокализации ароматической системы пиридинового кольца составляет 117 кДж/моль (против 151 кДж/моль для бензола).
Атом азота находится в состоянии sp2-гибридизации; его 3 валентных электрона участвуют в образовании двух -связей и -электронной сопряжённой системы ароматического кольца. А его неподелённая электронная пара находится на sp2-гибридной орбитали, ось которой лежит в плоскости гетероцикла, и потому эти электроны не могут участвовать в сопряжении с -электронной системой кольца.
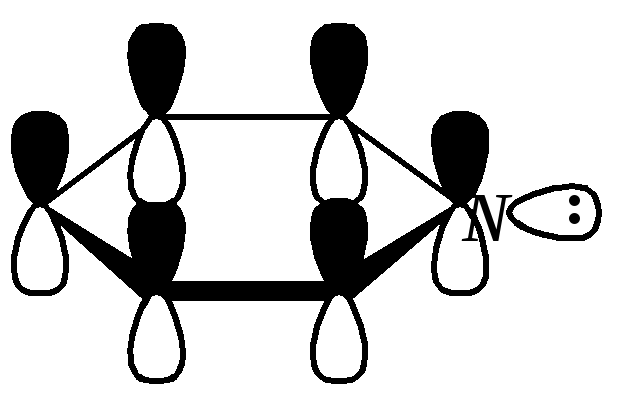
Атом азота в целом является электроноакцептором, понижая электронную плотность на атомах углерода кольца. Он проявляет –I-эффект и, участвуя в сопряжении, –М-эффект. В связи с этим распределение -электронной плотности в ароматическом кольце можно показать с помощью граничных структур:
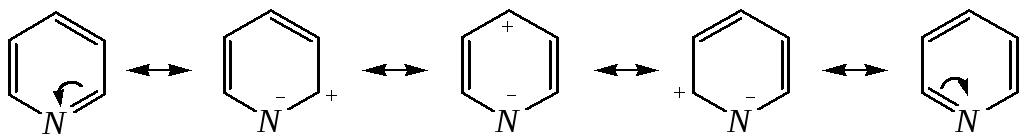 ,
,
из которых следует, что наибольшие эффективные положительные заряды, вызванные акцепторным влиянием атома азота, создаются в - и -положениях, причём акцепторное влияние азота на -атомы сильнее по причине индуктивного эффекта.
12.4.3. Химические свойства пиридина
Химические свойства пиридина, как следует из его строения, должны быть достаточно многообразны. Это и реакции непосредственно по атому азота (основные свойства, реакции алкилирования, окисления), и реакции с участием ароматического кольца (электрофильное и нуклеофильное замещение, гидрирование).
12.4.3.1. Основность
Пиридин является типичным основанием с рКb = 8.8. Его основность ниже основности аммиака и алифатических аминов, так как неподелённая электронная пара пиридинового азота, за счёт которой происходит взаимодействие с протоном, находится на sp2-гибридной орбитали. Электронная же пара аминного атома азота находится на sp3-гибридной орбитали, поэтому более удалена от ядра и легче взаимодействует с протоном (рКb аммиака равна 4.8, метиламина — 2.3).
С другой стороны, основность пиридина выше основности анилина и ароматических аминов (рКb анилина = 9.4). В молекуле анилина, как и других ароматических аминов, неподелённая электронная пара азота участвует в сопряжении с ароматическим кольцом и делокализована, а в молекуле пиридина пара электронов принадлежит только атому азота.
Основные свойства пиридина проявляются как при взаимодействии с кислотами, так и при взаимодействии с водой:

хлорид пиридиния
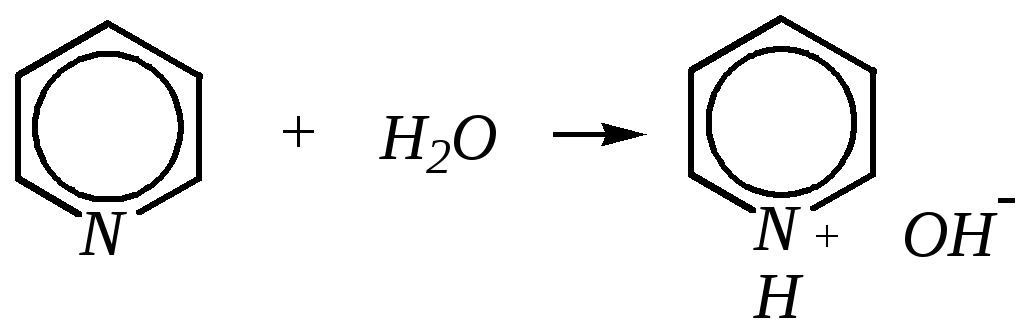
гидроксид пиридиния
12.4.3.2. Реакции алкилирования по атому азота
Неподелённая электронная пара азота энергетически более доступна для атаки электрофильными агентами, чем сопряжённая система ароматического кольца. Однако только с алкилирующими агентами атом азота образует устойчивые продукты взаимодействия. Реакции между пиридином и галогеналканами протекают легко:
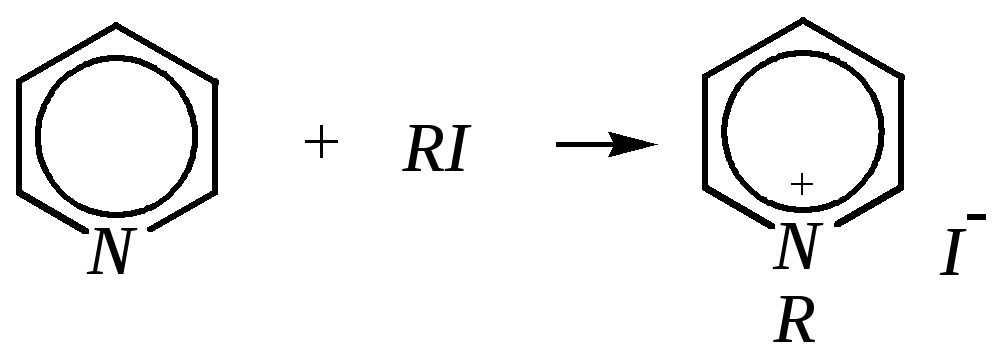
йодид N-алкилпиридиния
По механизму эти реакции — типичные примеры нуклеофильного замещения, в которых пиридин является нуклеофилом.
Но при нагревании продукт алкилирования по азоту претерпевает перегруппировку, протекающую по радикальному механизму, с выбросом галогеноводорода. Результатом этого является образование - и -алкилпиридинов:
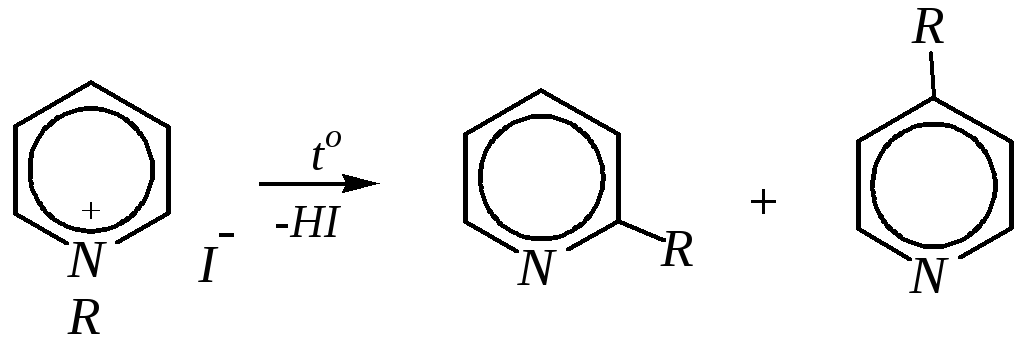
12.4.3.3. Реакции электрофильного замещения
В молекуле пиридина имеются два реакционных центра для электрофильной атаки, и, как было сказано выше, легче она должна осуществляться по атому азота. Действительно, большинство электрофилов на первой стадии атакует атом азота, а затем происходит перегруппировка с образованием более прочных связей электрофильных частиц с атомами углерода кольца. При этом электрофильное замещение всегда протекает по -углеродному атому в отсутствие других ориентирующих групп, так как - и -атомы дезактивированы электроноакцепторным влиянием атома азота (см. выше). В целом электрофильное замещение в цикле пиридина протекает в жёстких условиях (при температурах около 500—570 К). Одним из примеров является реакция хлорирования, которая без катализатора протекает при 470 К, а в присутствии хлорида алюминия — при 370 К. Образование связи C–Cl здесь происходит при действии избытка хлорирующего агента:
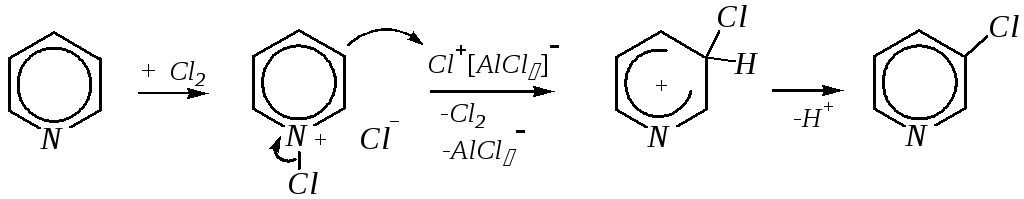
-хлорпиридин
Проведение хлорирования при более высокой температуре (500 К) приводит к смене механизма, в результате чего вместо SE-реакции протекает радикальное замещение (SR) и образуются продукты -замещения:
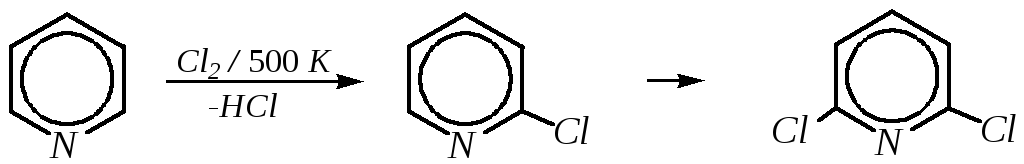
-хлорпиридин 2,6-дихлорпиридин
Для проведения электрофильного бромирования требуется использование раствора брома в олеуме при 400 К:
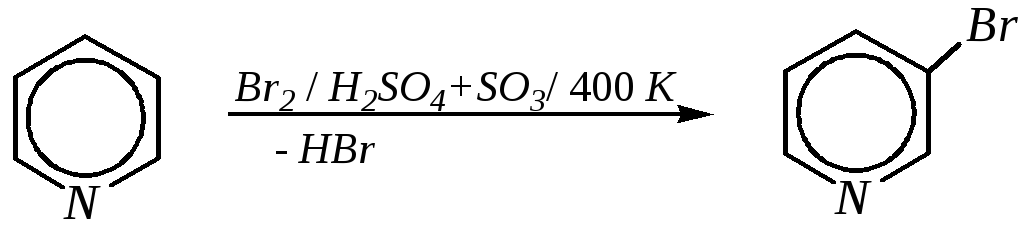
-бромпиридин
Проведение бромирования без растворителя при более высокой температуре (770 К) также приводит к смене механизма реакции, в результате протекает радикальное замещение:
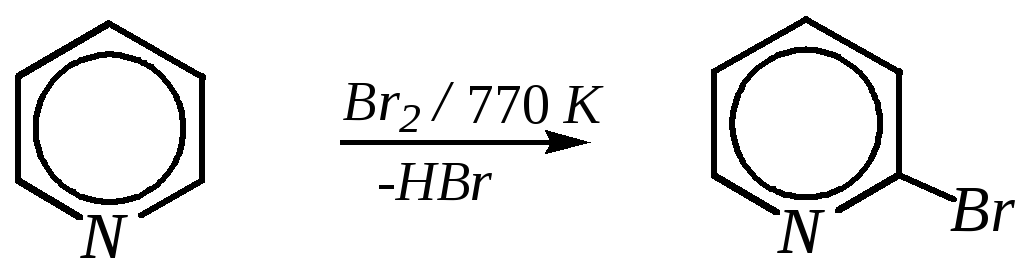
-бромпиридин
Реакции нитрования и сульфирования протекают в сильнокислой среде, поэтому первой стадией этих процессов является протонирование с образованием катиона пиридиния, что в свою очередь ещё в большей степени замедляет электрофильное замещение.
При нитровании повышение температуры выше 570 К (640 К) приводит к смене механизма с SE на SR. При этом вместо -нитропиридина образуется преимущественно -производное:
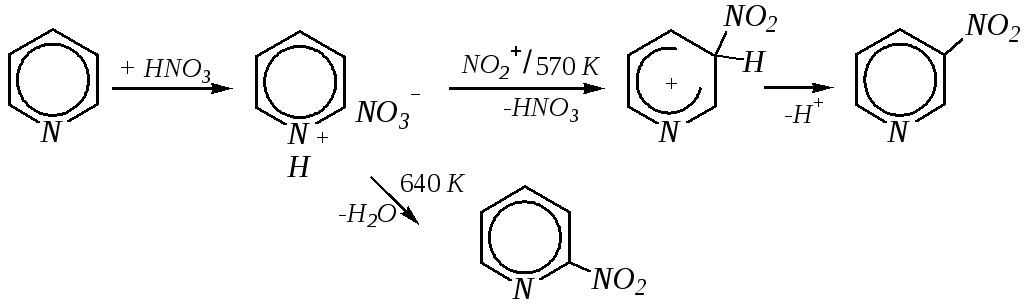
Сульфирование пиридина при 630 К даёт -пиридинсульфокислоту, существующую преимущественно в виде внутренней соли:
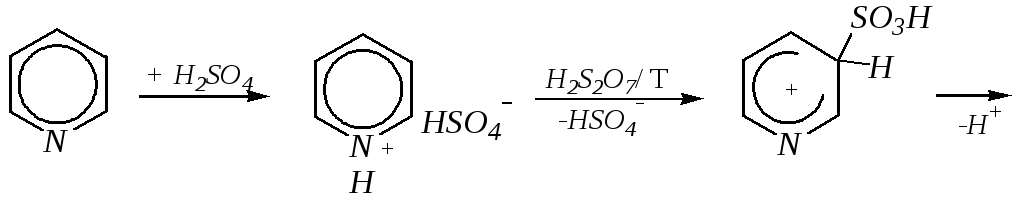
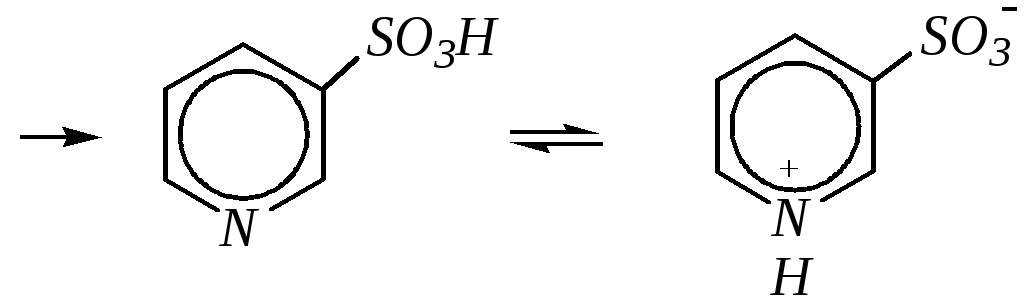
Некоторые другие типичные реакции электрофильного замещения, например, реакции алкилирования и ацилирования по Фриделю–Крафтсу, вовсе не характерны для пиридина, но такие реакции невозможны и для производных бензола с сильными электроноакцепторными группами (например, для нитробензола).
12.4.3.4. Реакции нуклеофильного замещения
Наличие атома азота в ароматическом кольце пиридина существенно понижает -электронную плотность, и становится возможной нуклеофильная атака по атому углерода в -положении (и в меньшей степени в -положении). Тем не менее пиридин и его гомологи реагируют только с сильными нуклеофильными агентами.
Щёлочи реагируют с пиридином только при температуре около 670 К с образованием -гидроксипиридина, который таутомеризуется в -пиридон. Механизм реакции — SN2аром.:
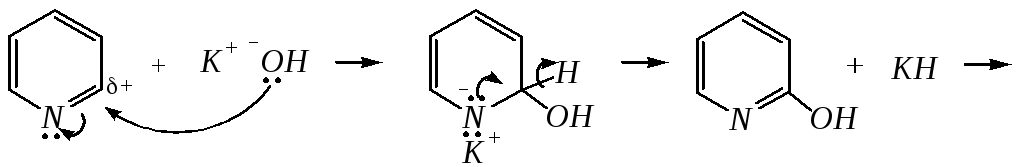
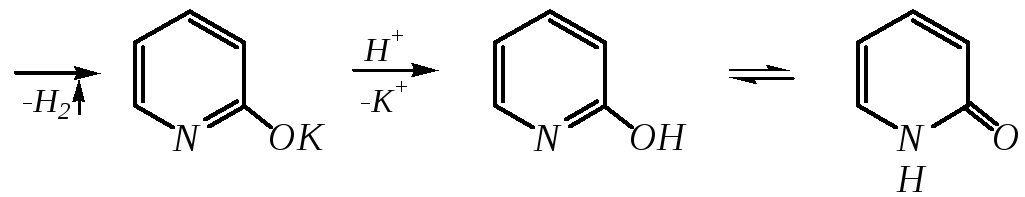
-гидроксипиридин -пиридон
Алкилирование и арилирование проводятся литийорганическими соединениями R-Li или Ar-Li при температуре 370 К. Эти реакции также селективно приводят к образованию -замещённых пиридинов. Например, взаимодействие с бутиллитием осуществляется по следующей схеме:
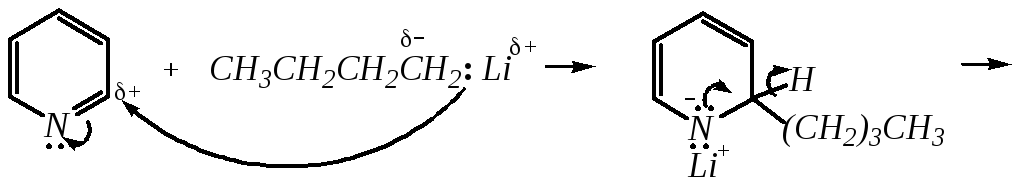
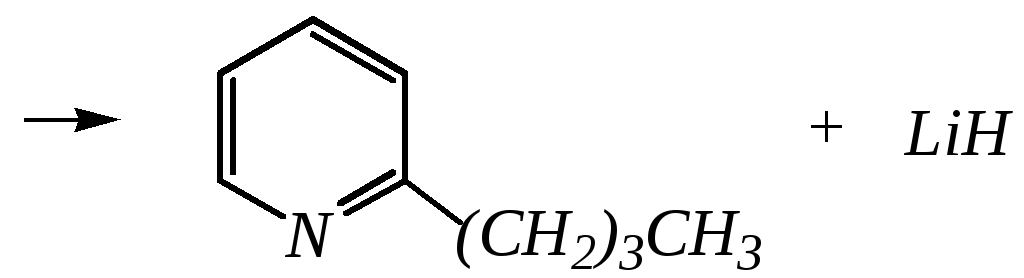
-бутилпиридин
Для отщепления гидрид-иона на стадии превращения -комплекса в продукты реакции может быть использовано окисление кислородом воздуха; тогда вместо гидрида лития образуется LiOH.
Аминирование пиридина и родственных гетероциклических соединений (реакция А.Е. Чичибабина*) осуществляется амидом натрия в апротонных растворителях при 370 К (или в жидком аммиаке при 240 К). Замещение осуществляется селективно в -положение.