
СЖ 1
.docxСӨЖ 1
Идеал және реал газдар заңдары. Термодинамиканың 1-ші заңы. Гесс заңы, оның салдары. Жылу сыйымдылық, оның температураға тәуелділігі. Химиялық реакцияның жылу эффектісінің температураға тәуелділігі. Анықтамалық әдебиеттер негізінде химиялық реакцияның жылу эффектісін әр түрлі температурада есептеу.
Термодинамиканың 2-ші заңы. Анықтамалық әдебиеттер негізінде химиялық реакцияның энтропиясының өзгерісін Т=298 К және Т298 К жағдайларында есептеу Тесттермен жұмыс жасау.
|
СH3CНO(г) + H2= C2H5OH(сұй) реакциясының тұрақты қысым және тұрақты көлем кезіндегі жылу эффектілерінің айырмасын (Дж) 298 К-де есептеңіз. |
|
|
Мg(ОН)2=МgО+ H2O(г) реакциясы 400 К және 101,3 кПа жағдайында ашық ыдыста өткенде 89,03 кДж жылу сіңіріледі. Егер реакция осы температурада, бірақ жабық ыдыста жүргізілсе, оның жылу эффектісі қандай болады? |
|
|
Ашық ыдыста 1000 К-де өтетін СаСО3=СаО+ CO2 реакциясының стандартты энтальпиясы 169,0 кДж./моль. Реакция осы температурада, бірақ жабық ыдыста жүргізілсе, оның жылу эффектісі қандай мәнге ие болады? |
|
|
2H2+CO=CH3OH
(г) (500 К) реакциясы үшін қысым 1,0133105
Па болған жағдайдағы
|
|
|
|
|
|
СО2+4H2=
CH4+
2H2O
(г) (800 К) реакциясы үшін қысым 1,0133105
Па болған жағдайдағы
|
|
|
298 К және стандартты қысым кезінде Fe2O3-тің жай заттардан түзілу жылуы -821,32 кДж/моль, ал Al2O3-тікі -1675,60 кДж/моль. Металдық алюминиймен 1 моль Fe2O3-ті тотықсыздандыру реакциясының жылу эффектісін еептеңіз. |
|
|
Буы идеал газдар заңына бағынады деп есептеп, 50 г толуол 300 С-де буланғандағы ішкі энергияның өзгірісін есептеңіз. Толуолдың меншікті булану жылуы 347,8 Дж/г. Толуолдың сұық күйдегі көлемін ескермеу керек.
|
|
|
1 кг су қалыпты қайнау температурасында буланғандағы ішкі энергияның өзгерісін есептеңіз, егер оның меншікті булану жылулығы 2258,7103 Дж/кг. Бу-идеал газ, сұйық су көлемін ескермеу керек.
|
|
|
298 К-де метанолдың булану жылуы 37,5 кДж/моль. Метанолдың 320 К-дегі булану жылуын есептеңіз. Қажетті деректерді анықтамалықтан (Қосымша І) алыңыз.
|
|
|
1. Термодинамиканың бірінші бастамасының теңдеуі қалай жазылады? 1) dQ=dU+dA. 2) Q= dU+dA. 3) TdS=dU+PdV. 4) Q=dU+A. 5) Q=dU-A.
2
Жүйенің жылу сыйымдылығының өзгерісі
оң болған жағдайда температураның
өсуімен
1) Органикалық заттар үшін азаяды; бейорганикалық заттар үшін өседі. 2) Өзгерісі реакцияға түсетін заттардың табиғатына байланысты әртүрлі болуы мүмкін. 3) Төмендейді. 4) Өзгермейді. 5) Өседі.
3. C(граф.)+O2= CO2 реакциясының жылу эффектісі тең: 1) fH0 298 (CO2) = f H0 298 C (графит) + f H0298 (O 2); 2)
3)
4)
5) барлық жауаптар дұрыс емес.
4. - Q= - dU - A теңдеуі қандай жағдайды көрсетеді? 1) Жүйеге берілген жылу жүйенің ішкі энергиясын өсіруге және жүйенің жұмыс жасауына жұмсалады. 2) Жүйенің жасаған жұмысы процестің жолына тәуелді болмайды. 3) Жүйенің жұмыс жасауы мен оның ішкі энергиясының азаюы нәтижесінде жылу бөлінеді. 4) Жылулық пен жұмыс бір-біріне эквивалентті мөлшерде айналады. 5) Барлық жауаптар дұрыс емес.
5. Төмендегі тұжырымдамалардың қайсысы дұрыс: 1) процестің жылулығы әрдайым оның жолына тәуелді; 2) тек идеал газ жүйелері үшін процестің жылулығы оның жолына тәуелсіз; 3) P=const немесе V=const жағдайда процестің жылулығы оның жүру жолына тәуелсіз; 4) бәрі процестің сипатына және оған қатысатын заттардың қасиеттеріне (табиғатына ) байланысты; 5) тек қайтымсыз процесс үшін жылулық оның жүру жолына тәуелсіз. 6. Жабық жүйе дегеніміз: 1) қоршаған ортамен жылу алмаспайтын жүйе; 2) жылу және масса алмаспайтын, көлемі өзгермейтін жүйе; 3) қоршаған ортамен масса және жылу алмасатын жүйе; 4) көлемі өзгермейтін жүйе; 5) масса алмаспайтын, бірақ қоршаған ортамен жылу алмасуы, сондай-ақ көлемі, электр заряды және т.б. өзгеруі мүмкін жүйе. 7. А+В=С реакциясы (эндотермиялық) үшін Cр>0. Реакцияның Т1 және Т2 (Т2>Т1 ) температурадағы энтальпияларының өзара қатынасы қандай ? 1)
2)
3)
4) Сұраққа жауап беру үшін келтірілген мәліметтер жеткіліксіз. 5) Температураның әсері тек заттың табиғатымен аңықталады.
8. Нитробензолдың (C6H5NO2 ) 1 молі түзілуінің жылулығы қандай химиялық реакцияның жылу эффектісі? 1) 6C(қ)+5H+O2+N= C6H5NO2(с). 2) CO2+H2O(г)+0,5N2= C6H5NO2(с). 3) C6H5NO2=6C(қ)+2,5H2+N+O2. 4) 6C(граф)+2,5H2+0,5N2+O2= C6H5NO2(с). 5) CO2+H2O(с)+NO2= C6H5NO2(с). 9. Химиялық реакцияның энтальпиясын (rHO) тәжірибе жүзінде анықтауға бола ма? 1) Жоқ, бұл шама тек теория жүзінде ғана есептелінеді. 2) Ол берілген жүйені құрайтын заттардың қасиеттеріне байланысты. 3) Болады, себебі термодинамиканың 1-ші заңы бойынша Р=const жағдайда Н=Qр. 4) Болмайды, себебі компоненттердің түзілу энтальпиясының абсолюттік шамасы белгісіз. 5) Болады, себебі Гесс заңы бойынша Р=const жағдайда U=Qр.
10. 1A1+…+ іAі=p1B1+…+ pjBj реакциясының жылу эффектісі: 1)
2)
3)
4)
5) барлық жауаптар дұрыс емес.
11. C6H5NO2 затының стандартты жану жылулығы осы заттың 1 молінің стандартты жағдайда (T=298, P=1 атм) тотығу реакциясының жылу эффектісі, реакция барысында қандай өнімдер түзіледі? 1) CO2+H2O(г)+NO2. 2) CO2+H2O(с)+N2. 3) CO+H2O(г)+NH3. 4) C+H2+NO2. 5) H2O(с)+ CO+ CO2+ NO5. 12. Тәжірибе жүзінде табылған Гесс заңы ылғида орындала ма? 1) Орындалуы ықтимал, себебі оның жарамсыздығы тәжірибие жүзінде аңықталған жоқ. 2) Ылғи орындалмайды, бірақ химиялық реакцияның көпшілігі үшін орындалады. 3) Компонеттері бірдей агрегаттық күйде болатын реакциялар үшін ғана орындалады. 4) Химиялық реакция тұрақты көлемде немесе тұрақты қысымда жүрсе ғана орындалады: Qv=U немесе Qp=H, ішкі энергия мен энтальпия процестің жүру жолына тәуелсіз. 5) Барлық жауаптар дұрыс емес.
13.
Қандай жағдайларда
1) Газ фазада моль саны өзгермей өтетін реакциялар үшін немесе конденсирленген жүйе ұшін. 2) Тек идеал газ жүйелері үшін. 3) Тек идеал сұйық жүйелер үшін. 4) Тек идеал кристалдар үшін. 5) Мұндай қатынас ешқашан орындалмайды.
14. Термодинамиканың 1-ші бастамасының тендеуі қайсысы? 1) Q=U+A. 2) Q=U+A. 3) Q=U+A. 4) Q=U+A. 5) Q=U+A.
15. Химиялық реакцияның ішкі энергиясының өзгерісін тәжірибе жолымен анықтауға бола ма? 1) Жоқ, бұл күй функциясы және оның өзгерісін тек есептеу арқылы анықтауға болады. 2) Болады, бірақ тек жоғары температурадағы идеал газдар үшін. 3) Болады, себебі U=Qv,V=const болғанда процестің жылу эффектісін анықтау керек. 4) Барлығы заттардың табиғатына және олардың агрегаттық күйіне байланысты. 5) Ешқандай жағдайда болмайды.
16. Оқшауланған жүйе дегеніміз: 1) сыртқы ортадан бөлініп тұратын шекаралары бар жүйе; 2) қоршаған ортамен тек жылу энергиясымен алмаса алатын жүйе; 3) температураның тұрақты жағдайында сыртқы ортамен зат бойынша ғана алмаса алатын жүйе; 4) бүкіл әлемнің бір бөлігі ғана қарастырылатынын көрсететін дерексіз ұғым; 5) барлық жауаптар дурыс емес .
17. Бір компонентті жүйенің күй параметрлері ретінде P,V және T алынса, онда оның күй теңдеуі жалпы түрде қалай жазылады? 1) PV= f(T). 2) P= f(T). V= f(T). 3) PV= const. 4) f(P,V,T)=0. 5) Келтірілген мәліметтер жеткіліксіз.
18. Қандай жүйелер ашық жүйеге жатады? 1) Термиялық тепе-теңдіктегі жүйелер. 2) Қоршаған ортамен жылу және зат алмасатын жүйелер. 3) Компоненттері реал сұйық ерітінділер түзетін жүйелер. 4) Қоршаған ортамен жылу алмасатын жүйелер. 5) Бір-бірімен зат алмасатын жүйелер.
19. Қандай жағдайда жүйенің ішкі энергиясының өзгерісі толығымен жылуға айналады? 1) Жүйеде жұмыс жасалмаса. 2) Жүйеге сырттан жұмыс жұмсалса. 3) Жүйе ашық жүйе болса. 4) Жүйе жұмыс өндірсе. 5) Оқшауланған жүйе болса.
20. Химиялық реакция жүретін жүйенің жылу сыйымдылығының өзгерісі бойынша нені аңықтауға болады? 1) Химиялық реакцияның бағытын. 2) Реакция өнімінің түзілу жылулығының температуралық коэффицентін. 3) Химиялық реакция өнімдерінің шығымын. 4) Химиялық реакция компоненттерінің кез келген температурадағы жылу сыйымдылықтарын. 5) Химиялық реакцияның жылу эффектісінің температуралық коэффициентін.
21. Қандай процестің жұмысы оның жүру жолына тәуелді емес? 1) Изобаралық. 2) Изохоралық. 3) Изотермиялық. 4) Тепе-теңдік процестің. 5) Барлық жауаптар дұрыс емес: жұмыс әрдайым процестің жүру жолына тәуелді.
22. Қатты, сұйық немесе газ тәрізді заттардың ерітіндіге айналған кезінде энтальпияның өзгерісін қалай деп атайды? 1) Фазалық ауысу жылулығы немесе энтальпиясы (балқу, булану, возгонка (бірден булану) және т.б. фазалық өзгерістер). 2) Еру жылулығы немесе еру энтальпиясы. 3) Сұйылту жылулығы немесе сұйылту энтальпиясы. 4) Химиялық реакция жылулығы немесе энтальпиясы. 5) Барлық жауаптар дұрыс емес.
23. Идеал газдар үшін Сp мен Сv қалай байланысты? 1) Сv = Сp - R. 2) Сv = Сp + R. 3) Сp = Сv - R. 4) Сp = Сv+ R/2. 5) Сp = Сv.
24. Еріткіштің кез келген мөлшерінде 1 моль зат еріген кездегі энтальпияның өзгерісі қалай аталады? 1) Интегралдық еру энтальпиясы. 2) Интегралдық сұйылту энтальпиясы. 3) Дифференциалдық еру жылулығы. 4) Парциалдық сұйылту жылулығы. 5) Дифференциалдық сұйылту жылулығы.
25. Суретте көрсетілген жүйе сипаттамаларының қайсысы дұрыс?
1) Реакция жылу сінірілуімен жүреді, (rHOT / T)р =0. 2) Реакция жылу бөлінуімен жүреді, Сp=0.
3)
4)
5)
26. (NO2)2C6H3COCl-дың (хлорлы динитробензоил) стандартты түзілу жылулығы төменгі қандай бастапқы заттардың арасындағы (стандартты жағдайда) реакциясының жылу эффектісі? 1) 2NO2 + C6H6(с )+ COCl2. 2) N2+2.5O2 +7C(граф.)+0.5Cl2+1.5H2. 3) 2NO2 +CO2+ H2O(г)+ Cl2. 4) 2N+7C(граф.)+3H+Cl+5O. 5) 2NO2+C6H6(с)+CO2+HCl.
27.Суреттен нені
көруге болады?
1) Сp=0. 2) Сp=const. 3) Сp<0. 4) Сp>0. 5) Температураның берілген аралығында Сp–ның таңбасы терістен оңға өзгереді.
28. Бейорганикалық қосылыстар үшін жылу сыйымдылықтың температураға тәуелділігі қандай тендеумен өрнектеледі?
1) 2)
3) CP=a+bT+cT2+dT3.
4)
5) CP=a+bT+c`/T2.
29. Белгілі концентрациялы, шексіз көп мөлшерлі ерітіндіге 1 моль еріткіш қосылғандағы процестың жылу эффектісі қалай аталады? 1) Интегралдық сұйылту жылулығы. 2) Дифференциалдық сұйылту жылулығы. 3) Интегралдық еру жылулығы. 4) Дифференциалдық еру жылулығы. 5) Барлық жауаптар дұрыс емес.
30. Диметилсульфоксидтің (СН3)2SO (с) стандарты жану жылулығын анықтау үшін оның 1 молін стандартты жағдайда қандай заттарға дейін тотықтыру керек? 1) CO2+H2O(с)+SO2. 2) CO+H2O(г)+SO2. 3) CO2+H2O(г)+SO3. 4) CO2+H2O(с)+S. 5) CO+H+S(қ).
31. С+2Н2=СН4
реакциясы үшін Т=1000К, Р=1,0133105
Па
болғанда
1) -8,31103 Дж. 2) 8,31105 Дж. 3) 1000 Дж. 4) -1000 Дж. 5) 0.
32. Кристалдық тор энергиясын нені қолданып табамыз? 1) Рауль заңын. 2) Гиббстің фазалар ережесін. 3) Гесс заңын. 4) Борн-Хабер циклін. 5) Темкин-Шварцман әдісін.
33. Бензолдың
С6Н6 1 молінің төмендегі жану реакциясы
үшін
1) Бірдей өнімдер
түзілетін болғандықтан,
2) Реакцияның
жүру жолына тәуелсіз,
3)
4) Қатынас мына
тендеумен анықталады :
5) Бұл қатынас тек тәжірибе жүзінде анықталады.
34. Егер сұйылту кезінде жүйенің соңғы күйі шексіз сұйылтылған ерітінді болса, онда бұл процестің жылуы қалай аталады? 1) Дифференциалдық сұйылту энтальпиясы. 2) Интегралдық сұйылту энтальпиясы. 3) Толық сұйылту энтальпиясы. 4) Ақырғы еру энтальпиясы. 5) Интегралдық еру энтальпиясы.
35. Химиялық реакциясының жылу эффектісінің температураға төмендегідей тәуелділігі нені көрсетеді?
1) Жылу эффектісінің температуралық коэффициенті теріс және тұрақты болатын эндотермиялық реакция экзотермиялық реакцияға айналады.
2)
3) Экзотермиялық реакция
үшін ( 4) Реакция жылу бөле жүреді, ал оның жылу эффектісінің температуралық коэффициенті оң. 5) Эндотермиялық реакция үшін Cp таңбасын өзгертеді.
36. Теңдеулердің қайсысы дұрыс жазылмаған? 1) Cv =(U2-U1)/(T2-T1). 2) CP=(H2-H1)/(T2-T1). T2 T2 3) Cv =(CPdT)/(T2-T1). 4) CP =(CPdT) / (T2-T1). T1 T1
5) CP=QP/(T2-T1).
37. Органикалық заттар үшін жылу сыйымдылықтың температураға тәуелділігі: 1) CP=a+bT+cT2+dT3; 2) CP=A+B/T+C/T3+D`/T4; 3) CP= j CP(өнім) - і СP(б.з.); 4) CP=(H2-H1)( T2- T1); 5) CP=a+bT+c`/T2.
38. Еріткіштің кез келген мөлшерінде заттың 1 молі еріген кездегі энтальпия өзгерісі қалай аталады? 1) Аралық еру энтальпиясы. 2) Интегралдық еру энтальпиясы. 3) Дифференциалдық еру энтальпиясы. 4) Толық еру энтальпиясы. 5) Парциалдық еру энтальпиясы.
39. Белгілі концентрациялы ерітідінің шексіз көп мөлшерінде 1 моль зат еріген кездегі энтальпия өзгерісі қалай аталады? 1) Парциалдық немесе дифференциалдық еру жылулығы. 2) Интегралдық сұйылту жылулығы. 3) Аралық еру жылулығы. 4) Ақырғы еру жылулығы. 5) Толық еру жылулығы.
40. Экзотермиялық реация үшін Т1 ден Т2-ге дейінгі температура аралығында Сp>О болса, Т2 температурада бөлінетін жылудың мөлшері: 1) Т1-дегіден көп; 2) Т1-дегіден аз; 3) Т1 температурада қанша бөлінсе, Т2-де де сонша бөлінеді; 4) әртүрлі қатынаста бөлінеді; 5) дұрыс жауап беру үшін қажетті мәліметтер жеткіліксіз.
41. Жауаптардың қайсысы дұрыс?
1) Реакция жылу сінірілуімен жүреді және жылу эффектісінің таңбасы өзгермейді, процестің жылу эффектісінің температуралық коэффициенті оң болады, Cp= f(T).
2) Реакция
экзотермиялы, Cp=f(T),
(
3)
4)
5) Реакция жүргенде жылу бөлінеді, Cp= f(T), процестің жылу эффектісінің температуралық коэффициенті оң.
42. 2 моль су алдымен 300К-нен 400К-ге дейін жылып, кейін 300 К-ге дейін қайта салқындағанда энтальпиясының өзгерісі неге тең?
Егер:
Сp(с)=18
Дж/(Кмоль),
Сp(г)=8
Дж/(Кмоль),
1) 51 кДж. 2) 42 кДж. 3) –18 кДж. 4) –42 кДж. 5) 0.
43. MeCl2–нің кристалл торының энергиясы төмендегі процестердің қайсысының энтальпиясына тең? 1) MeCl2(қ)Me2+(г)+2Cl-(г). 2) MeCl2Me(г)+2Cl(г). 3) MeCl2Me2+*aq+2Cl-(aq). 4) MeCl2Me(қ)+Cl2(қ). 5) Дұрыс жауап жоқ.
44. Суретте көрсетілген жүйені төменде берілген жауаптардың қайсысы дұрыс сипаттайды?
1) (
2) ( 3) Сp<0 және температураға тәуелсіз, процестің жылу эффектісі таңбасын қарама-қарсы бағытқа өзгертеді.
4) ( 5) Барлық жауаптар дұрыс емес.
45. Мына жүйені төмендегі жауаптардың қайсысы дұрыс сипаттайды?
1) Сp>0, гHO т таңбасын өзгертеді: реакция эндотермиялықтан экзотермиялыққа айналады.
2) ( 3) Сp>0, процестін жылу эффектісі таңбасын өзгертеді.
4) (
5)
46. Бір моль зат шексіз көп мөлшерлі қаныққан ерітіндіде еріген кезде байқалатын дифференциалдық жылулық қалай деп аталады? 1) Ақырғы еру жылулығы. 2) Ақырғы интегралдық еру жылулығы. 3) Ақырғы сұйылту жылулығы. 4) Бірінші интегралдық жылулық. 5) Барлық жауаптар дұрыс емес.
47. Еріткіштің шексіз көп мөлшерінде бір моль зат еріген кездегі энтальпияның өзгерісі қалай деп аталады? 1) Толық интегралдық еру жылулығы. 2) Бірінші интегралдық еру жылулығы. 3) Ақырғы интегралдық еру жылулығы. 4) Бірінші интегралдық сұйылту жылулығы. 5) Ақырғы сұйылту жылулығы.
48. Идеал газдар үшін Сp мен Сv арасындағы айырма неге тең? 1) 9.3 Дж/(Кмоль). 2) 8.31 Дж/(Кмоль). 3) 3.418 Дж/(Кмоль). 4) 22.3 Дж/(Кмоль). 5) айырма газдардың табиғатына байланысты.
49. Тұздың еру жылулығы нөлге тең болуы нені білдіреді? 1) Идеал ерітінді түзілгенді. 2) Идеал кристалл ерігенді. 3) Тұздың кристалдық торы өте берік еместігін. 4) Иондардың гидраттану жылулығы мен кристалл тордың бұзылу жылулығы бір-біріне тең екендігін. 5) Иондардың гидраттануы болмайтынын.
50. Суреттегі жүйе үшін төменде келтірілген сипаттамалардың қайсысы дұрыс келеді?
1) Жылу сіңіру арқылы жүретін химиялық реакцияның жылу эффектісінің температуралық коэффициенті теріс. 2) Эндотермиялық реакция үшін Сp<0. 3) Химиялық реакцияның жылу эффектісінің температуралық коэффициенті оң және ол температураға тәуелді.
4) Сp=f(T),
5) (
51. Қатты дене сұйықтықта еріген кездегі энтальпия өзгерісінің таңбасы әдетте қандай? 1) Оң таңбалы, себебі кристалдық тордың бұзылуы жүреді. 2) Теріс таңбалы, өйткені кристалдық тордың бұзылуына жылу жұмсалады. 3) Кез келген таңбалы болуы мүмкін, ол қатты дене табиғатына және оның концетрациясына байланысты. 4) Таңбасы концентрацияға байлынысты: аз концентрацияда оң, жоғары концетрациялы ерітінділер үшін – кері таңбалы болады. 5) Бөлшектердің сольваттауына байланысты әрдайым теріс таңбалы болады.
52. Борн-Хабер циклі қолданылады: 1) қатты ерітінділерге; 2) газдарға; 3) кристалды қосылыстарға; 4) идеал сұйық ерітінділерге; 5) бейэлектролит ерітінділерге.
53. Бірдей жағдайда жүргізілген 1 және 2 бейтараптану реакцияларының тәжірибе жүзінде анықталған жылу мөлшерлерінің абсолютті мәндерінің арасындағы байланыс қандай? 1. Күшті сілті +күшті қышқыл = тұз +су, Н1 2. Күшті сілті + әлсіз қышқыл= тұз + су, Н2 1) Н1 =Н2, себебі екі жағдайда да бірдей өнімдер - су мен тұз түзіледі. 2) Н1 >Н2, өйткені 1-ші реакция әрдайым тереңірек жүреді. 3) Н2>Н1, себебі 2-ші реакцияда әлсіз қышқылдың диссоциациялану жылулығы бөлінеді. 4) Н1>Н2, себебі әлсіз қышқылдың диссоциациясы жылу сіңіре жүреді. 5) барлық жауаптар дұрыс емес.
54. Химиялық реакцияның Т температурадағы жылу эффектісі қалай белгіленеді?
1)
55. Интенсивті шамалар дегеніміз; 1) заттың массасына тәуелді шамалар; 2) кез келген шамалар, мысалы V, Р, Т, себебі - бұлардың мәндерін тікелей өлшеуге болады; 3) заттың сәулелену интенсивтілігіне тәуелді шамалар; 4) зат массасына тәуелсіз шамалар; 5) барлық жауаптар дұрыс емес.
56. Жылу қандай жағдай үшін процестің жүру жолына тәуелсіз болды? 1) T=const үшін. 2) P=const үшін. 3) Оқшауланған жүйе үшін. 4) Ашық жүйе үшін. 5) Жылу әрдайым процестің жүру жолына тәуелді.
57. Заттың булану энтальпиясының
1) әрдайым оң таңбалы; 2) теріс таңбалы; 3) таңбасы заттың табиғатына байланысты; 4) төмен қысымда оң, ал қысымның өсуімен теріс таңбалы; 5) таңбасы сұйықтың қайнау температурасына байланысты.
58. Заттың стандартты булану жылулығы қалай белгіленеді?
1)
59. Үшфторсірке қышқылының CF3COOH стандартты жану жылулығы дегеніміз - оның бір молінің оттекпен тотығу реакциясының жылу эффектісі. Тотығу реакциясы барысында қандай өнімдер түзіледі? 1) CO+CO2+H2O(с)+F2. 2) CHF3+H2O(г)+CO2. 3) CH2F2+CO2+H2O(с). 4) CO2+H2O(с)+HF(г). 5) CO2+HF.
60. Егер жылу жүйеден қоршаған ортаға ауысса, онда: 1) жүйенің әсерінен қоршаған ортада бөлшектердің ретсіз қозғалысы туады; 2) қоршаған ортаның әсерінен жүйеде бөлшектердің ретті қозғалысы туады; 3) қоршаған ортаның жүйеге әсерінен бөлшектердің ретсіз қозғалысы туады; 4) жүйенің әсерінен сыртқы ортада бөлшектердің қозғалысы реттеледі; 5) дұрыс жауап жоқ.
61. Төменде берілген тендеулердің қайсысы қате жазылған?
1)
2)
3)
4)
5)
62. Суреттегі жүйе үшін төменде берілген сипаттамалардың қайсысы дұрыс?
1) Жылу эффектісінің температуралық коэффициенті эндотермиялық реакция үшін теріс таңбалы, Сp=f(T).
2)
3)
4) Реакция экзотермиялы, компоненттердің жылу сыйымдылығы температураға тәуелді емес, жылу эффектісінің температуралық коэффициенті теріс. 5) Сp<0, температураға тәуелсіз, процестің жылу эффектісі таңбасын өзгертеді.
63. Қайсы тендеу дұрыс емес? 1) A=P(V2-V1). 2) A=RT. 3) A=RTln(V2/V1). 4) A=RTln(P2/P1). 5) A=Cv(T1-T2).
64. 2A+3B= C+2F реакциясы үшін жылу сыйымдылықтың өзгерісі қандай тендеумен есептеледі? 1) CP = CP (C)+CP(F)- CP(B) - CP(A). 2) СP = CP(C)+2CP(F) - 3CP(B) - 2CP(A). 3) CP = CP(C)+CP2 (F) - CP3 (B) - CP2 (A). 4) CP = CP2 (A)+CP3 (B) - CP(C) - CP2 (F). 5) CP = CP(C)+2CP(F) - 2CP(A) - 3CP(B).
65. Химиялық реакцияның жылу эффектісінің температуралық коэффициенті қандай тендеумен анықталады ?
1) Ле-Шателье
теңдеуі:
2) Вант- Гоффтың
изобарасы :
3) Кирхгоффтың теңдеуі: (H/T)p=Сp. 4) Сp=vj Сp(өнім)-і Сp(б.з).
5) Клапейрон-Клаузиус
теңдеуі: dP/dT= 66. Кирхгофф тендеуі дегеніміз: 1) (H/T)p=Сp 2) Сp=pjСp(өнім)-vіСp(б.з.) 3) Сp=Сv+R 4) H=Qp 5) U=Qv
67. Жылулық дегеніміз: 1) энергия ауысу тәсілдерінің бір түрі; 2) энергияның бір түрі; 3) энергияның сақталу формасы; 4) энергияны сақтаудың практикалық қолайлы тәсілі; 5) энергияның ең көп таралған түрі.
68. Судың меншікті және молдік жылу сыйымдылықтарының арасындағы байланыс қандай? 1) Сp(мен) <Сp /2. 2) Сp >Сp(мен). 3) Сp =Сp(мен) . 4) Сp =18Сp(мен). 5) Сp(мен) =18Сp.
69. Егер жұмыс жүйеге істелсе, онда: 1) бөлшектердің қозғалысы қоршаған ортада ретті, ал жүйде ретсіз; 2) сыртқы ортадағы бөлшектердің қозғалысы жүйе әсерінен ретті болады; 3) жүйедегі бөлшектердің қозғалысы қоршаған ортаның әсерінен ретті; 4) жүйеде бөлшектердің қозғалысы ретсіз, ал қоршаған ортада ретті; 5) дұрыс жауап жоқ. _ 70. Идеал газдар үшін нақты (шынайы) (Сp) және орташа (Сp) жылу сыйымдылықтары арасында қандай байланыс бар? _ _ _ 1) СР >Cp. 2) CP = Cp. 3) CP < Cp. 4) байланыс кез келген болуы мүмкін. 5) CP -Сp = R.
71. Егер Сp>0 болса, онда экзотермиялық реакция үшін Т1 және Т2 кезінде жылу эффектілердің абсолюттік шамалары өзара қандай қатынаста болады?
1)
2)
3)
4) Сұраққа жауап беру үшін мәліметтер жеткіліксіз. 5) Бәрі нақты реакцияға байланысты.
|
|

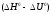 айырымын
есептеңіз.
айырымын
есептеңіз. S2+
2H2O
(г)=SO2+2H2
(900 К) реакциясы үшін қысым 1,0133105
Па болған жағдайдағы
S2+
2H2O
(г)=SO2+2H2
(900 К) реакциясы үшін қысым 1,0133105
Па болған жағдайдағы
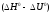 айырымын
есептеңіз.
айырымын
есептеңіз.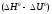 айырымын
есептеңіз.
айырымын
есептеңіз.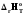 қалай өзгереді?
қалай өзгереді? =
=
 (CO
2);
(CO
2); =
=
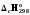 (CO2)
-
(CO2)
-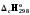 (O2)
-
(O2)
- (Cграф.);
(Cграф.);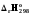 =
=
 (CO2);
(CO2);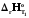 =
=
 .
. >
>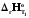 .
. 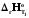 >
> .
. =
=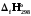 (өнім)-
(өнім)-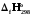 (б.з.);
(б.з.);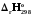 =
pj
=
pj
 (Bj)-і
(Bj)-і
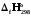 (Aі);
(Aі); =і
=і
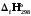 (б.з.)-pjfHO298
(өнім);
(б.з.)-pjfHO298
(өнім);
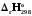 =і
=і (б.з.)-pj
(б.з.)-pj (өнім);
(өнім); =
=
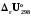 ?
?
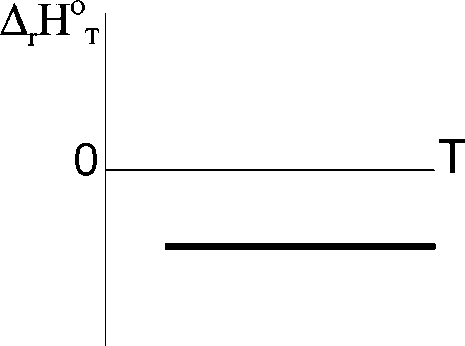
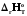 <
0, CP>0.
<
0, CP>0.
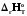 >
0, CP>0.
>
0, CP>0.
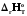 <
0, CP=f(T).
<
0, CP=f(T).
 =(CPdT)/(T2-T1).
=(CPdT)/(T2-T1). =
= +
CP(
T2-T1).
+
CP(
T2-T1). =
A+BT+CT2+DT3.
=
A+BT+CT2+DT3.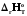 мен
мен
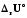 -дың
арасындағы айырма неге тең?
-дың
арасындағы айырма неге тең? және
және
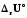 арасындағы қатынас қандай болады?
С6Н6+7,5O2=6CO2+3H2O.
арасындағы қатынас қандай болады?
С6Н6+7,5O2=6CO2+3H2O.
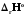 =
=
 ;
;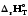 әрдайым rUOT
шамасынан үлкен болады, оны мына
тендеуден көруге болады
әрдайым rUOT
шамасынан үлкен болады, оны мына
тендеуден көруге болады
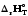 =
=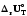 +
РV;
+
РV;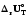 шамасы
шамасы
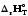 -ға
қарағанда әрдайым үлкен;
-ға
қарағанда әрдайым үлкен;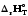 =
=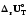 +RT,
мұнда
шамасы тәжірибе жүзінде су буы сұйыққа
айнала ма әлде айналмай ма соған
байланысты анықталады;
+RT,
мұнда
шамасы тәжірибе жүзінде су буы сұйыққа
айнала ма әлде айналмай ма соған
байланысты анықталады;
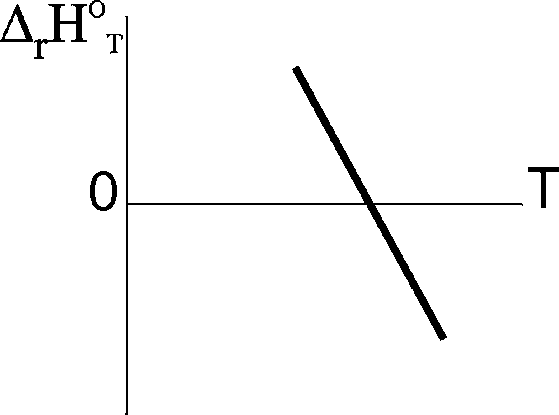
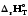 >0,
Cp>0
және температураға тәуелді.
>0,
Cp>0
және температураға тәуелді.
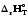 /T)р<0
.
/T)р<0
.
 /T)р<0.
/T)р<0.
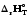 >0,
Cp=const,
(
>0,
Cp=const,
(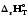 /T)р>0.
/T)р>0. <0,
Cp=const,
(
<0,
Cp=const,
(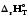 /T)р<0.
/T)р<0.
 =451
Дж/моль
=451
Дж/моль
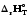 /Т)р>0,
Сp=const,
жылу эффектісі таңбасын өзгертеді.
/Т)р>0,
Сp=const,
жылу эффектісі таңбасын өзгертеді.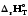 /Т)р<0,
Сp=f(T).
/Т)р<0,
Сp=f(T).
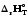 /Т)р<0,
Cp=
f(T), реакция экзотермиялықтан
эндотермиялыққа айналады.
/Т)р<0,
Cp=
f(T), реакция экзотермиялықтан
эндотермиялыққа айналады.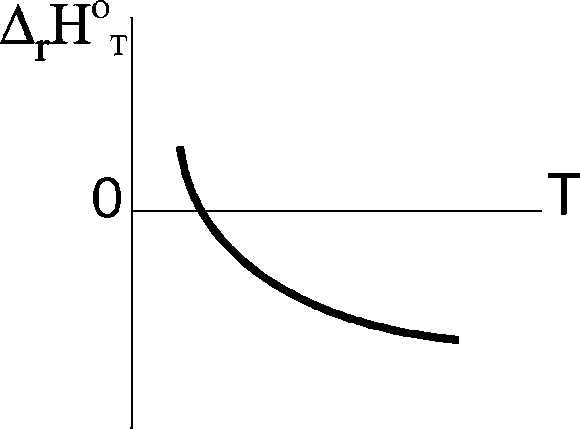
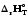 /Т)р<0,
Сp=f(T),
процестің жылу эффектісі таңбасын
өзгертеді: реакция эндо-дан экзотермиялыққа
айналады.
/Т)р<0,
Сp=f(T),
процестің жылу эффектісі таңбасын
өзгертеді: реакция эндо-дан экзотермиялыққа
айналады.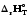 /Т)р<0,
Сp=const.
/Т)р<0,
Сp=const.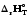 /Т>0,
Сp=const
температураның жоғарлауымен реакция
экзотермиялықтан эндотермиялыққа
ауысады.
/Т>0,
Сp=const
температураның жоғарлауымен реакция
экзотермиялықтан эндотермиялыққа
ауысады.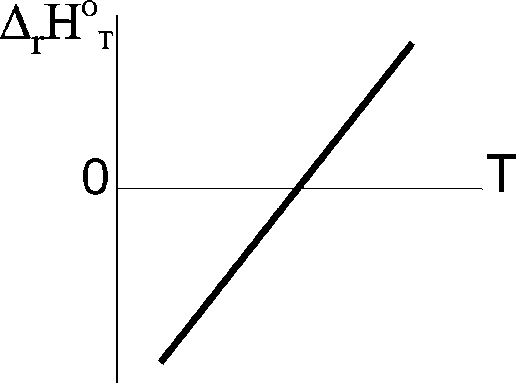
 <0.
<0. /Т)р>0,
Сp=const,
реакция экзотермиялықтан эндотермиялыққа
ауысады.
/Т)р>0,
Сp=const,
реакция экзотермиялықтан эндотермиялыққа
ауысады.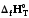 .
2)
.
2)
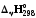 .
3)
.
3)
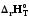 .
4)
.
4)
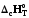 .
5)
.
5)
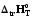 .
.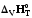 өзгерісі:
өзгерісі: .
2)
.
2)
 .
3)
.
3)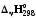 .
4)
.
4)
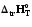 .
5)
.
5)
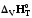 .
.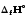 (г)
=
(г)
=
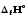 (қ)+
(қ)+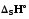 .
.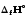 (г)
=
(г)
=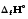 (с)+
(с)+
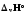 .
.
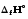 (с)=
(с)=
 (қ)+
(қ)+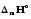 .
.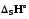 =
=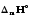 +
+ .
.
 (г)
=
(г)
=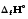 (с)+
(с)+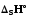 .
.
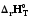 >0,
(
>0,
(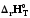 /Т)р>0,
Сp=const.
/Т)р>0,
Сp=const.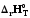 <0,
(
<0,
( /Т)р>0,
Сp=
f(T).
/Т)р>0,
Сp=
f(T).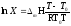 .
. .
.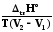 .
.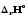 (T1)>
(T1)>
 (T2).
(T2). (T1)<
(T1)<
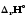 (T2).
(T2).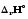 (T1)=
(T1)=
 (T2).
(T2).