
- •060301 Дневник
- •Табель посещаемости аптеки.
- •Анализ воды очищенной по фс - 42 – 26 – 20 – 97 и приказу №214.
- •Положение о химике-аналитике аптеки
- •Должностная инструкция Провизора-аналитика
- •II.Функции
- •Оснащение рабочего места провизора – аналитика
- •Правила хранения лекарственных средств
- •I. Общие положения
- •II. Общие требования к устройству и эксплуатации помещений
- •III. Общие требования к помещениям для хранения лекарственных средств и организации их хранения
- •IV. Требования к помещениям для хранения огнеопасных и взрывоопасных лекарственных средств и организации их хранения
- •V. Особенности организации хранения лекарственных средств в складских помещениях
- •VI. Особенности хранения отдельных групп лекарственных средств в зависимости от физических и физико-химических свойств, воздействия на них различных факторов внешней среды
- •16. 04. 2012 Анализ натрия гидрокарбоната
- •Анализ натрия хлорида
- •17.04.2012 Анализ натрия бромида
- •Анализ магния сульфата
- •18.04.2012 Анализ кислоты борной
- •Анализ кальция хлорида
- •19.04.2012 Анализ кальция хлорида
- •20.04.2012
- •23.04.2012 Анализ натрия бромида
17.04.2012 Анализ натрия бромида
Rp.: Natrii bromidi 1,0
Magnesii sulfatis 1,0
Aquae purificatae 100 ml
D.S.:
Виды контроля:
Обязательные:
Письменный;
Органолептический;
При отпуске.
Выборочные:
Физический;
Опросный;
Химический.
Письменный.
Aquae purificatae 100 ml
Natrii bromidi 1,0
Magnesii sulfatis 1,0
Vоб = 100 ml
Лукьянова 17.04.2012
Органолептический – бесцветная прозрачная жидкость, без запаха, без механических включений.
Химический.
Качественный с AgNO3
NaBr + AgNO3 = AgBr↓ + NaNO3
Светло – желтый осадок
2 AgNO3 + К2CrO4 = Ag2 Cr O4↓ + 2К NO3
Розовый осадок
Количественный: Метод Аргентометрии, так как галогенид с нитратом серебра образует малодиссациируемое соединение бромид серебра.
К т.н. 0.5мл добавляем индикатор хромат калия и титруем AgNO3 до светло – желтого окрашивания.
NaBr + AgNO3 = AgBr↓ + NaNO3
Светло – желтый осадок
2 AgNO3 + К2CrO4 = Ag2 Cr O4↓ + 2К NO3
Розовый осадок
Т = С * М = 0.1 * 102.90 = 0.01029 г/мл
1000 1000
W = VT * K * T * 100% = 0.48 * 1 * 0.01029 * 100% = 0.98 %
Т.н. 0.5
Х = VT * K * T * 100 = 0.48 * 1 * 0.01029 * 100 = 0.98 г
Т.н. 0.5
– 100 мл
Z = +- 6
1.0 – 100% = 2%
0.98 – 98 %
Контроль при отпуске: Этикетка «Внутреннее» с зеленой маркировкой, дополнительная «Хранить в прохладном, защищенном от света месте».
Вывод: лекарственная форма удовлетворяет требованиям ГФ XI.
Анализ магния сульфата
Rp.: Natrii bromidi 1,0
Magnesii sulfatis 2,0
Aquae purificatae 100 ml
D.S.:
Виды контроля:
Обязательные:
Письменный;
Органолептический;
При отпуске.
Выборочные:
Физический;
Опросный;
Химический.
Письменный.
Aquae purificatae 100 ml
Natrii bromidi 1,0
Magnesii sulfatis 2,0
Vоб = 100 ml
Лукьянова 17.04.2012
Органолептический – бесцветная прозрачная жидкость, без запаха, без механических включений.
Химический.
Качественный с BaCl2
MgSO4 + BaCl2 = BaSO4↓ + MgCl2
Белая муть
Количественный: комплексонометрия, образование комплексосоединения.
К т.н. 0.5мл добавляем 4кап аммиачного буфера, добавляем индикатор хром темно – синий и титруем трилоном Б до красно – фиолетового окрашивания.
CH2COONa
CH2COONa

N
CH2COOH
N CH2COO



CH2 + MgSO4 = CH2 Mg + H2SO4

CH2 CH2
N
CH2COOH
N CH2COO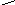


CH2COONa
CH2COONa

Т = С * М = 0.1 * 246.48 = 0.0246 г/мл
1000 1000
W = VT * K * T * 100% = 0.43 * 1 * 0.0246 * 100% = 2.11 %
Т.н. 0.5
Х = VT * K * T * 100 = 0.43 * 1 * 0.0246 * 100 = 2.11 г
Т.н. 0.5
– 100 мл
Z = +- 5
2.0– 100% = 5%
2.11 – 105 %
Контроль при отпуске: Этикетка «Внутреннее» с зеленой маркировкой, дополнительная «Хранить в прохладном, защищенном от света месте».
Вывод: лекарственная форма удовлетворяет требованиям ГФ XI.
