
- •60 Химическое строение и свойства витамина b1
- •Нехватка витамина b1, причины, симптомы
- •Нарушение обмена тиамина в организме
- •Суточная потребность в витамине b1, пищевые источники витамина b1
- •Продукты, богатые витамином b1
- •Химическое строение и свойства витамина b2 (рибофлавина)
- •Биохимические свойства витамина b2
- •Гиповитаминоз и гипервитаминоз витамина b2 Гиповитаминоз
- •Гипервитаминоз
- •Метаболизм пантотеновой кислоты (витамина b3)
- •Биохимические функции пантотеновой кислоты
- •Гиповитаминоз и гипервитаминоз пантотеновой кислоты
- •Суточная потребность и пищевые источники пантотеновой кислоты
- •Продукты, богатые пантотеновой кислотой (витамином b3)
- •Химическое строение и свойства витамина pp
- •Метаболизм витамина pp
- •Биохимические функции никотиновой кислоты
- •Гиповитаминоз витамина b5
- •Гипервитаминоз витамина b5
- •Оценка обеспеченности организма витамином pp
- •Суточная потребность и пищевые источники витамина b5
- •Продукты,богатые витамином pp (b5)
- •Гиповитаминоз пиридоксина (витамина b6)
- •Гипервитаминоз пиридоксина (витамина b6)
- •Врожденные нарушения обмена витамина b6
- •Гомоцистинурия
- •Цистатионинурия
- •Наследственная ксантуренурия (синдром Кнаппа)
- •Пиридоксинзависимый судорожный синдром
- •Пиридоксинзависимая анемия
- •Суточная потребность в витамине b6, пищевые источники пиридоксина
- •Метаболизм фолиевой кислоты
- •Биохимические функции и свойства витамина b9
- •Гиповитаминоз фолацина
- •Врождённые нарушения обмена витамина b9
- •Обеспеченность организма фолиевой кислотой
- •Суточная потребность в витамине b9, пищевые источники фолиевой кислоты
- •Продукты,богатые витамином b9
- •Химическое строение и свойства витамина b12 (кобаламина)
- •Метаболизм кобаламина в организме
- •Биохимические свойства и функции кобаламина (b12)
- •Недостаток кобаламина (витамина b12) в организме
- •Избыток витамина b12
- •Как проводят оценку?
- •Суточная потребность витамина b12, пищевые источники кобаламина
- •Продукты,богатые витамином b12
- •Химическое строение и свойства витамина h
- •Метаболизм биотина (витамина h)
- •Биохимические функции биотина
- •Врожденные нарушения обмена биотина, гипервитаминоз и гиповитаминоз витамина h Гиповитаминоз
- •Врожденные нарушения обмена биотина
- •Суточная потребностьи пищевые источники биотина
- •Продукты,богатые витамином h
- •Витамин с (аскорбиновая кислота), химическое строение и свойства
- •Метаболизм аскорбиновой кислоты в организме
- •Биохимические функции аскорбиновой кислоты
- •Гиповитаминоз и гипервитаминоз аскорбиновой кислоты Гиповитаминоз
- •Суточная потребность и источники аскорбиновой кислоты
- •Продукты, богатые витамином c
- •Химическое строение и свойства витамина а.
- •Метаболизм витамина а в организме человека
- •Биохимические функции ретинола
- •Участие витамина а в процессе зрения
- •Участие витамина а в антиоксидантной защите организма
- •Гиповитаминоз и гипервитаминоз ретинола Гиповитаминоз витамина а
- •Гипервитаминоз витамина а
- •Оценка обеспеченности организма ретинолом
- •Врожденные нарушения обмена ретинола
- •Суточная потребность витамина а, пищевые источники витамина а
- •Продукты, богатые витамином а
- •Химическое строение и свойства каротинов (провитаминов а)
- •Биохимические функции провитаминов а
- •Суточная потребность и пищевые источники каротинов
- •Продукты, богатые каротинами
- •Химическое строение и свойства витамина е
- •Метаболизм токоферола
- •Биохимические функции токоферола
- •Гиповитаминоз токоферола
- •Гипервитаминоз токоферола
- •Врождённые нарушения обмена токоферола
- •Оценка обеспеченности организма витамином е
- •Суточная потребность и пищевые источники токоферола
- •Продукты, богатые витамином е
- •Витамин д (кальциферол), химическое строение и свойства
- •Метаболизм витамина д
- •Биохимические функции кальциферола
- •Гиповитаминоз витамина д
- •Врожденные нарушения обмена кальциферола Семейный гипофосфатемический витамин-д-резистентный рахит.
- •Врожденный псевдодефинитный витамин-д-зависимый рахит.
- •Гипервитаминоз витамина д
- •Суточная потребность в витамине д и его источники
- •Метаболизм и биохимические функции витамина k Метаболизм витамина к
- •Биохимические функции витамина к
- •Недостаточность витамина к
- •Врожденные нарушения обмена витамина к
- •Оценка обеспеченности организма витамином к, суточная потребность
- •Продукты богатые витамином к
- •Метаболизм витамина f метаболизм витамина f
- •Биохимические функции витамина f
- •Недостаточность витамина f
- •Суточная потребность и источники витамина f
- •Продукты богатые витамином f
- •Химическое строение и свойства инозита (витамина b8)
- •Метаболизм витамина b8 (инозита)
- •Суточная потребность и источники витамина b8
- •Недостаточность карнитина
- •Потребность и пищевые источники липоевой кислоты
- •Потребность и источники парааминобензойной кислоты.
- •Суточная потребность и пищевые источники рутина
- •Продукты, богатые витамином p
60 Химическое строение и свойства витамина b1
Витамин В1, был первым витамином, выделенным в кристаллическом виде К. Функом в 1912 г. Позже был осуществлен его химический синтез. Свое название — тиамин — получил из-за наличия в составе его молекулы атома серы и аминогруппы.

Тиамин состоит из 2-х гетероциклических колец — аминопиримидинового и тиазолового. Последнее содержит каталитически активную функциональную группу — карбанион (относительно кислый углерод между серой и азотом). Тиамин хорошо сохраняется в кислой среде и выдерживает нагревание до высокой температуры. В щелочной среде, например при выпечке теста с добавлением соды или карбоната аммония, он быстро разрушается.
В желудочно-кишечном тракте различные формы витамина гидролизуются с образованием свободного тиамина. Большая часть тиамина всасывается в тонком кишечнике с помощью специфического механизма активного транспорта, остальное его количество расщепляется тиаминазой кишечных бактерий. С током крови всосавшийся тиамин попадает вначале в печень, где фосфорилируется тиаминпирофосфокиназой, а затем переносится в другие органы и ткани.

Существует мнение, что основной транспортной формой тиамина является ТМФ.

Витамин В1, присутствует в различных органах и тканях как в форме свободного тиамина, так и его фосфорных зфиров: тиаминмонофосфата(ТМФ), тиаминдифосфата (ТДФ, синонимы: тиамин пирофосфат, ТПФ, кокарбоксилаза) и тиаминтрифосфата (ТТФ).
ТТФ — синтезируется в митохондриях с помощью фермента ТПФ-АТФ-фосотрансферазы:

Основной коферментной формой (60—80 % от общего внутриклеточного) является ТПФ. ТТФ играет важную роль в метаболизме нервной ткани. При нарушении его образования развивается некротизирующая энцефалопатия. После распада коферментов свободный тиамин выделяется с мочой и определяется в виде тиохрома.
Витамин В, в форме ТПФ является составной частью ферментов, катализирующих реакции прямого и окислительного декарбоксилирования кетокислот.
Участие ТПФ в реакциях декарбоксилирования кетокислот объясняется необходимостью усиления отрицательного заряда углеродного атома карбонила кетокислоты в переходном, нестабильном, состоянии:
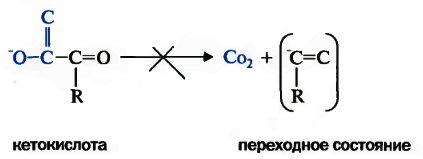
Переходное состояние стабилизируется ТПФ путем делокализаиии отрицательного заряда карбо-аниона тиазолового кольца, играющего роль своеобразного электронного стока. Вследствие такого протонирования образуется активный ацетальдегид (гидроксиэтил-ТПФ).
Аминокислотные остатки белков обладают слабой способностью осуществлять то, что с легкостью делает ТПФ, поэтому апобелки нуждаются в коферменте. ТПФ жестко связан с апоферментом мульти-ферментных комплексов дегидрогеназ а-оксикетокислот (см. ниже).
Участие ТПФ в реакции прямого декарбоксилирования пировиноградной кислоты (ПВК). При декарбоксилировании ПВК с помощью пируватдекарбоксилазы образуется ацетальдегид, который под воздействием алкогольдегидрогеназы превращается в этанол. ТПФ является незаменимым кофактором пируватдекарбоксилазы. Этим ферментом богаты дрожжи.

Участие ТПФ в реакциях окислительного декарбоксилирования. Окислительное декарбоксилирование ПВК катализирует пируватде-гидрогеназа. В состав пируватдегидрогеназного комплекса входит несколько структурно связанных ферментных белков и коферментов (см. с. 100). ТПФ катализирует начальную реакцию декарбоксилирования ПВК. Эта реакция идентична катализируемой пируватдекарбоксила-зой. Однако в отличие от последней, пируватдегидрогеназа не превращает промежуточный продукт гидроксиэтил-ТПФ в ацетальдегид. Вместо этого гидроксиэтильная группа переносится к следующему ферменту в мультиферментной структуре пируватдегидрогеназного комплекса. Окислительное декарбоксилирование ПВК является одной из ключевых реакций в обмене углеводов. В результате этой реакции ПВК, образовавшаяся при окислении глюкозы, включается в главный метаболический путь клетки — цикл Кребса, где окисляется до углекислоты и воды с выделением энергии. Таким образом, благодаря реакции окислительного декарбоксилирования ПВК создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующаяся при действии ПДГ-комплек-са активная форма уксусной кислоты служит источником для синтеза многих биологических продуктов: жирных кислот, холестерина, стероидных гормонов, ацетоновых тел и других. Окислительное дскарбоксилирование а-кетоглутатарата катализирует а-кетоглутаратдегидрогеназа. Этот фермент является составной частью цикла Кребса. Строение и механизм действия а-кетоглугарат-дегидрогеназного комплекса схожи с пируватдегидрогеназой, т. е. ТПФ также катализирует начальный этап превращения кетокислоты. Таким образом, от степени обеспеченности клетки ТПФ зависит бесперебойная работа этого цикла. Помимо окислительных превращений ПВК и а-кетоглутарата, ТПФ принимает участие в окислительном декарбоксилировании кетокислот с разветвленным углеродным скелетом (продукты дезаминирования ва-лина, изолейцина и лейцина). Эти реакции играют важную роль в процессе утилизации аминокислот и, следовательно, белков клеткой.
ТПФ — кофермент транскетолазы. Транскетолаза — фермент пентозофосфатного пути окисления углеводов. Физиологическая роль этого пути заключается в том, что он является основным поставщиком NADFH*H+ и рибозо-5-фосфата. Транскетолаза переносит дву-углеродные фрагменты от ксилулозо-5-фосфата к рибозо-5-фосфату, что приводит к образованию триозофосфата (3-фосфоглицеринового альдегида) и 7С сахара (седогептулозо-7-фосфата). ТПФ необходим для стабилизации карб-аниона, образующегося при расщеплении связи С2-С3 ксилулозо-5-фосфата.
Витамин В1 принимает участие в синтезе ацетилхолина, катализируя в пируватдегидрогеназной реакции образование ацетил-КоА — субстрата ацетилирования холина.
Помимо участия в ферментативных реакциях, тиамин может выполнять и некоферментные функции, конкретный механизм которых еще нуждается в уточнении. Полагают, что тиамин участвует в кроветворении, на что указывает наличие врожденных тиаминзависимых анемий, поддающихся лечению высокими дозами этого витамина, а также в стероидогенезе. Последнее обстоятельство позволяет объяснить некоторые эффекты препаратов витамина В, как опосредованных стресс-реакцией.
Переходное состояние стабилизируется ТПФ путем дслокализаиии отрицательного заряда карб-аниона тиазолового кольца, играющего роль своеобразного электронного стока. Вследствие такого протонирования образуется активный ацетальдегид (гидроксиэтил-ТПФ).
Аминокислотные остатки белков обладают слабой способностью осуществлять то, что с легкостью делает ТПФ, поэтому апобелки нуждаются в коферменте. ТПФ жестко связан с апоферментом мульти-ферментных комплексов дегидрогеназ а-оксикетокислот (см. ниже).
