
4 курс / Общая токсикология (доп.) / Судебно_медицинская_экспертиза_отравлений_антихолинэстеразными_веществами
.pdf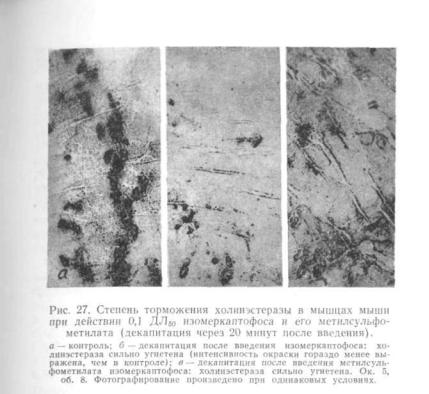
азота в четвертичный приводит к резкому изменению центрального действия, в частности исчезновению цент рального стимулирующего эффекта, свойственного само му эзерину .
При исследованиях, проведенных И. В. Семеновым и Н. К- Фруентовым (1956, 1957), было установлено, что при метилсульфометилировании изомеркаптофоса его антихолинэстеразное действие in vitro усиливается в де сятки раз.
Так же сильно возрастает и периферическое фармако логическое действие (способность вызывать бронхоспазм): у метилсульфометилата антихолинэстеразные свойства оказались приблизительно в 21 раз сильнее, чем у исходного вещества, а способность вызывать бронхоспазм возросла в 25 раз.
Отравление препаратами Гд-7 и Гд-42. На примере метилсульфометилирования изомеркаптофоса мы показа ли, что оно приводит к увеличению его токсичности в 118
119
раз, причем значительно ослабляется его действие на холинэстеразу центральной нервной системы.
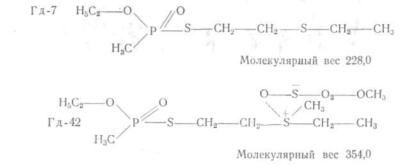
В связи с этим нам представлялось целесообразным проверить указанные закономерности на других серусодержащих ФОС. По нашей просьбе в лаборатории, руко водимой М. И. Кабачником, Института элементоорганических соединений (дир.— акад. А. Н. Несмеянов) Н. Н. Годовиковым были синтезированы новые серусодержащие фосфорорганические соединения: Гд-7 (содержа щий незаряженную двухвалентную серу) и его метилсульфометилат — Гд-42 (содержащий положительно заряжен ную трехковалентную серу).
Препарат Гд-7 — маслянистая, бесцветная прозрач ная жидкость с сильным запахом, свойственным всем про изводным тиофосфорных и тиофосфиновых кислот. Тем пература кипения 117—118° (при 3 мм рт. ст.). Удельный вес при 20° 1,13. Фармакологически ранее не изучался. По данным Д. М. Пайкина и др. (1957), по токсичности для насекомых близок к тиофосу.
Препарат Гд-42 — сиропообразная бесцветная жид кость, хорошо растворимая в воде; фармакологически также впервые изучался в лаборатории, руководимой М. Я. Михельсоном. И. В. Семенов и Н. К- Фруентов (1958) изучили сравнительную силу тормозящего дейст вия этих препаратов на истинную холинэстеразу и дейст вие на периферические синапсы, оцениваемые по спо собности вызывать спазм бронхов. Они показали, что при метилсульфометилировании препарата Гд-7 происходит более выраженное усиление антихолинэстеразного дейст вия и способности вызывать спазм бронхов: антихолин-
120
эстеразное действие возрастает приблизительно в 650 000 раз, а способность вызывать бронхоспазм — в 200 раз.
Мы поставили перед собой задачу изучить влияние перевода серы в молекуле фосфорорганического вещества из двухвалентной в трехвалентную, несущую положитель ный заряд, на соотношение антихолинэстеразного дейст вия в головном мозгу и мышцах организма (Я. С. Смусин, 1958). Соотношение степеней торможения холинэстеразы в центральной нервной си стеме и в периферических тканях дает возможность судить о распределении изучавшихся антихолинэстеразных веществ в ор ганизме.
В опытах на белых мышах была установлена средняя смертельная до
за, |
вызывающая |
смерть |
|
в течение |
первых |
суток |
|
при |
подкожном введении |
||
Гд-7 у 50% |
мышей. Эта |
||
доза |
оказалась |
равной |
|
0,53 |
мг/кг, |
а для его ме- |
|
тилсульфометилата (Гд42) — 0,023 мг/кг веса, т. е. метилсульфометилирование усиливает токсич ность исходного вещества в 23 раза.
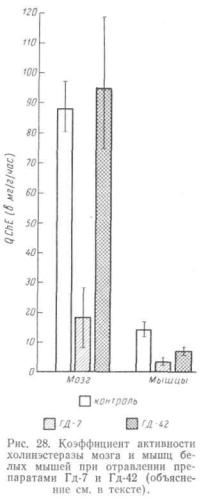
Степень торможения активности холинэстеразы сравнивалась при дейст вии равноэффектных доз обоих веществ (ДЛ50 и Vio ДЛ5о). Результаты, по лученные по определению активности холинэстеразы
истепени ее угнетения при отравлении препара тами Гд-7 и Гд-42 в дозе ДЛ5о, приведены в табл. 21
ина рис. 28.
121
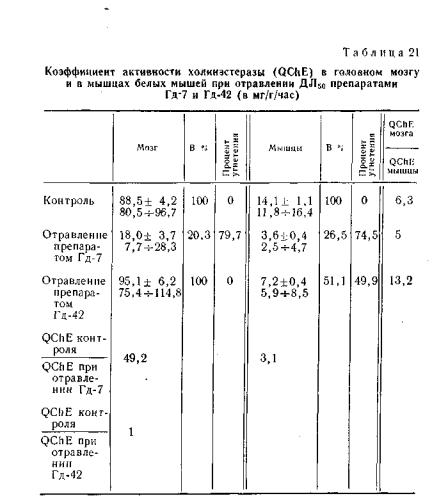
При действии препарата Гд-7 отмечается значительное угнетение активности холинэстеразы мозга и мышц. При этом холинэстераза мозга угнеталась сильнее (в 4,1 раза), чем холинэстераза мышц (в 3,1 раза). В результате тако го неравномерного угнетения холинэстераза мозга оказа лась только в 5 раз активнее холинэстеразы мышц, в то время как в контроле активность холинэстеразы мозга в 6,4 раза больше, чем в мышцах. При действии препара та Гд-42, наоборот, холинэстераза мозга не угнеталась, а холинэстераза мышц угнеталась в 3 раза. У животных,
122
отравленных препаратом Гд-42, холинэстеразная актив ность мозга в 13,2 раза превышает активность мышц.
Отсюда видно, что при отравлении белых мышей пре паратом Гд-7 активность холинзстеразы головного мозга и мышечной ткани угнетена приблизительно одинаково (соответственно на 79,7 и 74,5%). При отравлении метилатом препарата Гд-7 (препарат Гд-42) активность холин зстеразы головного мозга совсем не угнеталась, а наблю далось лишь снижение активности холинзстеразы мышеч ной ткани (на 48,9%). Тоже подтвердилось и при гистохимическом исследовании. Таким образом, на приме ре новой пары соединений подтвердилась та же закономер ность, которую мы отмечали при изучении изомеркаптофоса и его метилсульфометилата. Сопоставление степени торможения веществами холинзстеразы в мозгу и в мыш цах дает возможность судить об их распределении в орга низме. Тот факт, что препарат Гд-7 в одинаковой степени угнетает холинэстеразу мозга и холинэстеразу мышц, свидетельствует о равномерном распределении его в орга низме. Метилирование препарата Гд-7 (появление поло жительного заряда на сере) сопровождается некоторым снижением активности холинзстеразы только мышечной ткани. Холинэстераза мозга полностью сохранила свою активность. Отсюда следует, что полная ионизация пре пятствует проникновению вещества через гемато-энцефа- лический барьер из крови в мозг и несколько снижает его действие на холинэстеразу периферических тканей, в частности мышечной. Более того, препарат Гд-42 ока зывается во много раз более токсичнее, чем препарат Гд-7 (ДЛ50 в 23 раза меньше ДЛ5о препарата Гд-7).
Менее четкие результаты получаются при действии препаратов в дозах '/io ДЛбоЭто, вероятно, связано с тем, что при таких дозах торможение было вообще сла бо выражено, что затрудняет точное количественное со поставление.
Наши данные по изучению степени угнетения активно сти холинзстеразы головного мозга и мышечной ткани белых мышей были подтверждены опытами, проведенны ми Л. Г. Магазаником (1959) по определению степени угнетения холинзстеразы в различных отделах мозга и в периферических тканях кошек при введении им мини мальных бронхоспастических доз препаратов Гд-7 и Гд-42. Оказалось, что, препарат Гд-7 почти нацело тормозит ак-
1.23
тивность холинэстеразы мозга, мышцы и крови. Препа рат Гд-42 вызвал резкое угнетение холинэстеразы в пе риферических тканях (мышца, кровь), но в то же время почти не изменилась активность холинэстеразы различ ных отделов мозга. Учитывая высокую активность препа рата Гд-42 в опытах in vitro, Л. Г. Магазаник полностью относит полученные им данные за счет особенностей рас пределения препарата в организме.
Аналогичные факты были получены Koelle, Steiner (1956) при изучении другой пары фосфорорганических соединений.
Э.В. Зеймаль и М. Я- Михельсон (1961), работая
спрепаратом Гд-42, показали, что при введении кошке внутривенно одной смертельной дозы препарата холин-
эстераза мозга оказывается совсем не угнетенной. Но если ввести стократную смертельную дозу, то отмечается зна чительное угнетение.
В разных отделах мозга угнетение весьма различно: например, в коре на 95%, а в хвостатом ядре всего на 25%. Из этого факта нельзя делать вывод, что гематоэнцефалический барьер для Гд-42 лучше выражен в обла сти хвостатого ядра и слабее в области коры головного мозга, так как степень угнетения активности холинэсте разы при данной концентрации ФОС зависит от исходной активности холинэстеразы: степень торможения холин эстеразы тем больше, чем меньше исходная активность холинэстеразы. Авторы показали, что фактические кон центрации препарата Гд-42 в разных отделах мозга прак тически остаются одинаковыми. Отсюда следует, что существенной разницы в проницаемости гемато-энцефа- лического барьера различных отделов мозга для сульфониевого ФОС Гд-42 не отмечается.
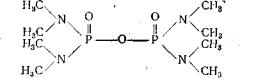
Отравление октаметилом. Одним из производных пирофосфорной кислоты является октаметил (октаметилтетраамидпирофосфат).
Молекулярный вес 286,24
Октаметил представляет собой жидкость без цвета
124
и почти без запаха. Водные растворы октаметила устой чивы к гидролизу. Удельный вес октаметила 1,399. Тем пература кипения 135—136° (при 1,5 мм рт. ст.). Октаметил смешивается во всех отношениях с водой и с боль шинством органических растворителей. За границей октаметил известен под названиями: ОМПА, пестокс-3, шрадан.
В настоящее время промышленность выпускает тех нический препарат, представляющий густую масляни стую жидкость темно-коричневого цвета со слабым запа хом. Применяется в виде водных растворов (0,1—0,25%).
Du Bois, Doull и Coon (1950) установили, что октаме тил не обладает заметным антихолинэстеразным дейст вием, но в организме под влиянием фермента, содержа щегося в печени, превращается в сильный ингибитор холинэстеразы. Другой отличительной чертой ОМПА яв ляется его неспособность проникать из крови в мозг (Frawley, Hagan, Fitzhugh, 1952). Поэтому его холинергическое действие ограничено периферическими тканями. Симптомов перевозбуждения холинергических структур центральной нервной системы при отравлениях октаметилом не бывает. Du Bois, Doill и Coon (1950) установили также, что активация октаметила происходит в процессе его окисления. Активация октаметила воспроизводится не только тканью печени, но и перманганатом калия (в молекуле октаметила аминогруппы переходят в амидооксидные) и хлором. Образующийся в результате окис ления N-оксид обладает высокой антихолинэстеразной активностью.
Подобной активации печенью подвергаются также тиофос, метафос и меркаптофос (систокс). Триортокрезилфосфат также активируется в организме, это проис ходит в результате его изомеризации.
Октаметил в настоящее время находит все более широкое применение в СССР в качестве инсектицида (Н. Н. Мельников, 1953; Т. Е. Изотова и др., 1957; Е. А. Покровский и П. И. Митрофанов, 1955; П. И. Мит рофанов, 1956; Ю. С. Каган, 1963). Он токсичен для тепло кровных животных и человека. Действие на теплокров ных животных связывают с антихолинэстеразными свой ствами продукта превращения октаметила в организме (N-оксида). Опасность отравления октаметилом людей и сельскохозяйственных животных при использовании
125
его в качестве инсектицида требует изучения токсиколо гических свойств препарата, выяснения гигиенических условий труда, разработки соответствующих гигиениче ских норм (Т. Е. Изотова и др., 1955; В. С. Бурый, 1957; М. Е. Мачабели и др., 1957, и др.).
Октаметил способен проникать в организм через ды хательные пути, пищеварительный тракт, кожу и слизи стые. Картина интоксикации характеризуется резким возбуждением холинергических структур (саливация, по вышение возбудимости желудочно-кишечного тракта, су дороги, фибриллярные подергивания мышц, расстройст ва координации движения) (В. С. Бурый, 1957).
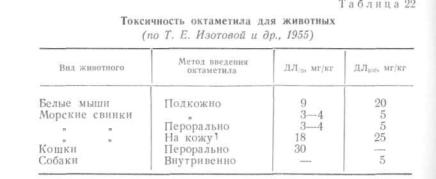
Приводим данные по токсичности октаметила для раз личных животных (табл. 22).
В. С. Бурый (1957) указывает, что абсолютной смер тельной дозой химически чистого октаметила для крыс (самцов) при пероральном введении является доза 8— 10 мг/кг. В. Д. Мдинарадзе (1957) приводит данные по токсичности октаметила для белых крыс и мышей: при пероральном введении ДЛ50 для белых крыс составляет 8—10 мг/кг, для белых мышей— 19 мг/кг; ДЛюо для бе лых крыс — 10 мг/кг, для белых мышей — 24 мг/кг.
И. Д. Неклесова и М. А. Кудрина (1956) при изучении токсикологических свойств октаметила в опытах на раз личных животных обратили внимание на замедленное и длительное проявление отравления. Авторы, изучая влияние октаметила на кровяное давление и дыхание, наблюдали, что при введении октаметила в дозе 30— 100 мг/кг внутривенно кошкам и собакам наступала
126
смерть животных от остановки дыхания (сердце «пере живало» дыхание па 3 минуты).
Медицинская литература об октаметиле к настояще му времени весьма обширна.
В опытах И. В. Семенова (1958) октаметил в дозе 30 мг/кг приводил к развитию спазма бронхов на 50% через 1'/2 часа после внутривенного введения препарата. И. В. Семенову в опытах по методу Концетт—Ресслера— Турпаева удалось проследить при длительном наблюде нии постепенное нарастание бронхоспастического дейст вия октаметила. Автор объясняет это прогрессирующим угнетением холинэстеразы в организме подопытного жи вотного. В этих же опытах in vitro октаметил совсем не угнетал холинэстеразу.
В опытах на животных В. Д. Мдинарадзе (1959) наб людал миоз, слюнотечение, брадикардию, повышение возбудимости, фибриллярное подергивание мышц, тре мор, расстройства координации движений, судороги, из менения в содержании сахара в крови, нарушения условнорефлекторной деятельности, лейкоцитоз. На секции животных, погибших от отравления октаметилом, отме чали резкое полнокровие внутренних органов, расшире ние крупных и мелких сосудов, кровоизлияния, в печени и почках — дистрофические изменения, в головном моз гу — выраженный клеточный отек.
Ю. С. Каган и В. С. Бурый (1956) у людей с острым отравлением октаметилом после скрытого периода наб людали брадикардию, иногда миоз, потоотделение, сон ливость, стойкий красный дермографизм, местно — дер матиты, конъюнктивиты. При хронических отравлениях отмечаются головная боль, вялость, потеря аппетита, тошнота, похудание, брадикардия, артериальная гипото ния, удлинение времени красного дермографизма (И. Я. Сосновик, 1959).
При изучении действия октаметила на активность хо линэстеразы мы были вынуждены использовать техниче ский препарат (из-за отсутствия чистого препарата). Мы отдавали себе отчет в том, что имеющиеся примеси в тех ническом препарате могут до некоторой степени извратить специфическое действие октаметила. Однако мы учитыва ли, что встречающиеся отравления человека и сельскохо зяйственных животных вызываются преимущественно техническими препаратами октаметила, которые выраба-
127
тываются нашей промышленностью и нашли широкое применение в сельском хозяйстве в качестве инсекти цидов.
Исследования мы проводили на кошках. Октаметил вводили внутримышечно в дозе 60 мг/кг (Я. С. Смусин, 1963).
Первые клинические явления отравления обычно от мечались через l'/г часа после введения препарата в виде неустойчивости походки, резкой саливации, мочеот деления, дефекации, бокового положения. Затем присое динялись фибриллярные подергивания, выпячивание глаз ных яблок, слезотечение, паралич задних конечностей. Гибель животных, как правило, наступала через 12— 24 часа после введения препарата.
В качестве контроля служили кошки, обездвиженные дитилином (1 мг/кг) и забитые кровопусканием.
Методом Хестрина исследовали активность холинэстеразы крови, сыворотки, миокарда, мышечной ткани, лег ких, печени, коры головного мозга, хвостатого ядра, среднего мозга, мозжечка, продолговатого и спинного мозга. Полученные результаты приведены в табл. 23 и на рис. 29.
Наши исследования показали, что при отравлении кошек октаметилом происходит значительное угнетение активности холинэстеразы крови, сыворотки и перифери ческих органов и тканей — на 62,7—79,3% от исходного. Угнетение активности холинэстеразы тканей центральной нервной системы выражено значительно слабее: от 11,5% (хвостатое ядро) до 53,7% (мозжечок), но обычно — в пределах 30—50% от исходного. Таким образом, окта метил, введенный в организм животного, лишь через оп ределенный Скрытый период проявляет токсическое дей ствие. Октаметил является сильным ингибитором хо линэстеразы, оказывая антихолинэстеразное действие преимущественно на периферические ткани.
В силу своих физико-химических свойств октаметил плохо проникает в клетки мозга и не вызывает централь ных эффектов, столь характерных для большинства ФОС (С. Н. Голиков и В. И. Розенгарт, 1960, 1964), в частно сти судорог и других симптомов действия яда на централь ную нервную систему (Du Bois, Doull и Coon, 1950).
Наблюдаемое в наших опытах также угнетение холин эстеразы тканей центральной нервной системы (в сред-
128
