
3 курс / Патологическая физиология / Норма_и_патология_в_человеческом_организме_Парнес_Е_Я_
.pdfхуже размножается в эритроцитах, содержащих измененный гемоглобин: не только у гомозигот, но и у гетерозигот. И хотя гомозиготы умирают от анемии, но зато гетерозиготы получают преимущество перед нормальными людьми, поскольку легче переносят малярию. Наверное, вы слышали о РЕЗУС-КОНФЛИКТЕ, приводящем к ЖЕЛТУХЕ НОВОРОЖДЕННЫХ. Развивается эта желтуха, когда у резус-отрицательной мамы и резус-положительного папы рождается резус-положительный ребенок, и при родах в кровь матери попадает чужеродный белок — резус-фактор.
В организме матери начинают вырабатываться антитела против резус-фактора. Однако ребенок родился, резус-фактор больше не поступает, реагировать не на кого, инцидент вроде бы исчерпан.
Но вот женщина опять захотела родить ребенка, и он опять резус-положительный. Иммунная же система матери продолжает в больших количествах вырабатывать антитела к резусфактору, проникающие в кровь плода через плаценту. Они вызывают массивный гемолиз у плода, и билирубин окрашивает ребенка в желтый цвет*. Иногда резус-конфликт может стать причиной бездетности в семьях.
Резус-конфликт развивается не всегда. Некоторые мои знакомые резус-отрицательные мамы имеют четыре-пять резус-положительных детей, и ни у одного из них не было гемолитической желтухи. Вероятно, секрет в том, что при нормальных родах кровь ребенка практически не попадает в кровь матери, а попавшие эритроциты ребенка уничтожаются средствами защиты без «включения» специфического распознавания. А вот после абортов резус-конфликты часты, т. к. при выскабливаниии смешиваются кровь плода и кровь матери.
У матери и плода раздельные круги кровообращения. В плаценте питательные вещества и кислород проникают из сосудов матери в сосуды ребенка. Обмен кислорода возможно благодаря тому, что эритроциты плода содержат ФЕТАЛЬ-
* Если ребенку повезет, то желтуха через несколько дней или недель исчезнет. Но часто резус-конфликт бывает причиной гибели плода или новорожденного.
20
НЫЙ ГЕМОГЛОБИН, который имеет большее сродство к кислороду и «отнимает» его у нормального гемоглобина матери. (Правда, феталъный гемоглобин хуже отдает кислород по сравнению с обычным.)
После рождения ребенка эритроциты, содержащие фетальный гемоглобин, разрушаются. Возникает ФИЗИОЛОГИЧЕСКАЯ ЖЕЛТУХА НОВОРОЖДЕННЫХ — вариант гемолитической анемии, наблюдаемый в той или иной степени v всех новорожденных. Но, к счастью, у ребенка быстро появляются эритроциты с нормальным (взрослым) гемоглобином.
Рассмотрим еще одну ситуацию, которая заканчивается гемолитической желтухой. У некоторых народов Средиземноморья распространен наследственный дефицит активности ГЛЮКОЗО-6-ФОСФАТДЕГИДРОГЕНАЗЫ (Г-6ФД). Этот фермент предотвращает окисление гемоглобина, которое могут вызывать некоторые лекарства: сульфаниламиды (этазол, стрептоцид), нитрофураны (фурагин, фуразолидон), анальгетики (аспирин, фенацетин) и др.
У здорового человека дефицит активности Г-6-ФД может никак не проявляться. Но представим себе, что человек с таким наследственным дефектом простудился. Порывшись в аптечке, он, скорее всего, примет «от температуры» аспирин, а «от горла» — стрептоцид, этазол или бисептол. И вдруг через сутки-двое у него вновь возрастает температура, появляется сильная слабость, головная боль, боли в правом подреберье (из-за того, что увеличенная печень растягивает свою капсулу), моча темнеет, а кожа желтеет.
Сходные симптомы характерны для острого вирусного гепатита. Поэтому больного могут отправить в инфекционную больницу. Если такие состояния повторяются, нередок диагноз хронического активного гепатита. Но опытные врачи смотрят анализ крови — и при низком содержании гемоглобина и эритроцитов понимают: все дело в гемолитической анемии при дефиците активности Г-6-ФД, а причина криза* — прием лекарств и/или воздействие вируса. При гемолитической анемии (независимо от ее вида) гибнет множество эритроцитов в сосудистом русле, возрас-
* КРИЗ — резкое изменение Физиологического состояния.
21
тает концентрация билирубина и развивается желтуха. Из-за нехватки эритроцитов ухудшается обеспечение кислородом тканей, в том числе — костного мозга. А это служит сигналом к усиленному делению клеток красного кроветворного ростка (см. § 5).
В результате в костном мозге возрастает число эрит-робластов, а в крови появляется много ретикулоцитов. Содержание же гемоглобина в эритроцитах нормальное: ведь никаких препятствий для деления клеток и синтеза гемоглобина нет.
АПЛАСТИЧЕСКИЕ АНЕМИИ
Наконец, рассмотрим АПЛАСТИЧЕСКИЕ* АНЕМИИ, развивающиеся при угнетении кроветворения. Их причины очень разнообразны:
—радиация;
—токсичные вещества (например, бензол);
—лекарственные препараты: очень популярный антибиотик левомицетин; противовоспалительный и обезболивающий препарат бутадион; цитостатики** и др.;
—некоторые тяжелые инфекционные и аутоиммунные болезни.
Особенность всех этих анемий — падение скорости деления предшественников всех клеток крови. В результате снижается количество лейкоцитов и тромбоцитов, а молодые формы эритроцитов в крови почти полностью отсутствуют.
Симптомы болезни — головокружение, обмороки, слабость, СЕРДЦЕБИЕНИЕ*** и т. д. — связаны с низким
*Этот термин обозначает нарушение процессов синтеза.
**ЦИТОСТАТИКИ — лекарства, угнетающие деление клеток. Они используются для подавления роста и деления агрессивных клеток иммунной системы или злокачественных опухолей.
***СЕРДЦЕБИЕНИЕ — ощущение человеком ударов сердца, которое возникает или из-за усиления его работы (например, после бега), или при резком учащении ритма сокращений.
22

содержанием кислорода в крови и тканях (ГИПОКСИЧЕ-СКИ-ЦИРКУЛЯТОРНЫЙ СИНДРОМ*). Больные обычно очень бледные, на коже — синяки или мелкоточечная сыпь (причину этого явления мы разберем, когда будем говорить о тромбоцитах). Низкий уровень лейкоцитов приводит к частым пневмониям, некротической ангине**, долго не заживающим язвам во рту, а также к сепсису.
§ 3. ТРОМБОЦИТЫ
ФУНКЦИИ ТРОМБОЦИТОВ
Тромбоциты циркулируют и выполняют свои функции только в крови.
У большинства позвоночных тромбоцит имеет ядро и, следовательно, является клеткой. Тромбоцит человека и других
Рис. 2. Мегакариоцит среди других клеток в костном мозге: а — эндотелиальная клетка; б — развивающиеся клетки крови; в — мегакариоцит; г — отросток мегакариоцита, отпоч-ковывающий тромбоциты; д — плазма крови; е — эритроцит
млекопитающих — это отшнурованный кусочек цитоплазмы МЕГАКАРИОЦИТА, огромной клетки костного мозга (рис. 2).
*СИНДРОМ — СОВОКУПНОСТЬ симптомов, вызванных одной причиной.
**НЕКРОТИЧЕСКАЯ АНГИНА — воспаление нёбных миндалин (в горле), сопровождающееся гибелью тканей.
23

Рис. 3. Микрофотоснимки тромбоцитов, полученные с помощью сканирующего электронного микроскопа: а — неактивированные клетки; б — активированные клетки При активации у тромбоцита вытягиваются отростки-псевдоподии (рис. 3), благодаря которым он
может прилипать к поверхности сосуда (АДГЕЗИЯ) или к другому тромбоциту (АГРЕГАЦИЯ). Органоидов в тромбоците мало; всё, что нужно для его функционирования, забирается из цитоплазмы мегака-риоцита.
Таким образом, тромбоцит — не клетка, а мешочек из мембраны, заполненный разнообразным и очень ценным содержимым. Химический состав этого содержимого определяет функции тромбоцита. Перечислим их.
1. ТРОФИЧЕСКАЯ функция. Благодаря ей обеспечивается поддержание нормальной структуры и функции сосудов, их устойчивости к повреждениям, а также ограничение их проницаемости. Клетки, выстилающие внутреннюю поверхность сосудов (ЭНДОТЕЛИЙ), часть питательных веществ получают из тромбоцитов, сливающихся с ними.
При пониженной концентрации тромбоцитов ухудшается подкормка эндотелиальных клеток, что ведет к их дистрофии*:
* ДИСТРОФИЯ — сложный патологический процесс, ПРИ КОТОРОМ нарушение обмена веществ вызывает структурные изменения сначала клеток, а затем и органа.
24
—между клетками эндотелия образуются щели;
—менее прочной становится БАЗАЛЬНАЯ МЕМБРАНА, на которой эти клетки расположены. Стенка капилляров становится проницаемой для эритроцитов, и они выходят за пределы сосудистого русла (диапедез).
2. Участие в регуляции тонуса сосудов. Спазм обеспечивают регуляторы тонуса сосудов (адреналин, серотонин, тром-боксан, ионы кальция), выделяемые тромбоцитами. Эти вещества крайне важны для поддержания длительного спазма поврежденных сосудов.
3. Закупоривание поврежденных сосудов ТРОМБОЦИ-ТАРНЫМ ТРОМБОМ благодаря способности тромбоцитов к адгезии и агрегации.
4. Участие в активации свертывающей системы крови. О свертывании крови следует рассказать подробнее.
СВЕРТЫВАНИЕ КРОВИ
Кровь жидкая, а значит, при нарушении целостности кровеносного сосуда она могла бы вся вытечь. Но зубы у вас выпадали или их вырывали, пальцы резали, а больших кровотечений не было. Спасает от массивной кровопотери свертывающая система крови. Благодаря ей формируется достаточно плотный кровяной сгусток — тромб, перекрывающий просвет поврежденного сосуда.
Перед свертывающей системой стоит сложная задача:
—сформировать тромб только в месте повреждения сосуда;
—не допускать образования тромба в неповрежденных сосудах.
Остановка кровотечения — ГЕМОСТАЗ — происходит сначала (за несколько минут) в результате образования тром-боцитарного тромба (из тромбоцитов), а затем (примерно за час) выпадения нитей фибрина и образования ими -конгломерата со сгустками тромбоцитов. Тромбоцитарный тромб осуществляет ПЕРВИЧНЫЙ ГЕМОСТАЗ, который предохраняет от кровотечений из мелких сосудов. Но этот тромб непрочный. При ВТОРИЧНОМ ГЕМОСТАЗЕ тромб из тромбоцитов и фибрина
25
более прочен и предохраняет от повторных кровотечений даже из крупных сосудов на протяжении нескольких дней.
Процесс свертывания крови очень сложен (схема 1). В нем участвует более десятка плазменных факторов. Окончательным результатом активации факторов свертывания является перевод неактивного ПРОТРОМБИНА (фактора II) в активный фермент ТРОМБИН (фактор На). Тромбин превращает растворимый белок фибриноген (фактор I) в фибрин-мономер, который затем «сшивается» в цепочки фибрина-полимера. Эти цепочки выпадают в виде нитей, в которых запутываются форменные элементы крови. В результате образуется прочная пробка — тромб (см. § 1), перекрывающая просвет сосуда.
Существуют внешний и внутренний пути свертывания крови.
Для запуска внешнего пути необходимо попадание в кровь внешнего фактора — ТКАНЕВОГО ТРОМБОПЛАСТИНА (одного из белков тканевой жидкости), например, при ранении сосуда. Внутренний путь свертывания крови начинается с появления отрицательного заряда на поверхности кровеносного сосуда, лишенного эндотелия, или на чужеродной поверхности (например, стеклянной стенке пробирки). Таким образом, чтобы активировался внутренний путь свертывания, необходима поверхность контакта (рис. 4). При повреждении внутренней оболочки сосуда процесс свертывания начинается с адгезии тромбоцитов к СУБЭНДОТЕЛИАЛЬНОМУ МАТРИКСУ: белку коллагену и другим элементам соединительной ткани, расположенным под эндотелием. Адгезия осуществляется благодаря ФАКТОРУ ВИЛЛЕБРАНДА — белку, который прикрепляет тромбоциты к матриксу. Это прикрепление вызывает
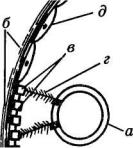
Рис. 4. Схема межмолекулярных взаимодействий в ходе прикрепления тромбоцита к стенке поврежденного сосуда: а — тромбоцит; б — субэндотелиальный матрикс; в — фактор Виллебранда; г — рецептор тромбоцита; д — эндотелий
26

Схема 1. Активация факторов свертывающей системы крови. Римскими цифрами обозначены плазменные факторы свертывания; А — поверхность контакта (например, субэндотелиальный матрикс); Б — мембрана активированного тромбоцита
27
их активацию, агрегацию, а следовательно — запуск образования тромбоцитарного тромба (схема
2).
Всвертывании крови участвуют также фосфолипиды мембраны активированных тромбоцитов, которые в тысячи раз ускоряют процессы активации плазменных факторов.
Как видно из схемы 1, начиная с определенного этапа (после активации фактора X) оба пути свертывания объединяются.
При снижении числа тромбоцитов в крови или нарушении их функций появляются одинаковые симптомы, не зависящие от исходных причин;
— кожные кровоизлияния;
— повышенная ломкость сосудов, когда после небольшого щипка образуется синяк;
— кровотечения: носовые, желудочно-кишечные и другие.
А при некоторых заболеваниях способность тромбоцитов склеиваться возрастает, что приводит к внутрисосуди-стым тромбам. Крайне опасно тромбообразование в артериях сердца и головного мозга, поскольку это может закончиться инфарктом миокарда* или инсультом**. Может быть, вы слышали, что при ишемической болезни сердца*** назначают малые дозы аспирина. Не странно ли — зачем лекарство «от температуры» больному с нарушенной циркуляцией крови по сосудам сердца?
Впрофилактике повторных инфарктов и инсультов главное — избежать закупорки сосудов, несмотря на возросшую склонность к тромбообразованию. Формирование тромба
*ИНФАРКТ МИОКАРДА — гибель участка сердечной мышцы в результате недостаточного поступления к нему кислорода (ИШЕМИИ).
**ИНСУЛЬТ — гибель участка головного мозга. Ишемический инсульт развивается при нарушении поступления крови к участку мозга. Чаше всего такая ситуация возникает вследствие сужения просвета мозговой артерии АТБРОСКЛЕРОТИЧЕСКОЙ БЛЯШКОЙ (см. пособие «Кровообращение»).
***ИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА (ИБС) возникает из-за несоответствия потребности сердечной мышцы (МИОКАРДА) в кислороде снизившемуся его поступлению. Наиболее распространенными формами ИБС являются стенокардия и инфаркт миокарда.
28

29
