
3 курс / Патологическая физиология / Воспаление
.pdf
Medicine Books (https://vk.com/medicinebook)
Рис 3-8: Гнойное воспаление. А, На фотографии кожный абсцесс (фурункул) вызванный Staphylococcusaureus. Абсцесс содержит гнойный очаг в дерме. Видны множественные дренирующие отверстия, содержащие гной. В, Фибринозное воспаление. Поверхность сердца «волосатая», с фибринозным экссудатом. С, Псевдомембрнозное воспаление. Отмечается некроз и желтый экссудат, покрывающая слизистую оболочку толстого кишечника, образуемый в результате воздействия токсина Clostridium difficilе.
9.3.Продукция резолвинов
Синтезируются из Ψ3-жирных кислот;
Препятствуют привлечению воспалительных клеток в очаг ОВ.
9.4.Повышение уровня апоптоза среди нейтрофилов.
10.Последствия острого воспаления.
10.1.Полное разрешение ОВ:
Происходит в том случае, когда поврежденные клетки способны вновь входить в клеточный цикл (н. лабильные и стабильные клетки-предшественники);
Примеры – первая степень ожогового повреждения кожи, укус пчелы.
10.2.Разрушение ткани и образование рубца:
Разрушение ткани и образование рубца происходит в случае сильного воздействия повреждающего фактора или повреждения клеток-предшественников в ткани;
Примеры – третья степень ожогового повреждения, острый инфаркт миокарда.
10.3.Формирование абсцесса (локализованное скопление нейтрофилов и участка колликвационного некроза)
Пример – абсцесс легкого в результате аспирации пищи.
10.4.Переход острого воспаления в хроническую форму.
II.Хроническое воспаление
1.Определение хронического воспаления (ХВ)
1.1.Пролонгированное воспаление (от нескольких недель до нескольких дней), часто приводящее к персистенции повреждающего агента.
2.Причины ХВ:
2.1.Инфекция – наиболее частая причина ХВ:
Например: туберкулез, лепра, гепатит С;
2.2.Аутоимунные заболевания:
Например: ревматоидный артрит, системная красная волчанка;
2.3.Стерильная воспалительная реакция:
Например: воспалительная реакция на пыль, мочевую кислоту, силикон в имплантатах и др.
3.Морфология ХВ:
3.1.Основные клеточные типы при ХВ:
Моноциты и макрофаги (ключевые клетки); лимфоциты, плазматические клетки и эозинофилы (рис. 3-9);

Medicine Books (https://vk.com/medicinebook)
Рис 3-9: Хроническое воспаление. В ткани видны |
Рис 3-10: Грануляционная ткань. Отмечаются как |
лимфоциты и небольшое количество плазматических |
клетки острого воспаления (нейтрофилы), так и |
клеток (клетки с эксцентричным ядром и |
хронического (лимфоциты, плазматические клетки, |
перинуклеарным просветлением, отмечены белой |
макрофаги), а так же большое количество |
стрелкой). |
небольших, расширенных сосудов. Одиночные, |
|
расплющенные фибробласты (отмечены стрелкой) |
|
синтезируют коллаген III типа. |
Трансформирующий фактор роста-β (ТФР-β) является хемоаттрактантом для макрофагов, лимфоцитов и фибробластов;
3.2.Разрушение паренхимы:
Происходит разрушение паренхимы со снижением ее функциональных возможностей, развивается склероз;
3.3.Формирование грануляционной ткани:
Определение – богато васкуляризированная ткань, состоящая из кровеносных сосудов и фибробластов (рис. 3-10):
o Кровеносные сосуды образуются из пресуществующих, а так же denovo из предшественников эндотелиальных клеток, рекрутируемых из костного мозга (т.н., ангиогенез). Важнейшие ростовые факторы ангиогенеза – сосудистый эндотелиальный фактор роста, фактор роста фибробластов, эпидермальный фактор роста, фактор роста – производный тромбоцитов, ТФР-β;
o Васкуляризация – важнейший этап нормального заживления ран;
o Грануляционная ткань является предшественницей рубцовой ткани.
Фибронектин необходим для образования грануляционной ткани;
oФибронектин – гликопротеин клеточной адгезии, располагающийся во внеклеточном матриксе (ВКМ). Он связывается с коллагеном, фибрином и рецепторами на клеточной поверхности (например, с интегринами);
oЯвляется хемотаксическим фактором для привлечения фибробластов (синтезируют коллаген) и эндотелиальных клеток (для формирования новых кровеносных сосудов).
3.4.Сравнение острого и хронического типа воспаления (см. таблицу 3-3).
3.5.Грануломатозное воспаление:
Определение – особый вид хронического воспаления;
Причины:
oИнфекции
Например – туберкулез или системные грибковые инфекции (н. гистоплазмоз);
Подобные заболевания часто ассоциированы с казеозным некрозом (т.н. мягкие грануломы, см. Главу 2). Казеозсвязан с выделением липидов из мембран погибших микроорганизмов.
oНеинфекционные причины
Например – саркоидоз или болезнь Крона;
Medicine Books (https://vk.com/medicinebook)
Саркоидоз и болезнь Крона имеют безказеозныегрануломы (т.н. твердые гранулемы).
Морфология гранулемы:
o Определение – бледный, белесоватый узел с/без центрального некроза; o Обычно хорошо отграничена от окружающей ткани;
oКлетки, представленные в инфекционной гранулеме (н. при туберкулезе):
Эпителиоидные клетки (активированные макрофаги) и мононуклеарные клетки, являющиеся CD4 Т-клетками, а именно Т-хелперами первого типа (клетки памяти);
Многоядерные гигантские клетки, образующиеся при слиянии эпителиоидных клеток. Чаще всего, подобные клетки
располагаются на периферии гранулемы.
oФНО-α играет важную роль в формировании и поддержании гранулемы при туберкулезе или системном кандидозе;
ФНО-α и интерферон-γ рекрутируют клетки, формирующие гранулему;
Ингибиторы ФНО-α приводят к разрушению гранулемы, что
может привести к диссеминации инфекции.
oСпецифические реакции, происходящие при образовании в гранулеме, подробнее описаны в Главе 4 в разделе о реакции гиперчувствительности IV типа.
Таблица 3-3. Сравнение острого и хронического воспаления
|
Острое воспаление |
Хроническое воспаление |
Причины |
Микробные патогены, травма, ожоги |
Персистирующее ОВ, инородные тела (н. |
|
|
силикоз), аутоиммунные заболевания, |
|
|
определенные типы инфекций (н. |
|
|
туберкулез, лепра) |
Первичные |
Нейтрофилы |
Моноциты/макрофаги (ключевые клетки), |
клетки |
|
В и Т-лимфоциты, плазматические клетки, |
|
|
фибробласты |
Первичные |
Гистамин (ключевой медиатор), |
Цитокины (н. ИЛ-1), ростовые факторы |
медиаторы |
простагландины, лейкотриены |
|
Некроз |
Присутствует |
Редко |
Образование |
Отсутствует |
Присутствует |
рубца |
|
|
Начало |
Быстрое |
Отсроченное |
Длительность |
Несколько дней |
Недели, месяцы, года |
Исход |
Полное разрешение, переход в |
Формирование рубцовой ткани, |
|
хроническое воспаление, формирование |
нарушение функции, амилоидоз (см. |
|
абсцесса |
Главу 4) |
Основной |
IgM |
IgG |
иммуноглобулин |
|
|
Электрофорез |
Умеренная гипоальбуминемия |
Поликлональнаягаммапатия, значительная |
|
|
степень гипоальбуминемии |
Изменения |
Нейтрофильный лейкоцитоз |
Моноцитоз |
лейкоцитов в |
|
|
периферической |
|
|
крови |
|
|
III.Репарация тканей
1.Факторы, вовлеченные в тканевую репарацию:
Регенерация паренхиматозных клеток;
Восстановление путем разрастания соединительной ткани (фиброз).
Medicine Books (https://vk.com/medicinebook)
2.Регенерация паренхиматозных клеток:
Клеточное восстановление зависит от способности клеток к репликации (см. Главу
2):
o Лабильные клетки (н. стволовые клетки в эпидермисе) и стабильные клетки (н. фибробласты) могут реплицироваться;
o Перманентные клетки не могут реплицироваться. Например, сердечная и поперечно-полосатая мышечные ткани заменяются соединительной тканью;
Клеточная регенерация зависит от факторов, стимулирующих клеточное деление и миграцию. Стимулирующие факторы включают повреждения и потерю ткани, а так же продукцию факторов роста (см. таблицу 3-4).
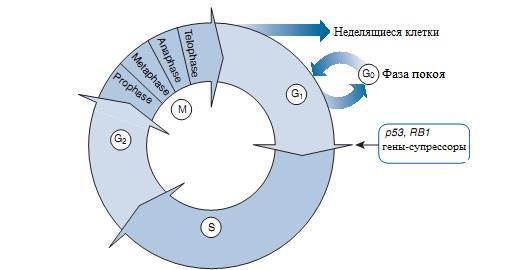
Клеточный цикл (рис. 3-11)
oФазы:
G0-фаза. Фаза отдыха стабильных паренхиматозных клеток;
G1-фаза. В клетках происходит синтез РНК, белков, органелл и циклина Д. Особенности данной фазы очень сильно варьируют у различных клеток.
S (синтетическая) фаза. Происходит синтез ДНК, РНК и белков.
G2-фаза. В клетках происходит синтез тубулина, необходимого для образования веретена деления.
М (митотическая) фаза. Образование двух дочерних клеток в результате митоза.
oРегуляция G1-точки контроля (переход G1 вS):
Наиболее критичная фаза в клеточном цикле. Если в данную фазу происходит мутация, то в S фазу она будет копирована, что приведет к увеличению риска развития рака.
Контролирующие белки включают в себя циклин-зависимую киназу 4 (Цзк4; Cdk4, cyclin-dependentkinase 4) и циклин Д.
Факторы роста активируют ядерную транскрипцию протоонкогенов (см. Главу 9), что приводит к продукции циклина Д и Цкз4. Циклин Д связывается с Цкз4, формируя комплекс, обеспечивающий переход клетки в Sфазу.
Роль РБ1 (RB1, retiboblastoma)супрессорного гена в клеточном цикле. РБ1-белок останавливает клетку в G1-фазе. Цзк4фосфорилирует РБ1-белок, обеспечивая переход клетки в синтетическую фазу. Однако, если РБ1-белок не фосфорилирован, то клетка вынуждена оставаться в G1-фазе.
Роль p53 супрессорного гена в клеточном цикле. Белок р53 вызывает остановку клеточного цикла в G1фазу за счет ингибирования Цзк4. Ее ингибирование приводит к отсутствию фосфорилирования РБ1-белка, что позволяет клетке выиграть время для репарации существующих повреждений ДНК.
Если количество или характер повреждений ДНК не позволяют ее полностью восстановить, то белок р53 может способствовать двум процессам: 1) ингибировать трансляцию BCL-2 антиапоптотических генов, что приведет к развитию апоптоза, или 2) ингибировать трансляцию генов, способствующих росту (н. MYCпрото-онкогена, см. главу 9), что приведет к остановке роста.
Отсутствие продукта гена р53 позволяет клетке перейти в S фазу.
Восстановление нормального состояния:
oТребуется наличие базальной мембраны;
oТребуется наличие относительно интактного внеклеточного матрикса (н. коллагена, адгезивных белков)
Medicine Books (https://vk.com/medicinebook)
Ламинин, ключевой адгезивный белок в базальной мембране, взаимодействует с коллагеном IV типа, рецепторами на клеточных поверхностях и компонентами внеклеточного матрикса.
Таблица 3-4. Факторы вовлеченные в тканевую репарацию
Фактор |
Функции |
Факторы роста |
|
Эндотелиальный сосудистый |
Стимулирует ангиогенез (эмбриональныйангиогенез, частично в |
фактор роста (VEGF, |
сердце), репарация тканей, опухолевый ангиогенез (из |
vascularendothelialgrowthfactor) |
пресуществующих сосудов). |
|
Стимулирующие факторы: выделение ФНО из макрофагов, гипоксия |
|
через гипоксия-индуцибельный фактор (HIF, hypoxia-induciblefactor), |
|
выделяемый из клеток. |
Фактор роста фибробластов (FGF, |
Хемотаксис фибробластов; стимулирует миграцию кератиноцитов, |
fibroblast growth factor) |
ангиогенез и сокращение краев раны. |
Эпидермальный фактор роста |
Стимулирует миграцию кератиноцитов, формирование |
(EGF, epidermal growth factor) |
грануляционной ткани |
Тромбоцитарныйфакторроста |
Хемотаксис нейтрофилов, макрофагов, фибробластов, |
(PDGF, platelet-derived growth |
эндотелиальных клеток (ангиогенез), гладкомышечных клеток |
factor) |
(ангиогенез) |
Трансформирующий фактор |
Хемотаксис макрофагов, лимфоцитов, фибробастов, гладкомышечных |
роста-β (TGF- β, transforming |
клеток (ангиогенез) |
growth factor- β) |
|
Интерлейкины (ИЛ), Цитокины |
|
ИЛ-1 |
Стимулирует синтез металлопротеиназ (ферменты, содержащие |
|
металлы) |
|
Стимулируют синтез и выделение белков острой фазы клетками |
|
печени |
Факторнекрозаопухоли (TNF, |
Активирует макрофаги, стимулирует выработку белков острой фазы |
tumor necrosis factor) |
|
Рис 3-11: Клеточный цикл. Переход из фазы G1в фазу S – наиболее критичный период клеточный цикл, который контролируется генами-супрессорми – p53 и RB1. Более подробно о них написано в тексте.
3.Восстановление путем разрастания соединительной ткани (фиброз)
Восстановление фиброзом происходит в случае тяжелых или персистирующих повреждений:
o Структура кожи при ожогах третьей степени не может адекватно восстановиться в результате разрушения эпидермиса, базальной мембраны
инарушения структуры соединительной ткани.
Последовательность событий при фиброзе:
Medicine Books (https://vk.com/medicinebook)
oНеобходима нейтрофильная трансмиграция (по механизмам описанным выше) для разрушения поврежденной ткани и трансмиграция макрофагов для удаления тканевого детрита.
o Необходимо формирование грануляционной ткани, предшественницы рубцовой ткани (описано выше).
o Необходимо начало отложения коллагена III типа.
Коллаген главный фиброзный компонент соединительной ткани. Тропоколлаген, структурная единица коллагена, состоит из трех спиральных α-цепей. Тропоколлаген в процессе своего синтеза подвергается большому количеству посттрансляционных модификаций. Реакции гидрокслирования происходят в шероховатом ЭПР, где происходит превращение пролина в гидроксипролин, а лизина в гидроксилизин. Для реакций гидроксилирования требуется аскорбиновая кислота. Гидроксипролиновые остатки образуют стабилизирующие связи в тройной цепи молекулы тропоколлагена.
Гидроксилизированные остатки могут окисляться до альдегидов, что позволяет ковалентно связываться отдельным тропоколлагеновым молекулам. Лизил-оксидаза – это металлопротеиназа (содержащая медь), опосредующая образование «сшивок» между молекулами тропоколлагена. Подобные сшивки позволяют увеличить прочность коллагена, и, например, эластической ткани. Коллаген Iтипа находится в коже, костях и связках, обеспечивая там механическую прочность ткани. А коллаген IIIтипа участвует главным образом в заживлении ран, не играя существенной роли в укреплении тканей. Количество «сшивок» в коллагене и эластической ткани увеличивается с возрастом. Это приводит к снижению эластичности кожи, суставов, кровеносных сосудов и может привести к сосудистой нестабильности и разрывам при минимальных травмах (н. сенильная пурпура; см. Главу 15). Снижение количества сшивок (н. при дефиците витамина С) приводит к уменьшению механической прочности коллагена. При дефиците витамина С возникает структурная слабость коллагена, что приводит к пурпуре (т.н. кровоизлияния в кожу и суставы) и плохому заживлению ран (см. Главу 7). Синдром Элерса-Данло (СЭД) объединяет группу наследственных заболеваний, характеризующихся дефектом синтеза и структуры коллагена Iи IIIтипа. Клинически это проявляется гипермобильностью суставов, расслоение аорты (наиболее частая причина гибели больных), пролапсом митрального клапана, кровоизлияниями в кожу (экхимозы), кровотечениями в кишечнике и плохим заживлением ран (рис. 3-12).
oПлотная рубцовая ткань, образуемая из грануляционной ткани, содержит большое количество коллагена IIIтипа, который должен быть
ремоделирован. Подобное ремоделирование приводит к увеличению плотности и механической стойкости рубцовой ткани.
oВ процессе ремоделирования важную роль играют металлопротеиназы (коллагеназы, содержащие цинк), замещающие коллаген IIIтипа на Iтипа коллагена, что усиливает плотность ткани на 70-80% в течении 3 месяцев. Как правило, по истечению этого срока рубец в основном состоит из безклеточной соединительной ткани, в которой отсутствуют воспалительные клетки, придатки кожи, но наблюдается интактный эпителий.

Medicine Books (https://vk.com/medicinebook)
 БЛОК 3-1. Заживление ран первичным, вторичным и третичным натяжением
БЛОК 3-1. Заживление ран первичным, вторичным и третичным натяжением
Первичное натяжение
День 1: Появляется фибринозный сгусток (гематомы). Нейтрофилы инфильтрируют края раны (главный хемоаттрактант – тромбоцитарный фактор роста). Наблюдается повышение митотической активности базальных клеток многослойного эпителия в краях раны (FGF, EGF вовлечены в процесс миграции кератиноцитов.
День 2: Клетки с базального слоя мигрируют под фибринозный сгусток и окружают его в течение 48 часов. Макрофаги активно мигрируют в рану (PDGF, ТФР-β привлекают их).
День 3: Грануляционная ткань начинает свое формирование (FGF, EGF, PDGFи ТФР-β вовлечены в ангиогенез). Начальное отложение коллагена III типа фибробластами начинается в результате воздействия указанных выше хемоаттрактантов на фибробласты. Макрофаги замещают нейтрофилы.
День 4-6: Грануляционная ткань формирует «узелки», а коллагеновые «мостики» связывают края раны.
Неделя 2: Отложение коллагена приводит к сдавлению кровеносных сосудов в фиброзной ткани, что снижает кровоток. Прочность ткани ~10%.
Месяц 1: Коллагеназаремоделирует содержимое раны (разрушаются пептидные связи), что приводит к деградации коллагена III типа и замещение его на коллаген I типа. Прочность значительно увеличивается и достигает ~80% к третьему месяцу. Рубцовая ткань лишена воспалительных клеток и придатков (кожи, потовых желез).
Вторичное натяжение
Обычно, данный вид заживления отличается от первичного натяжения следующим:
Более выраженной воспалительной реакцией;
Увеличением количества образуемой грануляционной ткани;
Сокращение раны обусловлены увеличением количества миофибробластов.
Третичное натяжение
Подобным образом заживают контаминированные ткани, на фоне применения антибактериальных средств или местного хирургического лечения.
Заживление раны первичным, вторичным и третичным натяжением (см. Блок 3-1) o Заживление первичным натяжением. Характерно для чистых
хирургических ран.
oЗаживление вторичным натяжением. Характерно для открытых ран, закрывающихся путем реэпителизации со сведением краев дефекта. Чаще всего наблюдается при контаминации раны.
oЗаживление третичным натяжением. Возникает при лечении первично контаминированных ран после проведения системной антибактериальной терапии и местного хирургического лечения в течение нескольких дней. После проведенной терапии используются стандартные методы – наложение швов, транспланты и пр.
4.Факторы, ухудшающие заживление ран:
Персистирующая инфекция:
o Наиболее частая причина длительно незаживающих ран; o S.aureus наиболее частый патоген;

Medicine Books (https://vk.com/medicinebook)
Рис 3-12: Синдром Элерса-Данлоса. У детей |
Рис 3-10: Типы закрытия раны. Сверху, закрытие раны |
наблюдается гиперазгибание пальцев, до такой |
первичным натяжением. Происходит в случае чистой |
степени, что они могут быть параллельны |
резанной раны (А) и сопоставлении краев раны (В) с |
предплечью. Это классический признак |
помощью швов, скоб или адгезивных полосок. При этом |
данного синдрома. |
наблюдается образование минимального количества |
|
рубцовой ткани. Внизу, заживление вторичным |
|
натяжением. Рана заживает посредством сокращения, |
|
разрастания грануляционной ткани и эпителизации (А и |
|
В). В результате образуется обширный рубец (С). |
oРоль больничного и внебольничного метицилен-резистентного золотистого стафилококка (MRSA) достаточно велика. MRSA не чувствителен к бета-лактамным антибиотикам (н. пенициллин, цефалоспорин). Нарушение кожных покровов и питания значительно
увеличивают риск раневой инфекции.
oВажнейший фактор предупреждения развития раневой инфекции – тщательное мытье рук, так как у 20-40% людей в популяции, MRSA
живет на коже ладоней.
o Внебольничный MRSA способен продуцировать лейкоцидин, приводящий к апоптозу нейтрофилов, что позволяет бактерии выживать. Прогрессирование MRSA-инфекции, может привести к развитию некротизирующего фасцита.
oТриметроприм (первая линия) и ванкомицин (вторая линия) наиболее часто используются для лечения подобных инфекций.
Сахарный диабет
oУвеличивает восприимчивость тканей к инфекции, уменьшая кровоток и сопровождаясь повышенным уровнем глюкозы в крови.
Неполноценное питание
oСниженное поступление белка;
oДефицит витамина С (смотреть раннее);
oДефицит металлов:
Дефицит меди приводит к снижению количества сшивок в коллагене (так же и в эластической ткани);
Дефицит цинка приводит к дефектам удаления коллагена III типа при ремоделировании соединительной ткани в ране. Коллаген III типа снижает механическую прочность, что приводит к ухудшению заживления ран.
Глюкокортикостероиды
oПрепятствуют образованию коллагена и снижают механическую прочность соединительной ткани;
oИспользуются для предупреждения чрезмерного образования рубцовой ткани:

Medicine Books (https://vk.com/medicinebook)
Дексаметазон используются совместно с антибиотиками для предупреждения образования рубцов при бактериальных менингитах;
Пластические хирурги используют введение стероидов для предупреждения чрезмерного роста рубцовой ткани.
Келоидные и гипертрофические рубцы
oКелоиды характеризуются разрастанием рубца за пределы изначальной раны (рис. 3-14);
Развиваются у 15-20% афроамериканцев, азиатов и испанцев; видимо существует генетическая предрасположенность;
Часто рефрактерны к медикаментозному и хирургическому
лечению.
oГипертрофические рубцы характеризуются разрастанием рубцовой ткани в пределах раны;
Как правило, регрессируют самостоятельно.
oВ «обычных» рубцах, коллаген располагается хаотично без какой-либо структурной направленности. В случае гипертрофических и келоидных рубцов, коллаген располагается упорядочено, повторяя направленность эпидермиса.
Рис 3-14: Формирование келоида. Отмечается |
Рис 3-15: Регенеративный узел при повреждении |
||||
разрастание, утолщение рубца на тыльной стороне |
печени. Отмечается удвоение печеночных балок. |
||||
кисти. В отличие от гипертрофированных рубцов, |
Балки утолщены из-за активного деления |
||||
келоиды разрастаются за пределы первоначальной |
гепатоцитов. Виден двойной ряд ядер в каждой |
||||
раны |
и |
требуют |
медикаментозного |
или |
пластине. В регенеративных узлах отсутствуют |
хирургического лечения. |
|
|
триады. |
||
5.Восстановление других видов тканей
Печень
oУмеренное повреждение (н. вирусный гепатит А)
Регенерация гепатоцитов происходит в случае сохраненнойцитоархетиктоники.
oСерьезное или персистирующее повреждение (н. вирусный гепатит С)
В регенеративных узлах наблюдается удвоение клеток в печеночных балках, с параллельно расположенными ядрами (рис. 3-15);
В регенеративных узлах отсутствуют триады;
Вокруг регенеративного узла развивается фиброз, приводящий к циррозу печени, если повреждающий агент не будет удален (см. Главу 19).
Легкие
oПневмоциты II типа - ключевые клетки в процессах легочной регенерации;
Medicine Books (https://vk.com/medicinebook)
oОни замещают поврежденные пневмоциты I и II типа, и синтезируют сурфактант.
Головной мозг
oАстроциты пролиферируют в ответ на травму (н. при инсульте). Пролиферация астроцитов носит название «глиоз»;
oМикроглиальные клетки (макрофаги) являются мусорщиками и удаляют клеточный детрит (н. разрушенный миелин).
Периферические нервы
oБез иннервации атрофия мышц происходит через ~15 дней;
oПосле разрезания нерва, происходит дистальная дегенерация аксона и миелина, а проксимальный аксон разрушается до ближайшего перехвата Ранвье.
Макрофаги и Шванновские клетки фагоцитируют детрит (аксоны и миелин);
Тела нервных клеток подвергаются центральному хроматолизису. Тела клеток надуваются, а тельца Ниссля (состоящие из шероховатого ЭПС и свободных рибосом) исчезают. Ядро при этом перемещается на периферию;
Шванновские клетки пролиферируют в сторону дистальной культи;
Аксоны из проксимальной культи начинают расти в сторону дистальной, используя Шванновские клетки в качестве проводника;
Регенерации аксона происходит со скоростью 2-3 мм в день;
Мышцы, как правило, реиннервируются.
Сердце
o Сердечная мышца – постоянная ткань.
oПоврежденные мышечные волокна замещаются несократимой рубцовой тканью.
Скелетные мышцы после выполнения физических упражнений
oПосле упражнений, в мышечных волокнах наблюдаются повреждения саркомер. Саркомеры – базовая единица мышцы, придающая волокнам
поперечную исчерченность.
oСателитные клетки, являются стволовыми элементами. Они участвуют в процессе репарации и образования новых миофибрилл в саркомерах, что позволяет восстановить их.
IV. Лабораторные признаки воспаления
1.Изменения в лейкоцитах
Острое воспаление (н. бактериальная инфекция)
oАбсолютный нейтрофильный лейкоцитоз (рис. 3-16)
Различные цитокины (н. ИЛ-1) приводят к высвобождению постмитотического пула нейтрофилов (метамиелоциты, палочко-ядерные и сегменто-ядерные нейтрофилы) из костного мозга, приводя к абсолютному (увеличение числа клеток) нейтрофильному лейкоцитозу.
Появление в анализе крови увеличенного количества палочко-
ядерных нейтрофилов и метамиелоцитов, носит название сдвига лейкоцитарной формулы влево.
oТоксическая зернистость
Определение – наличие темно-синих или пурпурных первичных гранул в метамиелоцитах, палочко- и сегментоядерных нейтрофилах.
