
3 курс / Патологическая физиология / pecheni
.pdf
Тема: Патофизиология печени
Печень – жизненно важный орган с многообразными функциями, направленными на поддержание гомеостаза в организме. Структурно-функциональная единица печени - печеночный ацинус. В печени происходят:
1.Образование желчных пигментов, синтез холестерина, синтез и секреция желчи.
2.Обезвреживание токсичных продуктов, поступающих из желудочно-кишечного тракта.
3.Синтез белков, в том числе протеинов плазмы крови, их депонирование, переаминирование и дезаминирование аминокислот, образование мочевины и синтез креатина.
4.Синтез гликогена из моносахаридов и неуглеводных продуктов.
5.Окисление жирных кислот, образование кетоновых тел.
6.Депонирование и обмен многих витаминов (A, PP, B, D, K), депонирование ионов железа, меди, цинка, марганца, молибдена и др.
7.Синтез большинства ферментов, обеспечивающих метаболические процессы.
8.Регуляция равновесия между свертывающей и антисвертывающей системами крови, образование гепарина.
9.Разрушение некоторых микроорганизмов, бактериальных и других токсинов.
10.Депонирование плазмы крови и форменных элементов, регуляция системы крови.
11.Кроветворение у плода.
Печеночная недостаточность. Этиология, патогенез, проявления
Печѐночная недостаточность – стойкое снижение или полное выпадением одной, нескольких или всех функций печени, приводящее к нарушению жизнедеятельности организма.
Классификация
Выделяют несколько видов печѐночной недостаточности.
Рис. 1. Виды печѐночной недостаточности.
По происхождению.
•Печѐночно-клеточная (паренхиматозная). Является результатом первичного повреждения гепатоцитов и недостаточности их функции.
•Шунтовая (обходная). Обусловлена нарушением тока крови в печени и, в связи с этим, еѐ сбросом (минуя печень) по портокавальным анастомозам в общий кровоток.
По скорости возникновения и развития.
•Острая. Развивается в течение нескольких суток.
•Хроническая. Формируется в течение нескольких недель, месяцев или лет.
По числу нарушенных функций: парциальная и тотальная.
В зависимости от обратимости повреждения гепатоцитов.
1

•Обратимая. Исчезновение признаков печеночной недостаточности наблюдается при прекращении воздействия патогенного агента и устранении последствий этого воздействия.
•Необратимая (прогрессирующая). Развивается в результате продолжающегося влияния причинного фактора или неустранимости патогенных изменений, вызванных им.
Причины печеночной недостаточности.
•Внепечѐночные: нарушение кровообращения (сердечная недостаточность, шок), гипоксия (например, циркуляторная при сердечной недостаточности, тканевая при интоксикациях), хроническая почечная недостаточность, эндокринопатии (например, острая недостаточность надпочечников), гипо- и дисвитаминозы (например, гиповитаминоз E),
•Печѐночные: гепатиты, дистрофии (гепатозы), циррозы, опухоли, холестаз (камни, опухоли, воспаление желчевыводящих путей), паразитарные поражения печени, расстройства внутрипеченочного кровообращения.
Рис. 2. Основные причины печѐночной недостаточности.
Дистрофии печени наиболее часто развиваются под действием химических веществ (например, антибиотиков, сульфаниламидов, наркотиков; промышленных ядов — бензола, четырѐххлористого углерода, метанола, этанола и др. спиртов, отравлений грибами).
Гепатиты — диффузное воспаление ткани печени. Обычно возникают в результате вирусной инфекции или интоксикации.
Циррозы печени — хронически протекающие патологические процессы в печени, характеризующиеся прогрессирующим повреждением и гибелью гепатоцитов, а также развитием избытка соединительной ткани (фиброзом). Проявляется недостаточностью функций печени и нарушением кровотока в ней.
Патогенез. Модификация и деструкция мембран гепатоцитов, развитие иммунопатологических, воспалительных, свободно-радикальных процессов, активация гидролаз приводит к массированному разрушению клеток печени, выходу в интерстиций их содержимого, включая многочисленные гидролитические ферменты.
Всѐ это приводит к снижению массы функционирующей печѐночной паренхимы и развитию печѐночной недостаточности.
2
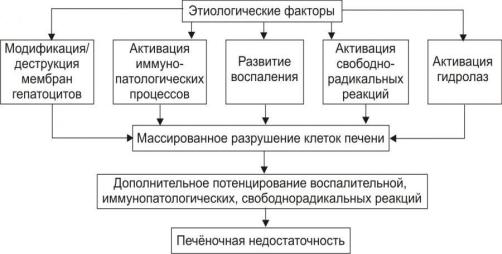
Рис. 3. Основные общие звенья патогенеза печѐночной недостаточности.
Проявления печеночной недостаточности
Печѐночная недостаточность характеризуется признаками расстройств обмена веществ и функций печени.
Нарушение углеводного обмена. Печень участвует в поддержании нормального уровня глюкозы в сыворотке крови путем гликогеногенеза, гликогенолиза и глюконеогенеза. Снижается способность гепатоцитов, с одной стороны, превращать глюкозу в гликоген, а с другой – расщеплять гликоген до глюкозы. Это обусловливает характерный признак печеночной недостаточности – неустойчивый уровень глюкозы крови. После приема пищи развивается гипергликемия, а натощак – гипогликемия.
Нарушение белкового и ферментного обменов проявляется в изменении расщепления белков (до аминокислот), синтеза белков, дезаминирования, трансаминирования, декарбоксилирования аминокислот, образования мочевины, мочевой кислоты, аммиака, креатина.
Вследствие этого возникают следующие нарушения:
Гипопротеинемия – снижение уровня белка обычно отражает нарушение белковосинтетической функции печени. Гепатоциты синтезируют практически весь альбумин, до 85% глобулинов.
Диспротеинемия развивается при синтезе в печени качественно измененных глобулинов (парапротеинов – макроглобулинов, криоглобулинов).
Нарушение метаболизма аминокислот приводит к повышению уровня свободных аминокислот в крови и моче (аминоацидемия, аминоацидурия).
Геморрагический синдром развивается вследствие нарушения синтеза факторов свертывания и ингибиторов коагуляции и фибринолиза.
Увеличение остаточного азота и аммиака в крови обнаруживается при нарушении синтеза мочевины (показатель тяжелой печеночной недостаточности).
Повышение содержания в крови ряда ферментов (аминотрансфераз и др.). Наибольшее диагностическое значение имеет определение в сыворотке крови активности аминотрансфераз - АлАТ и АсАТ. Их активность является наиболее надежным показателем цитолиза гепатоцитов. Из маркѐров холестаза (экскреторные ферменты) наибольшее клиническое значение приобретает определение в крови активности щелочной фосфатазы. Повышение активности щелочной фосфатазы является важным показателем нарушения жѐлчеоттока (холестаза).
Нарушение жирового обмена.
3
•Нарушение синтеза в гепатоцитах ЛПНП и ЛПОНП (обладающих атерогенными эффектами), а также ЛПВП (оказывающих антиатерогенное действие) нередко сопровождается развитием липидной дистрофии печени (жирового гепатоза).
•Повышение в плазме крови уровня холестерина (обладающего проатерогенным свойством).
Нарушение обмена гормонов. Нарушение обмена гормонов и биологически активных веществ проявляется в изменении:
•синтеза гормонов (из фенилаланина образуется тирозин – предшественник тироксина, трийодтиронина, катехоламинов), транспортных белков (транскортина, связывающего 90% глюкокортикоидов);
•инактивации гормонов (стероидных гормонов, катехоламинов, инсулина);
•инактивации биологически активных веществ (окислительного дезаминирования серотонина и гистамина).
Поражение печени и нарушение инактивации таких гормонов, как инсулин, тироксин, кортикостероиды, андрогены, эстрогены ведет к изменению их содержания в крови и развитию соответствующей эндокринной патологии. Уменьшение дезаминирования БАВ может усугубить клинические проявления аллергии при патологии печени.
Нарушение обмена витаминов характеризуется:
•уменьшением всасывания жирорастворимых витаминов (A, D, E, K) в результате нарушения желчевыделительной функции печени;
•нарушением синтеза витаминов и образования активных форм (вит. А из каротина, активных форм витамина В6 и др.);
•нарушением депонирования витаминов (В12, фолиевой, никотиновой кислот и др.) и их экскреции. В результате нарушения обмена витаминов многие патологические процессы в печени могут сопровождаться гиповитаминозами.
Нарушение обмена минеральных веществ (железо, медь, хром). Например, при наследственной патологии — гемохроматозе в ткани печени накапливается железо, развиваются гепатомегалия и цирроз.
Нарушения функций печени.
Дезинтоксикационная функция. Характеризуется снижением эффективности процессов детоксикации в печени: • эндогенных токсинов (образующихся и накапливающихся в кишечнике
—фенолов, скатолов, аммиака, путресцина, кадаверинов и патогенных продуктов метаболизма
—низкомолекулярных жирных кислот, сульфатированных аминокислот и др.); • экзогенных ядовитых веществ (например, токсинов грибов и микробов; ядохимикатов; ЛС).
Антимикробная функция. При печѐночной недостаточности страдают фагоцитоз клетками Купфера различных микроорганизмов, транспорт IgА в жѐлчь, где они оказывают бактериостатическое и бактерицидное действие.
Желчеобразование и желчевыделение (с развитием желтух и нарушений пищеварения).
Основные синдромы печеночной недостаточности Синдром нарушенного питания (ухудшение аппетита, тошнота, боли в животе,
неустойчивый стул, похудание, появление анемии). В основе этого синдрома лежат нарушения обменных процессов.
Синдром желтухи.
Синдром эндокринных расстройств. Отмечаются снижение либидо, атрофия яичек, бесплодие, гинекомастия, атрофия молочных желез, матки, нарушение менструального цикла. Возможно развитие сахарного диабета и вторичного альдостеронизма;
Синдром нарушенной гемодинамики – накопление гистаминоподобных и других вазоактивных веществ, приводящее к вазодилатации (компенсаторное повышение сердечного выброса в сочетании с гипотензией).
4
Отечно-асцитический синдром обусловливают снижение синтеза альбуминов и падение онкотического давления, а также развитие вторичного альдостеронизма.
Специфический печеночный запах (fetor hepaticis) связан с выделением метилмеркаптана. Это вещество образуется из метионина, который накапливается в связи с нарушением в печени процессов деметилирования и может содержаться в выдыхаемом воздухе;
«Печеночные знаки» – телеангиэктазии (сосудистые звѐздочки) и пальмарная эритема. Синдром геморрагического диатеза – снижение синтеза факторов свертывания крови и
частые кровотечения обусловливают возможность развития ДВС-синдрома.
Печѐночная кома. Определение, виды, патогенез
Печеночная кома (от греч. koma – глубокий сон) развивается как финальный этап прогрессирующей печѐночной недостаточности.
Причиной печеночной комы является интоксикация организма, повреждение органов и тканей (прежде всего ЦНС) продуктами метаболизма, траснсформация, обезвреживание и выделение которых с участием печени грубо нарушено.
Печеночная кома характеризуется утратой сознания, отсутствием рефлексов и расстройствами жизнедеятельности организма (включая нарушения дыхания и кровообращения), чреватыми смертью.
Виды печеночной комы.
•Паренхиматозная кома. Интоксикация организма в связи с повреждением и гибелью значительной массы печени (например, при еѐ травме, некрозе, удалении). В результате этого нарушаются все функции печени. Наибольшее патогенное значение при этом имеет утрата дезинтоксикационной функции.
•Шунтовая кома («обходная»). При сбросе крови из системы портальной вены в общий кровоток, минуя печень. Чаще возникает при циррозах в случае развития мощных коллатералей между системами воротной и нижней полой вен.
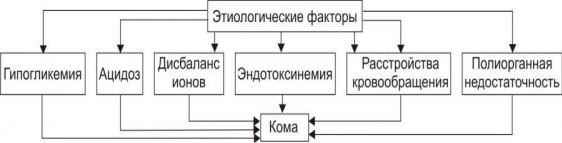
Рис. 4. Основные факторы патогенеза печѐночных коматозных состояний.
Патогенез печеночной комы.
•Гипогликемия. Является результатом нарушения гликогенеза и гликогенолиза.
•Ацидоз (метаболический, на финальных стадиях дополнительно развивается респираторный и выделительный ацидоз).
•Дисбаланс ионов в клетках, интерстициальной жидкости и в крови (в крови нарастает
[K+], в клетках — [Na+], [Ca2+], [H+]).
•Интоксикация организма — эндотоксинемия (особенно продуктами белкового и липидного метаболизма, а также непрямым билирубином, что обусловлено нарушением его трансформации и конъюгации с глюкуроновой кислотой).
•Нарушения центральной, органно-тканевой и микрогемоциркуляции как следствие сердечной недостаточности, нарушения тонуса артериол.
5
• Полиорганная недостаточность. Ранее всего и наиболее выраженно нарушается функции сердца, дыхательного и сосудодвигательного центров. Последнее приводит к смешанной гипоксии, прекращению сердечной деятельности, дыхания и смерти пациента.
Синдром портальной гипертензии
Синдром портальной гипертензии возникает вследствие нарушения кровотока в воротной вене. Портальная гипертензия — стойкое повышение давления в сосудах системы воротной вены выше нормы (т.е. выше 6 мм рт.ст.).
Виды портальной гипертензии.
1.Надпеченочная портальная гипертензия возникает вследствие компрессии или тромбоза печеночных вен, правожелудочковой недостаточности, перикардита и характеризуется затруднением венозного оттока от печени.
2.Внутрипеченочная портальная гипертензия развивается при циррозе, опухолях, эхинококкозе и других поражениях печени.
3.Подпеченочная портальная гипертензия связана с тромбозом или компрессией воротной вены (рубцы, сдавление асцитической жидкостью, опухолью) либо с аномалиями ее развития.
Основным звеном патогенеза портальной гипертензии является застой крови в системе воротной вены.
Портальная гипертензия сопровождается компенсаторным шунтированием крови через портокавальные анастомозы (нижняя треть пищевода и кардиальная часть желудка, передняя брюшная стенка в области пупка – «голова Медузы» (caput Medusae), система геморроидальных вен) с последующим варикозным расширением сосудов. Это делает стенки сосудов уязвимыми к механическим повреждениям, исходом которых могут быть желудочно-кишечные кровотечения, нередко заканчивающиеся летально. Длительно текущая портальная гипертензия нередко приводит к дистрофии печени и еѐ недостаточности.
Характерное проявление портальной гипертензии – клиническая триада: возникновение коллатерального венозного кровообращения (расширение портокавальных анастомозов – «голова Медузы»), асцит и увеличение селезенки (спленомегалия).
Последствия портальной гипертензии:
• спленомегалия – увеличение размеров селезенки,
• гиперспленизм – повышение функции селезенки, следствием чего являются панцитопения (тромбоцитопения, анемия, лейкопения)
• асцит – скопление жидкости в брюшной полости.
В механизме развития асцита играют роль следующие патогенетические факторы:
• повышение давления в воротной вене;
• снижение онкотического давления крови в связи с нарушением белок-синтезирующей функции печени (гипопротеинемия);
• нарушение лимфообращения;
• вторичный альдостеронизм (активация РААС, снижения метаболизма в печени), что сопровождается гипернатриемией, гипокалиемией, гиперволемией.
• увеличение проницаемости стенки сосудов в результате гипоксии, ацидоза и эндогенной интоксикации.
Асцит проявляется вздутием живота и прогрессирующим нарастанием массы тела. Наиболее частым осложнением асцита является бактериальный перитонит (возникает при инфицировании асцитической жидкости, в 90% случаев происходит спонтанно).
6
Желтуха. Виды, причины, патогенез, проявления
Желтуха (icterus) – симптомокомплекс, характеризующийся избыточным содержание в крови, интерстициальной жидкости и тканях компонентов жѐлчи, обусловливающее желтушное окрашивание кожи, слизистых оболочек и мочи.
Все виды желтух объединены одним признаком — гипербилирубинемией, от которой зависит степень и цвет окраски кожи: от светло-лимонной до оранжево-жѐлтой, зелѐной или оливково-жѐлтой. Видимая желтуха появляется при гипербилирубинемии более 35 мкмоль/л.
Гипербилирубинемия – следствие нарушений в одном или нескольких звеньях обмена билирубина.
Различают следующие фракции билирубина:
• Свободный, он же непрямой, несвязанный, неконъюгированный.
•Связанный, он же прямой, конъюгированный.
Метаболизм билирубина.
•Высвобождение гема из гемоглобина, миоглобина и цитохромов. Более 80% гема образуется в результате разрушения эритроцитов и около 20% — миоглобина и цитохромов.
•Трансформация протопорфирина гема в биливердин. Происходит под влиянием микросомальных оксидаз гепатоцитов.
•Окисление биливердина с образованием непрямого билирубина (неконъюгированный, свободный билирубин). Непрямой билирубин, циркулирующий в крови, связан с альбуминами и поэтому не фильтруется в почках и отсутствует в моче.
•Транспорт непрямого билирубина в гепатоциты, где он образует комплекс с белками и глутатион–S–трансферазами.
•Диглюкуронизация билирубина в гепатоцитах с образованием растворимого в воде конъюгированного билирубина. Прямой билирубин не связан с альбумином. В связи с этим он активно («прямо») взаимодействует с диазореактивом Эрлиха, выявляющим этот пигмент.
•Экскреция конъюгированного билирубина в желчевыводящие пути.
Очень важным является положение о том, что в нормальных условиях транспорт билирубина через гепатоцит происходит только в одном направлении – от кровеносного к жѐлчному капилляру. При повреждении гепатоцита (некроз) или препятствии для прохождения жѐлчи (на уровне жѐлчных ходов или ниже) возможна регургитация конъюгированного билирубина, его движение в обратном направлении – в кровеносный капилляр. Метаболизм билирубина в печени осуществляется в три этапа: 1. захват гепатоцитом билирубина из крови, 2. связывание билирубина с глюкуроновой кислотой (обеспечивает фермент глюкуронилтрансфераза), 3. выделение конъюгированного билирубина в систему жѐлчных протоков.
• Трансформация конъюгированного билирубина:
-в уробилиноген (в верхнем отделе тонкой кишки), всасывающийся в тонкой кишке и попадающий по системе воротной вены в печень, где разрушается в гепатоцитах.
-в стеркобилиноген (в основном в толстом кишечнике), большая часть которого выделяется с экскрементами, окрашивая их; другая часть всасывается в кровь геморроидальных вен, попадая в общий кровоток и фильтруется в почках (в норме придавая моче соломенножѐлтый цвет).
7
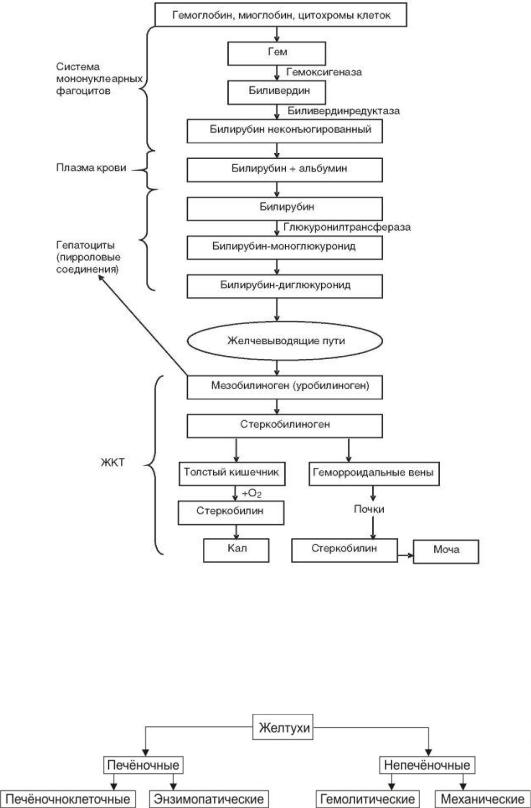
Рис. 5. Метаболизм билирубина. ЖКТ – желудочно-кишечный тракт.
Классификация желтух. Все желтухи в зависимости от происхождения подразделяют на две группы: печѐночные и непечѐночные.
Рис. 6. Виды желтух по происхождению.
Печѐночные желтухи (паренхиматозные и энзимопатические) возникают при первичном повреждении гепатоцитов. Непечѐночные желтухи первично не связаны с повреждением гепатоцитов. К ним относятся гемолитические (надпечѐночные) и механические (подпечѐночные) желтухи.
8
Гемолитическая желтуха. Причины. Избыточное разрушение эритроцитов, обусловленное внутри- и внеэритроцитарными факторами (см. гемолитические анемии).
Помимо проявлений, обусловленных гемолизом эритроцитов (анемии, гемоглобинурии), отмечается повышение содержания в крови непрямого билирубина. Это является результатом избыточного его образования из гемоглобина и неспособностью нормального гепатоцита захватить и трансформировать избыточно содержащийся в протекающей крови непрямой билирубин.
Избыток непрямого билирубина в крови обусловливает окрашивание кожи и слизистых оболочек (степень окраски зависит от интенсивности гемолиза).
Одновременно с эти в большей мере окрашиваются кал и моча, поскольку в них увеличивается концентрация стеркобилиногена (гиперхолия - увеличенная секреция желчи в кишечник).
В случае желтухи, обусловленной массивным гемолизом эритроцитов, в крови и моче обнаруживается уробилиноген. В общий кровоток уробилиноген попадает, «проскакивая» печеночный барьер в связи с высокой концентрацией пигмента в крови портальной вены. Это обусловлено в свою очередь избытком образования прямого билирубина в печени, а следовательно – уробилиногена в тонкой кишке, откуда он всасывается в портальную вену и поступает в печень.
Механическая желтуха. Механическая желтуха развивается при стойком нарушение выведении жѐлчи по жѐлчным капиллярам (что приводит к внутрипечѐночному холестазу), по жѐлчным протокам и из жѐлчного пузыря.
Причины.
•Закрывающие желчевыводящие пути изнутри (например, конкременты, опухоли, паразиты).
•Сдавливающие жѐлчные пути снаружи (например, новообразования головки поджелудочной железы или большого дуоденального сосочка; рубцовые изменения ткани вокруг желчевыводящих путей; увеличенные лимфоузлы).
•Нарушающие тонус и снижающие моторику стенок желчевыводящих путей (дискинезии).
Патогенез. Указанные факторы обусловливают повышение давления в жѐлчных капиллярах, перерастяжение (вплоть до микроразрывов) и повышение проницаемости стенок желчеотводящих путей, диффузию компонентов жѐлчи в кровь.
В случаях острой полной обтурации жѐлчевыводящих путей возможен разрыв жѐлчных капилляров. При этом жѐлчь, вступая в контакт с печеночной тканью, вызывает ее повреждение и развитие воспалительного процесса, что получило название билиарного гепатита.
Проявления механической желтухи.
Для механической желтухи характерно развитие холемии и ахолии.
Синдром холемии (желчекровия) — комплекс расстройств, обусловленных появлением в крови компонентов жѐлчи, главным образом — жѐлчных кислот (гликохолевой, таурохолевой и др.), прямого билирубина и холестерина.
Признаки холемии.
•Высокая концентрация конъюгированного билирубина в крови (с развитием желтухи) и как следствие — в моче (придает моче тѐмный цвет).
•Избыток холестерина накапливается в тканях в виде ксантом (в коже кистей, предплечий, стоп).
•Зуд кожи вследствие раздражения жѐлчными кислотами нервных окончаний.
•Артериальная гипотензия вследствие снижения базального тонуса ГМК артериол, уменьшение адренореактивных свойств рецепторов сосудов и сердца, повышения тонуса бульбарных ядер блуждающего нерва под действием жѐлчных кислот.
9
•Брадикардия вследствие прямого тормозного влияния жѐлчных кислот на клетки синусно-предсердного узла.
•Повышенная раздражительность и возбудимость пациентов в результате снижения активности тормозных нейронов коры больших полушарий под действием компонентов жѐлчи.
•Депрессия, нарушение сна и бодрствования, повышенная утомляемость (развивается при хронической холемии).
Синдром ахолии — состояние, характеризующееся значительным уменьшением или прекращением поступления жѐлчи в кишечник, сочетающееся с нарушением полостного и мембранного пищеварения.
Признаки ахолии.
•Стеаторея — наличие жира в кале, что обусловлено нарушением эмульгирования, переваривания и усвоения жира в кишечнике в связи с дефицитом жѐлчи.
•Дисбактериоз.
•Кишечная аутоинфекция и интоксикация вследствие отсутствия бактерицидного и бактериостатического действия жѐлчи. Это способствует активации процессов гниения и брожения в кишечнике и развитию метеоризма.
•Полигиповитаминоз (в основном, за счѐт дефицита жирорастворимых витаминов A, D, E, K). Дефицит жирорастворимых витаминов приводит к нарушению сумеречного зрения, деминерализации костей с развитием остеомаляции и переломов, снижение эффективности системы антиоксидантной защиты тканей, развитию геморрагического синдрома.
•Обесцвеченный кал вследствие уменьшения или отсутствия жѐлчи в кишечнике.
Печеночная желтуха. К печеночной желтухе относят печеночно-клеточную (паренхиматозную) и энзимопатическую разновидности желтух.
Паренхиматозная желтуха развивается при острых и хронических заболеваниях печени любой этиологии (вирусной, алкогольной, аутоиммунной), а также при тяжело протекающих инфекциях (тифы, малярия, острая пневмония), сепсисе, отравлениях грибами, фосфором, хлороформом и другими ядами.
Практически при любом варианте повреждения печени нарушается жѐлчеобразовательная и жѐлчевыделительная функция гепатоцитов в зоне поражения.
Ранними специфическими признаками поражения гепатоцитов являются высокий уровень в крови печеночных трансаминаз (АлАТ, АсАТ), легко проникающих через поврежденную клеточную мембрану.
Врезультате поражения гепатоцитов печеночные клетки выделяют жѐлчь в кровеносные сосуды (развивается холемический синдром). В крови отмечается гипербилирубинемия как за счет прямого, так и непрямого билирубина, что связано со снижением активности глюкуронилтрансферазы в поврежденных гепатоцитах и нарушением образования прямого билирубина.
Моча имеет темный цвет за счет билирубинурии (прямой билирубин) и уробилинурии (нарушено превращение уробилиногена в поврежденных гепатоцитах, всасывающегося в кровь из тонкой кишки и поступающего в печень).
Энзимопатические желтухи обусловлены нарушением метаболизма билирубина в гепатоцитах. Речь идет о парциальной форме печеночной недостаточности, связанной с уменьшением или невозможностью синтеза ферментов, участвующих в пигментном обмене. По происхождению эти желтухи, как правило, наследственные. Вместе с тем некоторые формы наблюдаются после перенесенных ранее заболеваний печени.
Взависимости от механизма развития выделяют следующие формы энзимопатических
желтух.
Синдром Жильбера. В основе развития этой желтухи лежит нарушение активного захвата и транспорта непрямого билирубина из крови в печеночную клетку. Причиной еѐ является генетический дефект синтеза соответствующих ферментов. При этом повышение уровня
10
