

общедоступными методами; в) смешиваться в необходимых соотношениях с титруемым раствором; г) быть устойчивыми в течение достаточно длительного времени; д) быть окрашенными.
Способы приготовления стандартных растворов
Рассмотрены ранее. Это метод точной навески, неточной навески,
из фиксанала и метод разведения.
Требования, предъявляемые к реакциям в титриметрии:
 реакция должна протекать необратимо и количественно;
реакция должна протекать необратимо и количественно;
 скорость реакции должна быть высокой;
скорость реакции должна быть высокой;
 должны отсутствовать побочные реакции;
должны отсутствовать побочные реакции;
 реакции между исследуемыми веществом и титрантом должны идти стехиометрично, т.е. соответствовать коэффициентам в уравнении реакции.
реакции между исследуемыми веществом и титрантом должны идти стехиометрично, т.е. соответствовать коэффициентам в уравнении реакции.
должна легко и точно фиксироваться точка эквивалентности.
Классификация титриметрических методов анализа
1. По типу основной реакции, протекающей при титровании, различают:
а) Методы кислотно-основного титрования (нейтрализации), основанные на переносе протона.
Na2CO3 + 2HCl |
2NaCl + H2O + CO2 |
б) Методы окисления-восстановления. |
|
5Fe2+ + MnO4- + 8H+ |
5Fe3+ + Mn2+ + 4H2O |
в) Методы комплексообразования. |
|
3K4[Fe(CN)6]+4FeCl3→Fe4[Fe(CN)6]3 +12KCl |
|
г) Методы осаждения. |
|
AgNO3 + NaCl |
AgCl↓ +NaNO3 |
2. По химическим процессам.
Классификация титриметрических методов электронной пары, а также процессов осаждения (табл.2).
40

Таблица 2.
|
|
Вещества, |
|
Метод титрования |
Подгруппы метода |
применяемые для |
|
приготовления |
|||
|
|
||
|
|
титрантов |
|
|
|
|
|
Кислотно-основное |
Ацидиметрия (Н+) |
HCl |
|
|
|
|
|
|
Алкалиметрия (ОН-) |
NaOH, Na2CO3 |
|
|
|
|
|
|
Перманганатометрия |
KMnO4 |
|
|
|
|
|
|
Иодометрия |
I2 |
|
|
|
|
|
|
Дихроматометрия |
K2Cr2O7 |
|
|
|
|
|
Окислительно- |
Броматометрия |
KBrO3 |
|
|
|
||
Иодатометрия |
KIO3 |
||
Восстановительное |
|||
|
|
||
Цериметрия |
Ce(SO4)2 |
||
|
|||
|
|
|
|
|
Ванадатометрия |
NH4VO3 |
|
|
|
|
|
|
Титанометрия |
TiCl3 |
|
|
|
|
|
|
Хромометрия |
CrCl2 |
|
|
|
|
|
Комплексонометрия |
Меркуриметрия |
Hg(NO3)2 |
|
|
|
||
Комплексонометрия |
ЭДТА |
||
|
|||
|
|
|
|
Осадительное |
Аргентометрия |
AgNO3 |
|
|
|
||
Меркурометрия |
Hg2(NO3)2 |
||
|
|||
|
|
|
2. По приемам титрования.
а) Способ прямого титрования заключается в непосредственном титровании определяемого вещества (А) рабочим раствором (В): А+В=С+Д.
Например, раствор кислоты HCl с известной концентрацией по каплям прибавляют к щелочи с неизвестной концентрацией.
б) Способ обратного титрования. Реактив В прибавляют к исследуемому раствору А в точно отмеренном избыточном количестве, а затем
41
оттитровывают этот избыток каким-либо другим реактивом Е: В+Е=А+G. Этот метод пригоден для определения легко изменяющихся на воздухе веществ.
Кислотно-основное титрование.
Метод кислотно-основного титрования основан на реакции нейтрализации кислоты с щелочью. Этот метод позволяет определить содержание кислот и щелочей в растворе, а также концентрации солей при гидролизе которых образуются кислоты и основания (например NaHCO3).
Сущность метода заключается во взаимодействие катионов водорода и гидроксид иона, приводящее к образованию воды.
H+ + OH- = H2O
В зависимости от применяемых стандартных растворов различают ацидиметрию и алкалиметрию. При ацидиметрии в качестве стандартных растворов используют растворы кислот, при алкалиметрии – растворы щелочей.
Метод нашел широкое применение в медицинской практике, в частности используется для определения аммиака, кислот в моче, кислотности желудочного сока, состава крови и т.д. Кроме медицинской практики метод применяют при анализе питьевой и сточных вод, пищевых продуктов, объектов окружающей среды.
В реакциях нейтрализации изменяется концентрация ионов водорода.
Заканчивается нейтрализация тогда, когда прореагируют эквивалентные количества веществ. Зная объемы растворов реагирующих веществ и концентрацию одного из них, вычисляют концентрация раствора неизвестного вещества.
Кислотно-основное титрование предполагает: выбор титранта, способ его приготовления, способ фиксирования точки эквивалентности.
42
Для определения концентрации кислот используют буру Na2B4O7 и
карбонат натрия Na2CO3, т.к. эти вещества – устойчивые на воздухе соединения и из них можно готовить растворы методом точной навески.
Если есть и бура и сода, то в первую очередь берется соединение , которое обладает большей молекулярной массой, что бы ошибка при взвешивании была меньше.
Использование этих солей диктуется тем, что они образованы слабой кислотой и сильным основанием, в растворах полностью подвергаются гидролизу с выделением эквивалентного количества щелочи и которое вступает во взаимодействие с кислотой:
Na2B4O7+7H2O=2NaOH+4H3BO3
Na2CO3+ H2O=2NaOH+NaOH
Если Na2CO3 и Na2B4O7 нет, то можно определять концентрацию кислот вторичными стандартами NaOH и КOH, но предварительно нужно установить точную концентрацию этих веществ титрованием щавелевой кислотой.
Кривые кислотно-основного титрования
В процессе титрования происходит изменение рН титруемого раствора.
Так при титровании кислоты щелочью вначале среда кислая, затем рН увеличивается, т.к. концентрация кислоты уменьшается. При нейтрализации кислоты щелочью реакция нейтральная, а при избытке щелочи становится щелочной.
Кривые титрования – графическое изображение изменения величины рH
раствора в процессе титрования. Кривые строятся с помощью прибора рН-
метра. Эти кривые даны теоретически для разных видов титрования. 1.Рассмотрим титрование сильной кислоты сильным основанием
HCl+NaOH=NaCl+H2O
43

Особенно резкое изменение рН
происходит около точки эквивалентности.
Резкое изменение изменение рН вблизи
точки эквивалентности, которое
вызывается последней каплей титранта,
называется скачком титрования. В
данном случае скачок титрования при рН
4-10. При этом соль NaCl не
гидролизуется. |
Поэтому |
точка |
эквивалентности |
всегда совпадает с |
|
точкой нейтральности (рН 7). |
|
|
2. Титрование слабой кислоты сильным основанием.
СН3СООН+ NaOH=СН3СООNa+ H2O
Уксусная кислота – слабый электролит.
Поэтому концентрация Н+ не равна концентрации кислоты.
Соль СН3СООNa гидролизуется и в результате появляется избыток ионов ОН. В этом случае Т.Э. не совпадает с точкой нейтральности и лежит в щелочной области. Т.Э.~9. Скачок титрования =8-10 рН
3. Титрование слабого основания сильной кислотой
NH4OH+HCl=NH4Cl+ H2O
44

Соль NH4Cl гидролизуется и в растворе появляется избыток ионов Н+. В
этом случае Т.Э. находится в кислой области и равна ~5рН. Скачок титрования при 6-4рН.
Титрование слабой кислоты слабым основанием на практике не
применяется, т.к. трудно фиксируется точка эквивалентности.
Таким образом рН в точке эквивалентности определяется характером
образующейся в результате реакции нейтрализации соли – подвергается или не
подвергается соль гидролизу.
Правило выбора индикатора в кислотно-основном титровании.
При титровании используют такой индикатор, который изменяет свою окраску около Т.Э., т.е. интервал перехода окраски индикатора должен совпадать или захватывать скачок титрования на кривой титрования.
|
|
|
|
|
Интервал |
|
|
|
Скачок |
|
|
перехода |
|
Кислота |
Основание |
Т.Э. |
Индикатор |
окраски |
||
титрования |
||||||
|
|
|
|
индикатор |
||
|
|
|
|
|
||
|
|
|
|
|
ов |
|
|
|
|
|
|
|
|
|
|
|
~7 |
Фенолфталеин |
8-10 рН |
|
Сильная |
Сильное |
4-10 рН |
Метиловый |
|||
|
3-4,5 рН |
|||||
рН |
оранжевый |
|||||
|
|
|
||||
|
|
|
|
|||
|
|
|
|
Лакмус |
|
|
|
|
|
|
|
|
|
|
|
45 |
|
|
|
|
|
|
|
|
5-8 рН |
|
Слабая |
Сильное |
8-10 рН |
~9 |
Фенолфталеин |
8-10 рН |
|
рН |
||||||
|
|
|
|
|
||
|
|
|
|
|
|
|
Сильная |
Слабое |
6-4 рН |
~5 |
Метиловый |
3-4,5 рН |
|
рН |
оранжевый |
|||||
|
|
|
|
|||
|
|
|
|
|
|
Достоинства титриметрического анализа:
1.Быстрота определения
2.Простота оборудования
3.Возможность автоматизации
4.Точность определения – относительная погрешность 0,1-0,01%.
5. |
Возможность определять как малые, так и |
большие количества |
определяемых веществ. |
|
|
6. |
Возможность определять два и более вещества одновременно. |
|
Ограничениями метода являются: 1.Требуется стандартизация титранта.
2.Невозможность использования нестехиометрических реакций,
кинетических реакций.
3.Невысокая чувствительность
46

6. НИРС. ЛАБОРАТОРНАЯ РАБОТА
Приготовление растворов NaOH . Определение концентрации приготовленного раствора NaOH по стандартному раствору щавелевой кислоты.
Цель занятия:
Научить студентов готовить растворы разной концентрации, используя различную химическую посуду; познакомиться с титриметрическим анализом и его применением на практике.
Студент должен знать:
Роль растворов в жизнедеятельности организма, классификацию растворов, способы выражения концентраций растворов, методы приготовления растворов, основы титриметрического анализа.
Студент должен уметь:
Решать задачи на приготовление растворов, готовить растворы различной концентрации, определять концентрацию неизвестного раствора методом титрования, сущность метода нейтрализации и применение его для определения концентрации кислот, оснований и солей подвергающихся гидролизу.
Студент должен владеть:
-навыками безопасной работы в химической лаборатории
-навыками приготовления растворов определенной концентрации;
-физико-химическими методом исследованияметодом нейтрализации.
Каждый студент получает задание на приготовление раствора, готовит раствор и определяет его концентрацию методом нейтрализации.
|
Варианты заданий: |
|
1. |
Приготовьте 50 мл 0,025N раствора NaOH разбавлением 1N раствора NaOH |
|
. |
Рассчитайте массовую долю полученного раствора, считая |
1г/мл. |
47

Определите точную концентрацию этого раствора по стандартному раствору
Н2С2О4 и титр.
2. Приготовьте 50 г 0,02% раствора NaOH разбавлением 0,4% раствора NaOH .
Рассчитайте молярную концентрацию эквивалента (N) полученного раствора,
считая |
1,08г/мл. Определите точную концентрацию этого раствора по |
||
стандартному раствору Н2С2О4 . |
|
||
3. Приготовьте 50 мл 0,025N |
раствора NaOH разбавлением 0,4 N раствора |
||
NaOH . Рассчитайте массовую |
долю полученного раствора, считая |
1,05г/мл. |
|
Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
4. Приготовьте 50 г 0,5% раствора NaOH разбавлением 1,55% раствора NaOH
. Рассчитайте нормальную концентрацию полученного раствора, считая
1,03г/мл. Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
5. Приготовьте 25 мл 0,04 N раствора NaOH разбавлением 0,1N раствора
NaOH . Рассчитайте массовую долю полученного раствора, считая  1г/мл.
1г/мл.
Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
6. Приготовьте 75 г 0,75% раствора NaOH разбавлением 3,80% раствора NaOH
. Рассчитайте молярную концентрацию (М) полученного раствора, считая 
1,045г/мл.
Определите точную концентрацию этого раствора по стандартному
раствору Н2С2О4 и титр.
7. Приготовьте 50 мл 0,25N раствора NaOH разбавлением 1 N раствора NaOH
. Рассчитайте массовую долю полученного раствора, считая его  1,05г/мл.
1,05г/мл.
Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
8. Приготовьте 40 г 0,5% раствора NaOH разбавлением 2,55% раствора NaOH
. Рассчитайте нормальную концентрацию полученного раствора, считая
48

1,03г/мл. Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
9. Приготовьте 65 г 1,% раствора NaOH разбавлением 3,85% раствора NaOH .
Рассчитайте нормальную концентрацию полученного раствора, считая
1,08г/мл. Определите точную концентрацию этого раствора по стандартному
раствору Н2С2О4 и титр.
10. Приготовьте 50 мл 0,025N раствора NaOH разбавлением 0,1 N раствора
NaOH . Рассчитайте массовую долю полученного раствора, считая его
1,04г/мл. Определите точную концентрацию этого раствора по стандартному
раствору Н2С2О4 и титр.
11. Приготовьте 25 мл 0,05N раствора NaOH разбавлением 0,1 N раствора
NaOH . Рассчитайте массовую долю полученного раствора, считая его
1,02г/мл. Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
12. Приготовьте 65 г 0,8,% раствора NaOH разбавлением 3,85% раствора NaOH
. Рассчитайте нормальную концентрацию полученного раствора, считая его 
1,07г/мл. Определите точную концентрацию этого раствора по стандартному
раствору Н2С2О4 и титр.
13. Приготовьте 45 г 0,75% раствора NaOH разбавлением 1,55% раствора
NaOH . Рассчитайте молярную концентрацию полученного раствора, считая 
1,06г/мл.
Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
14. Приготовьте 25 мл 0,015 М раствора NaOH разбавлением 0,1 М раствора
NaOH. Рассчитайте массовую долю полученного раствора, считая его

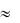 1,02г/мл. Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
1,02г/мл. Определите точную концентрацию этого раствора по стандартному раствору Н2С2О4 и титр.
15. Приготовьте 25 мл 0,025N раствора NaOH разбавлением 0,05 N раствора
NaOH . Рассчитайте массовую долю полученного раствора, считая его
49
