
3 курс / Общая хирургия и оперативная хирургия / Хирургия_тетрады_Фалло_Константинов_Б_А_,_Черепенин_Л_П_,_Иванов
.pdf
|
|
|
|
Т а б л и ц а |
19 |
|
Результаты расширяющей вальвулопластики при наличии |
|
|||||
передней комиссуры (I группа) и переднего синуса (II группа), |
|
|||||
ориентированного к передней поверхности ВОПЖ |
|
|||||
|
|
|
|
|
|
|
Показатели |
Груп |
До операции |
После операции |
|
Р |
|
па |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Возраст, лет |
|
12,2+1,4 |
|
|
|
|
|
|
21,7 ±3,4 |
|
|
|
|
|
|
|
|
|
|
|
ППТ, м2 |
|
1,14 + 0,07 |
|
|
|
|
|
|
1,5±0,14 |
|
|
|
|
|
|
|
|
|
|
|
Диаметр ФКЛА, мм |
|
14,0 + 0,67 |
16,8 + 0,58 |
|
* |
|
|
|
* |
||||
|
|
14,3±0,81 |
19,3 ±0,94 |
|
||
|
|
|
|
|
|
|
Длина ФКЛА (средняя), мм |
|
44,0 |
52,6 ( + 8,8) |
|
* |
|
|
|
45,8 |
60,1 |
(+14,8) |
|
** |
|
|
|
|
|||
|
|
|
|
|
|
|
Площадь сечения ФКЛА, мм2 |
|
307,7 |
443,1 |
|
|
|
|
|
348,5 |
|
584,8 |
|
|
|
|
|
|
|
|
|
Давление в ЛА сист., |
|
20,0+1,62 |
32,9 + 2,68 |
|
** |
|
|
|
** |
||||
мм рт. ст. |
|
15,8±3,3 |
26,7 ±3,46 |
|
||
|
|
|
||||
|
|
|
|
|
|
|
Давление Л А диаст., |
|
7,1+0,85 |
13,0+1,16 |
|
** |
|
|
|
** |
||||
мм рт. ст. |
|
4,3 ±3,2 |
8.6 ±0,95 |
|
||
|
|
|
||||
|
|
|
|
|
|
|
Перепад давления |
|
23,8 ±6,72 |
12,7 ±2,24 |
|
** |
|
|
|
|
||||
|
|
|
|
|
|
|
ПЖ-ВО-ЛА, мм рт. ст.: |
|
37,0+16,6 |
11,0 + 2,54 |
|
** |
|
|
|
** |
||||
до операции |
|
1,01+0,01 |
0,56+0,03 |
|
||
|
|
** |
||||
|
|
1,13+0,13 |
0,49 ±0,04 |
|
||
|
|
|
|
|
|
|
через 12 ч после операции |
|
- |
0,38 + 0,02 |
|
** |
|
|
|
** |
||||
|
|
|
0,36 ±0,02 |
|
||
|
|
|
|
|
|
|
Регургитация на ЛА от СВ, % |
|
- |
1,33 + 0,33 |
|
|
|
|
|
|
4,0 ±0,4 |
|
|
|
|
|
|
|
|
|
|
П р и м е ч а н и е . Р—достоверность различия показателей до и после операции.
Сравнительный анализ показал достоверные различия по воз расту и ППТ (Р<0,01) между I и II группой. Используя пред ложенные оперативные приемы, удалось увеличить диаметр фиброзного кольца у больных I группы на 8,8 мм, II группы на 14,8 мм (Р < 0,01), как показано на рис. 27.
Учитывая недостоверные отличия в показателях расширя ющей вальвулопластики с передней комиссурой (I гр.) и с пе редним синусом (II гр.), обе группы пациентов объединены и анализируются вместе. Результаты вальвулопластики (II гр.) сравнивали с пластическим расширением ВОПЖ без вмеша тельства на фиброзном каркасе корня Л А (I гр.) (табл. 20).
81

Исход |
Комиссуротомия Вальвулопластика |
Рнс. 27. |
Результаты |
|
|
клинического |
использова |
ния расширяющей вальвулопластики при передней комиссуре
Пациенты I и II групп относились к одной возрастной категории и практически не отличались по ППТ. Достоверные отличия получены при характеристике полицитемического синдрома (Р<0,05), более выраженного у пациентов I группы, что обусловлено более значительным клапанным стенозом. Дооперационная и интраоперационная морфометрическая оценка показала, что с учетом ППТ нормативный показатель Дфкла в группах одинаков и составляет 16,5 + 0,2 мм. Диаметр ФКЛА, измеренный ангиографически и интраоперационно, дос товерно был меньше во II группе. Выявлены различия и в пока зателе степени гипоплазии ФКЛА —Z (Р<0,05). Рассчитанный, по данным ангиографии, средний ПЖ/ЛЖ при выполнении операции без пересечения ФКЛА, был достоверно (Р<0,01) выше во II группе. При планировании трансаннулярного вме шательства с учетом диаметров ветвей ЛА получены одинако вые показатели ПЖ/ЛЖ.
Анализ данных до- и интраоперационного измерений Дфкла выявил изолированную, умеренную его гипоплазию на 11,5% диаметра по сравнению с нормой. После выполнения расширяющей вальвулопластики длина окружности ФКЛА увеличилась на 10,7 мм, что равносильно выполнению транс аннулярного вмешательства с аналогичной полезной шириной заплаты. С учетом ширины тканей, попадающих в шов, необ ходимо использовать заплату шириной не менее 14,7 мм, что, без сомнения, приведет к нарушению коаптации створок ЛА
ивызовет гемодинамически значимую регургитацию. В дан ном случае регургитация на КЛА была минимальной и сос тавила 2,0 + 0,2% от эффективного СВ, достоверно не отлича ясь от I группы. Также не отмечено различия после операции показателей систолического перепада давлений между ПЖВО
иЛ А и ПЖ/ЛЖ, который через 12 ч снизился ниже расчетных показателей до 0,37 + 0,02 и был одинаков в обеих группах.
82
Т а б л и ц а 20
Характеристика клинического состояния
ипоказа 1 елей центральной i емодинамики у больных
сизолированной пластикой ВОПЖ (I гр.)
ирасширяющей вальвулопластикой КЛА (II гр.)
Показатели |
1 группа (п = 61) |
11 группа (п = 31) |
[> |
|
|
|
|
|
|
Возраст, лет |
15,6±0,9 |
14,4 ±1,4 |
* |
|
|
||||
|
|
|
|
|
ППТ, м2 |
1,3 ±0,05 |
1,2 ±0,07 |
* |
|
Нв, г/л |
18,5±0,4 |
16,9 ±0,5 |
* |
|
|
||||
|
|
|
|
|
Эритроциты, млн. |
6,2 + 0,13 |
"5,5 ±0,15 |
* |
|
|
|
|
|
|
Р02 кап., мм рт. ст. |
49,6 ±2,0 |
52,1 ±2,7 |
|
|
|
|
|
|
|
Нв02 кап., % |
76,9 ±2,4 |
80,7 ±2,3 |
|
|
|
|
|
|
|
Дфкла, мм: |
16,5 + 0,2 |
|
|
|
норма |
16.5 + 0,3 |
** |
||
до операции |
19,5 + 0,5 |
14.6 + 0,5 |
||
|
||||
после операции |
19,5±0,5 |
18,0 ±0,5 |
|
|
|
|
|
|
|
Длина окружности ФКЛА, мм: |
61,5 |
|
* |
|
до операции |
45,8 |
|||
|
||||
после операции |
61,5 |
56,5 (+10,7) |
|
|
|
|
|
|
|
Степень гипоплазии ФКЛА |
12,7 ±0,39 |
-1,7 ±0,45' |
* |
|
|
||||
|
|
|
|
|
Расчетная ширина заплаты на |
- |
9,23 ±1,07 |
|
|
ПЖ/ЛЖ (ед.) ФКЛА |
|
|
|
|
|
|
|
|
|
без пересечения |
0,46 + 0,01 |
0,53 + 0,03 |
** |
|
|
||||
ФКЛА —расчетный с пере |
0,41 ±0,01 |
0,41 ±0,01 |
|
|
сечением |
|
|
|
|
ФК Л А — расчетный после |
0,48 ±0,02 |
0,54 ±0,03 |
|
|
операции |
|
|
|
|
через 12 ч |
0,37 ±0,02 |
0,37 ±0.02 |
|
|
|
|
|
|
|
Перепад давления ПЖ/ЛА, |
|
|
|
|
мм рт. ст.: |
|
|
|
|
до операции |
20,2 + 5,3 |
26,6 + 6,3 |
|
|
после операции |
10,1 ±1,3 |
12,3 ±1,7 |
|
|
|
|
|
|
|
Длина заплаты на ВОПЖ, мм |
45,8 ±1,5 |
54,0 ±1,9 |
** |
|
|
||||
|
|
|
|
П р и м е ч а н и е . Р—достоверность различия между 1 и 11 гр.
Таким образом, разработанные типы расширяющей вальвулопластики позволяют адекватно реконструировать ВОПЖ, избежав резидуального стенозирования и выраженной регургитации на клапанах ЛА, воздержаться от необоснованного использования трансаннулярной пластики у 13,4% больных.
По нашему мнению, эти операции могут дать хороший гемодинамическйй эффект только при умеренных изменениях
S3
к-

клапанного аппарата, когда после выполнения вальвулопластики получена удовлетворительная подвижность створок, со хранен достаточной длины их свободный край и достигнуто адекватное смыкание.
Большую проблему составляют пациенты, у которых соче тается умеренная гипоплазия ФКЛА и арочного кольца при переднерасположенном синусе.
Мы продолжили экспериментальные разработки в этом направлении, и как промежуточный этап между расширяющи ми вальвулопластиками и использованием моностворчатых трансплантатов, предлагаем вариант двухзаплатной техники.
Для этой цели выполнены эксперименты на изолированных выходных отделах ПЖ и ствола Л А свиней. Из ксеноперикарда были изготовлены комбинированные заплаты треуголь ной и прямоугольной формы различных типоразмеров. На заплату из более плотного бычьего ксеноперикарда фик сировали треугольник из тонкого телячьего ксеноперикарда (рис. 28). Продольным разрезом вскрывали ВОПЖ с пересече нием ФКЛА посередине переднего синуса, разрез продолжали до середины высоты передней створки и через синус до его вершины с пересечением арочного кольца. Фиксацию заплаты начинали с внутренней поверхности вшиванием фрагмента треугольной формы в разрез створки, а ВОПЖ и арочное кольцо расширяли за счет наружной заплаты.
Таким образом, используя комбинированную заплату, воз можно адекватно расширить не только фиброзное кольцо, но и арочное, увеличив при этом площадь передней створки.
Рис. 28. Схема расши ряющей вальвулопластики с использованием ком бинированной заплаты (тип 1): 1—вид заплаты, 2—гидравлическое сече ние в месте имплантации заплаты
84
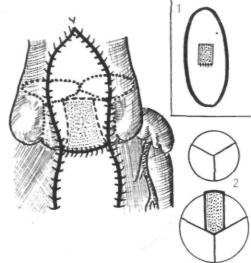
Рис. 29. Схема расширя ющей вальвулопластики с использованием комби нированной заплаты (тип 2): 1 —вид заплаты, 2—ги дравлическое сечение в месте .имплантации за платы
Неизменной остается длина свободного края передней створ ки, что может приводить к неполной коаптации ее с другими створками в связи с увеличением общего диаметра СЛА. Это осложнение можно избежать, используя комбинированные за платы прямоугольной формы (рис. 29). Имплантация их от личается от предыдущего метода тем, что производится пол ное пересечение передней створки. Прямоугольная внутренняя заплата фиксируется по краям к рассеченной створке, подкра ивая ее свободный край по высоте передней створки, а наруж ная заплата помещается на ВОПЖ и СЛА. Варьируя шириной внутренней заплаты можно адекватно расширить не только ВОПЖ и СЛА, но и свободный край передней створки, увели чивая соответственно и ее площадь. Приведенные оперативные приемы выполнены только в эксперименте.
4.2. Ксеноперикард.
Разработка и создание на его основе моностворчатых ксеноперикардиальных трансплантатов (МКТ)
Основной принцип, заложенный в конструкцию моноствор чатых трансплантатов, — возможность адекватного расшире ния гипоплазированного конуса ПЖ и СЛА в сочетании с вос становлением замыкательной функции клапана Л А.
Применение запирательных элементов в позиции КЛА на чато с 1967 г., когда впервые был использован гомотрансплан-
85

тат аорты [209]. В настоящее время ряд зарубежных фирм выпускаю! коммерческие образцы таких трансплантатов (Polistan-Benelux, Lonescu-Shiley), а в некоторых клиниках (Техасский институт сердца, США; Токийский институт сердца, Япония; Институт сердечно-сосудистой хирургии им. А. Н. Бакулева, г. Москва; НИИ грудной хирургии, г. Киев и др.) имеется опыт создания собственных моностворок. Для их изготовления используются как синтетические (дактрон, тефлон, гортекс), так и биологические материалы (аутоперикард, ксеноперикард). Наиболее часто используются компо зитные трансплантаты, когда наружная поверхность представ лена синтетическим материалом или дупликатурой тефлона с ксеноперикардом, а запирающий элемент изготовлен на опе рационном столе из аутоперикарда или заранее из ксеноматериала. Цельные ксеноперикардиальные моностворки изготав ливает фирма «Lonescu-Shiley». Промышленные образцы выпускаются 6-7 типоразмеров. При этом расстояние между комиссурами запирающего элемента варьирует от 15 до 40 мм и глубина запирающего элемента —от 4 до 14 мм.
Различие в конструктивной особенности применения МКТ сводится к использованию створок треугольной формы или в виде естественных створок, повторяющих форму эллипсоида вращения (рис. 30, 31). С гидродинамической точки зрения использование последних наиболее выгодно, так как сохраня ются условия гладкого смыва и образования устойчивых вих рей Хилла, исключающих избыточное отложение фибрина, которое может возникнуть при использовании створок тре угольной конструкции. Применение композитных материалов с различными механическими свойствами вызовет неоднород ное распределение нагрузок, что может отразиться на функции трансплантата в отдаленном послеоперационном периоде, тем более, что дополнительное укрепление выходного отдела ПЖ
Рис. 30. Типы конструкции МКТ. Стрелками показаны вихревые потоки в диастолическую фазу
86

Рис. 31. Приспособление для моделирования запирающего элемента МКТ (в разобранном виде)
синтетической заплатой не избавляет от образования ложных аневризм. Спонтанная же коллагеновая дегенерация наружных заплат ксеноматериала связана в основном с технологией его обработки.
Для создания оптимального типа моностворчатого транс плантата необходимо: 1) разработать и оценить биологиче ский материал для создания МКТ и провести сравнительные исследования его механических свойств со структурами проте зируемых элементов ЛА; 2) создать конструкцию МКТ, от вечающую основным принципам оптимальных гидродинами ческих условий (минимальный перепад давления и отсутствие выраженной регургитации).
Материал для создания новых типов трансплантатов дол жен отвечать ряду требований: 1. Обладать прочностными и деформативными характеристиками, показатели которых не отличаются от свойств клапана и ствола ЛА. 2. Иметь гладкое внутреннее покрытие с минимальными адгезивными свойствами. 3. Обладать нулевой хирургической порозностью, делающей его пригодным при операциях с управляемой гемо филией. 4. Не вызывать реакции организма на имплантацию. 5. Сохранять стерильность при хранении. 6. Хорошо модели роваться в месте имплантации.
Этим требованиям отвечает ксеноперикард крупного рога того скота, широко используемый в кардиохирургии как плас тический материал и для создания протезов клапанов сердца.
87
V -
Мы применили ксеноперикард телят и быков, полученный в первые 6 ч после забоя животных. Проводилась механичес кая очистка с удалением покрывающей перикард клетчатки
иутолщенных фрагментов в местах фиксации к диафрагме
ипереходных складок. Затем выполнялась двенадцатичасовая промывка в проточной воде для экстракции водорастворимых белков.
Для снижения антигенности биоматериала нами модифи цирована ферментно-химическая обработка ксеноаортальных комплексов при производстве биопротезов БАКС. При ис пользовании раствора террилитина на фосфатном буфере рН-7,8 в концентрации 10 ед. на 1 г вещества в течение 30 мин при t= +43° С разрушаются клеточные элементы. В подобран ной концентрации фермент не обладает коллагено- и эластоли тической активностью. После нейтрализации фермента рас твором ПИКЕЛЬ (лимонная кислота + хлорид натрия) в течение 20 мин, ПИКЕЛЬ нейтрализуют 0,1%-м раствором соды в течение 20 мин. Продукты гидролиза удаляют в проточ ной воде в течение 1 ч с последующей солевой экстракцией 2%-м раствором хлорида натрия в течение 12 ч и 7%-м — в течение 5 ч. Соли удаляют проточным промыванием в тече ние 2 ч. Обработанный перикард помещают на специальные приспособления в ненапряженном состоянии для придания соответствующей формы и проводят структурную стабилиза цию в слабых растворах глютарового альдегида на фосфатном буфере со следующей сменой растворов: двукратной в течение 3 сут. и четырехкратной 0,5%-м раствором —7 сут. При этом достигается равномерная проработка ткани ксеноперикарда альдегидом и прекращается его поглощение. Затем материал снимается с приспособления, сохраняя приданную форму. Сле дующий этап —сборка МКТ. Из полученного материала вы краивали запирающий элемент и фиксировали на плоскостную заплату из бычьего ксеноперикарда непрерывным обвивным швом нитью Etibond-5,0. В области вершины комиссур накла дывали П-образный шов через всю толщину материала с завя зыванием снаружи и соединяли их непрерывным обвивным швом, проведенным через толщу заплаты. При фиксации створки следили за тем, чтобы не происходила ее деформация и створка фиксировалась в открытом состоянии. После завер шения фиксации стерилизовали в 0,5%-м растворе глутарового альдегида в течение 10 суток при t= +25° С в герметичных контейнерах, приготовляемых для клинического использова ния (рис. 32, 33).
Гистологическое изучение нативного материала (окраска гематоксилин-эозином и по Ван-Гизону) показало, что телячий перикард —это соединительно-тканное образование из двух
88

Рис. 32. Приспособление для моделирования МКТ (в собранном виде)
Рис. 33. Типоразмеры МКТ (общий вид)
слоев (по расположению коллагеновых волокон). Внутрен ний слой представлен плотно упакованными коллагеновыми
89

волокнами извитого характера. Во втором слое толстые пучки коллагеновых волокон рыхлые, между ними имеются много численные тонкие эластиновые волокна. Сосудистые элементы немногочисленны. Клетки расположены во всех слоях равно мерно. Слой мезотелия разрушается при предварительной ме ханической обработке (рис. 34).
Рис. 34. Нативный ксеноперикард (окраска гематоксилин-юзином. ув.х250)
После ферментной обработки клетки сохранялись только по ходу кровеносных сосудов в небольшом количестве. В тол ще ткани сохранялось около 10% клеток (в сравнении с нативным материалом), при почти неизмененных коллагеновых и эластиновых волокнах (рис. 35).
Предложенный метод обработки с использованием фер мента позволяет практически полностью разрушить и удалить клеточные элементы и гликозаминогликаны межклеточного вещества как основных носителей антигенности. Волокнистые белки — коллаген и эластин сохраняют структуру, а структур ная стабилизация глютаровым альдегидом превращает, благо даря образованию поперечных связей, биологическую ткань в биополимер.
Механические испытания проводили в условиях одноос ного растяжения на плоских образцах, вырезанных в форме лопатки специальным штампом. Размеры рабочего участка:
90
