
- •Обмен веществ и энергии. Терморегуляция.
- •Обмен веществ включает три этапа:
- •Внутриклеточный метаболизм (промежуточный обмен)
- •Интенсивность метаболизма зависит от :
- •Баланс энергии
- •В соответствии с первым законом термодинамики энергия не может возникать из ничего и
- •Вся энергия, высвобождаемая во время обменных процессов, в конечном счете превращается в тепло,
- •Стандартная единица энергии
- •Измерение энергии включает:
- •Физическая калориметрия
- •Калориметр («бомба») Бертло
- •Физиологическая калориметрия
- •Прямая калориметрия
- •Калориметр Лавуазье
- •Биокалориметр Этуотера-Бенедикта
- •Непрямая калориметрия
- •Полный газовый анализ
- •Для методов полного газового анализа может быть достаточно
- •ДК сильно зависит от выполняемой физической работы
- •Неполный газовый анализ
- •Определение легочной вентиляции с помощью мешка Дугласа
- •Различают два уровня энерготрат:
- •ОСНОВНОЙ ОБМЕН
- •При измерении величины основного обмена у человека соблюдают следующие условия:
- •На величину основного обмена влияют:
- •3. Специфически-динамическое действие пищи.
- •На величину основного обмена влияют гормоны щитовидной железы трийодтиронин и тироксин.
- •РАБОЧИЙ ОБМЕН
- •В организме основной потребитель энергии - это мышцы:
- •ГРУППЫ РАБОТНИКОВ ПО ЭНЕРГОТРАТАМ
- •ТЕМПЕРАТУРНЫЙ
- •Температура тела
- •Втеле
- •В жаркой среде и/или при высоком уровне двигательной активности границы «ядра» расширяются. В
- •Эволюция разместила в периферических частях тела клетки и ткани, способные выполнять свои функции
- •Постоянство температуры тела
- •Температуру ядра тела измеряют разными способами:
- •Наиболее распространенный в клинической практике показатель теплового состояния — температура подмышечной области (аксиллярная
- •ТЕРМОРЕЦЕПТОРЫ
- •Центральные механизмы терморегуляции
- •Еще в 1860-х гг. немецкий врач К. Либермейстер высказал гипотезу, согласно которой центры
- •Установочная точка гипоталамического термостата меняется в зависимости от:
- •Теплопродукция
- •Теплопродукция бывает:
- •Теплоотдача
- •Теплоотдача бывает
- •ТЕРМОРЕГУЛЯЦИЯ
- •Механизмы физической и химической терморегуляции
- •Механизм, понижающий температуру тела
- •Перераспределение части кровотока из ядра тела в его оболочку для увеличения теплоотдачи
- •Механизмы, повышающие температуру тела
- •Механизм теплоотдачи на холоде (А) и в тепле (Б)
- •Гуморальная терморегуляция
- •РАССТРОЙСТВА
- •Из расстройств питания наибольшее социальное и клиническое значение имеет ожирение, поскольку оно сочетается
- •Индекс массы тела
- •Классификация ожирения
- •Типы ожирения
- •Механизмы развития ожирения и факторы, способствующие ожирению:
- •Адипоциты
- •Потребление пищи и окисление пищевых субстратов
- •Возможные причины инсулинорезистентности при ожирении:
- •БУЛИМИЯ
- •НЕРВНАЯ АНОРЕКСИЯ
- •НАРУШЕНИЯ
- •Воздействие различных агентов может привести к изменению теплового баланса организма.
- •Гипертермические состояния
- •Лихорадка
- •Гипотермические состояния
- •Управляемая (искусственная) гипотермия
- •Локальная управляемая гипотермия отдельных органов или тканей (головного мозга, почек, желудка, печени, предстательной

Обмен веществ и энергии. Терморегуляция.

Обмен веществ включает три этапа:
1.поступление веществ в организм (дыхание и питание),
2.метаболизм,
3.выделение конечных продуктов из организма.

Внутриклеточный метаболизм (промежуточный обмен)
включает два типа реакций: катаболизм и анаболизм.
Катаболизм — процесс расщепления органических молекул до конечных продуктов. Конечные продукты превращений органических веществ - СО2, Н2О и мочевина. Реакции катаболизма сопровождаются выделением энергии.
Анаболизм - биосинтетические процессы. В анаболических реакциях используется энергия, освобождающаяся при катаболизме.

Интенсивность метаболизма зависит от :
1.мышечной работы (+)
2.недавнего употребления пищи (+),
3.температуры окружающей среды,
4.роста, массы и площади поверхности тела,
5.пола (у мужчин +),
6.эмоционального состояния (или +),
7.возраста (- после 30 лет жизни),
8.температуры тела (прямо пропорционально +),
9.йодсодержащих гормонов щитовидной железы (+) и адреналина (+).

Баланс энергии
В организме насчитывается пять форм энергии:
1.химическая,
2.механическая,
3.осмотическая,
4.электрическая,
5.тепловая.
Клетки способны использовать только химическую энергию. Химическая энергия в организме может превращаться во все другие формы энергии.

В соответствии с первым законом термодинамики энергия не может возникать из ничего и исчезать бесследно
Уравнение энергетического баланса:
Е = А + Н + S,
где Е — общее количество энергии, получаемой организмом с пищей;
А — внешняя (полезная) работа; Н — теплоотдача;
S — запасенная энергия.
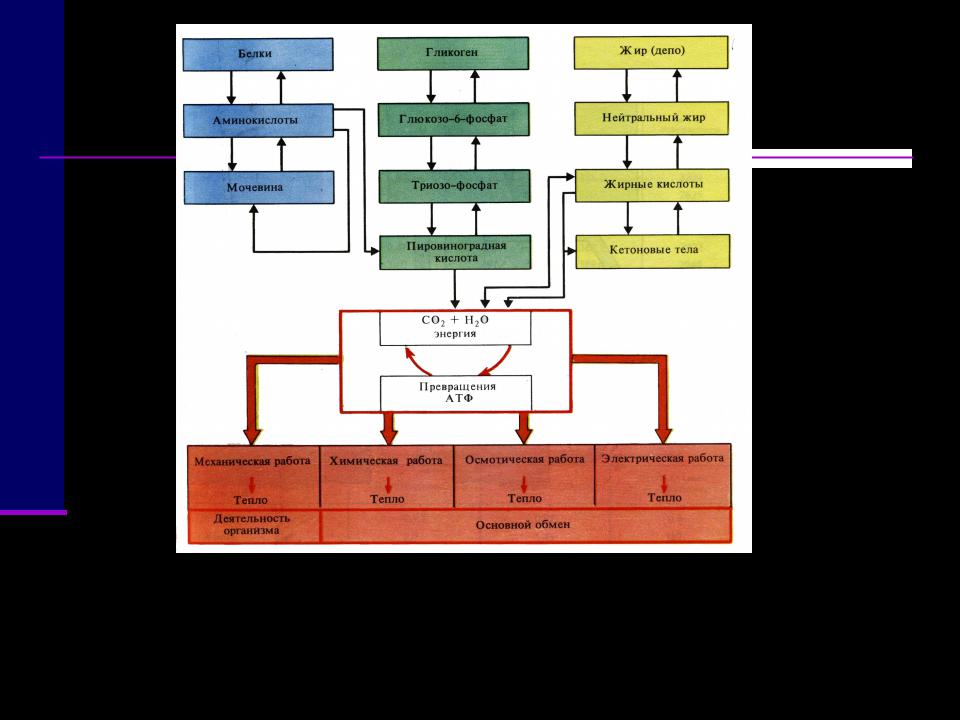
Вся энергия, высвобождаемая во время обменных процессов, в конечном счете превращается в тепло, если не происходит внешней работы или накопления химической энергии.

Стандартная единица энергии
1.в международной системе единиц (СИ) — джоуль (Дж)
2.не входящая в СИ единица тепловой энергии — калория (кал).
Калорию определяют как количество тепла, необходимое для нагрева 1 г воды на 1 градус Цельсия (1 калория = 4,187 Дж).

Измерение энергии включает:
1.Физическую калориметрию
2.Физиологическую
калориметрию

Физическая калориметрия
позволяет определить энергетическую ценность вещества или калорический коэффициент вещества.
Калорический коэффициент - количество тепла, образуемого при сгорании 1 г вещества в атмосфере чистого кислорода:
ЖИРЫ - 9,3 ккал; БЕЛКИ – 5,3 ккал, УГЛЕВОДЫ - 4,1 ккал
