
- •5.3.4. Естественное течение
- •5.3.5. Кардиальные проявления синдрома Марфана (клиника, диагностика и хирургическое лечение)
- •5.3.5.2. Аневризма восходящей аорты
- •5.3.6. Общие вопросы хирургии аневризм восходящей аорты
- •5.3.6.1. Открытая техника формирования дистального анастомоза
- •5.3.7. Частные вопросы хирургии аневризм восходящей аорты
- •5.3.7.1. Имплантация клапансодержащего кондуита
- •5.3.7.2. Клапансохраняющие операции
- •5.3.7.3. Протезирование дуги аорты
- •5.3.8. Осложнения
- •5.3.9. Результаты операций
- •5.3.10. Синдром Марфана у детей
- •5.3.11. Особенности кардиологического мониторинга у пациентов с синдромом Марфана
- •5.4. Врожденные деформации дуги аорты
- •5.5. Коарктация аорты
- •5.6. Открытый артериальный проток
- •5.7. Аневризмы грудного отдела аорты
- •5.7.1. Аневризмы грудной аорты
- •5.7.2. Отдельные нозологические формы, вызывающие развитие аневризм грудной аорты
5.3.5.2. Аневризма восходящей аорты
Симптомы и признаки. Большинство аневризм восходящей аорты выявляются случайно во время рентгенографии грудной клетки или при использовании других методов визуализации, применяемых для диагностики различных заболеваний. Около 25—30 % пациентов жалуются на боль в грудной клетке, которая обычно локализуется пре-кардиально с иррадиацией в шею и нижнюю челюсть при вовлечении в патологический процесс дуги аорты. В то же время 75 % пациентов с острым расслоением аорты отмечают сильную боль, локализующуюся обычно в спине. Иногда определяется синдром верхней полой вены, сопровождающийся одышкой и непродуктивным кашлем. Охриплость голоса свидетельствует о поражении дуги и/или проксимальных отделов нисходящей аорты.
Физикальное исследование. Число физикальных признаков заболевания не столь велико. Аневризмы больших размеров порождают эктопическую пульсацию, пальпируемую на передней стенке грудной клетки, вызывают узурацию ребер, выбухание грудной клетки и кожи. При наличии аортальной регургитации определяются высокое пульсовое давление, дефицит пульса, а также диастолический шум, выслушиваемый обычно парастернально.
Инструментальные методы диагностики. Распознавание аневризмы восходящего отдела аорты не представляется трудной задачей и может быть достигнуто уже при использовании обычных диагностических методов. В то же время определенные, а иногда значительные трудности возникают при диагностике расслоения аортальной стенки и его протяженности.
Электрокардиография. Электрокардиограмма может оставаться нормальной. При наличии аорталь-
557

ной регургитации определяются признаки левожелудочковой гипертрофии и перегрузки. Признаки ишемии миокарда могут наблюдаться у пациентов с расслаивающей аневризмой вследствие перекрытия отслоившейся интимой устьев коронарных артерий.
Рентгенография органов грудной клетки. Как отмечено выше, многие бессимптомные аневризмы удается выявить во время рентгенографии. Расширение средостения в сочетании с дислокацией трахеи и пищевода на рентгенограмме в прямой проекции может свидетельствовать о наличии аневризмы. Аневризмы восходящего отдела аорты могут давать выпуклый контур в правом верхнем средостении (рис. 5.17). Тень грудины часто затеняет расширенную аорту в переднезадней проекции. В боковой проекции нередко определяется уменьшение ретростернального воздушного пространства. В тени артериальной стенки могут определяться глыбки кальция. Аневризмы, ограниченные корнем аорты и
синусами Вальсальвы, иногда затеняются сердцем.
Эхокардиография (ЭхоКГ) — чрезвычайно важный метод диагностики аневризм восходящей аорты и контроля над ними. Дилатация корня аорты или аневризма восходящей аорты с клапанной регурги-тацией могут быть впервые обнаружены во время эхокардиографиче-ского исследования. При подозрении на острое расслоение при трансторакальной ЭхоКГ могут определяться признаки гемопери-карда.
Несмотря на простоту и доступность перечисленных выше методов, полученная с их помощью информация остается ограниченной. При трансторакальной ЭхоКГ не удается оценить состояние дуги аорты и ее ветвей, а при рентгенографии невозможно получить представление о морфологии и замыка-тельной функции аортального клапана. Оба метода малоинформативны при расслоении аортальной стенки, но оказываются ценными в качестве первых диагностических
558

процедур, позволяющих врачу заподозрить патологию аорты и рекомендовать пациенту дальнейшее обследование в специализированном отделении.
Чреспищеводная ЭхоКГ является быстрым и точным методом визуализации, позволяющим получить более подробную информацию о состоянии восходящей аорты и в более высоком проценте наблюдений (до 90 %) распознать расслоение аортальной стенки (рис. 5.18), тромботические массы в ложном просвете аорты или интрамураль-ной гематомы, а также более детально оценить морфологию аортального клапана, что может оказаться ценным при выборе метода хирургической коррекции, в частности определении возможности проведения клапансберегающих операций.
Четкая визуализация дистальных отделов восходящей аорты и дуги при чреспищеводной ЭхоКГ затруднена воздушным столбом трахеи и главных бронхов. Это обстоятельство не позволяет четко визуализировать дистальные сегменты во время чреспищеводной ЭхоКГ приблизительно в 40 % наблюдений.
Аортография. Золотым стандартом при диагностике аневризмы восходящей аорты в течение длительного времени считали аортогра-фию, которую и сегодня широко используют в клинической практике. Этот метод, доступный только в специализированных клиниках, дает возможность оценить диаметр аорты на уровне аневризматическо-го расширения, протяженность патологически измененного участка аорты, степень аортальной регурги-тации (рис. 5.19) и у части больных с большей или меньшей степенью достоверности — выявить наличие и распространенность расслоения аортальной стенки. При аортогра-фии также хорошо определяются расположение аневризмы по отношению к сосудам дуги аорты, выраженность дилатации синусов Валь-сальвы и смещение устьев коронарных артерий.
Ограничениями данного метода являются его относительная труд-нодоступность, инвазивность и недостаточная информативность при расслоении.
Коронарография обычно входит в стандартный план предоперацион-
559
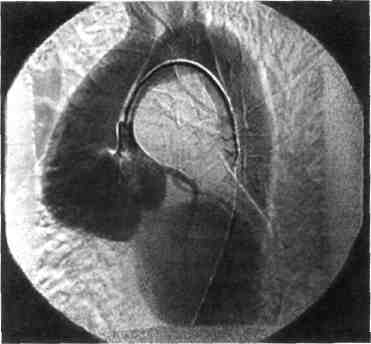
Рис. 5.19. Аортография: аортальная ре-гургитация.
фии. При подозрении на острое расслоение аортальной стенки независимо от возраста пациента ко-ронарография должна производиться лишь в исключительных случаях. Компьютерная томография (КТ) с внутривенным введением контрастных веществ (компьютерная томографическая ангиография) дает возможность довольно точно оценить характер и размеры аневризм аорты. КТ дополняет данные, полученные при аортографии, особенно в случае внутрисосудистого тромбоза и расслоения (рис. 5.20, а—в). При этом наблюдается экстраваза-ция контраста с вовлечением в процесс рядом расположенных структур. КТ может быть полезной для

Рис. 5.20. Компьютерная томограмма: расслоение аортальной стенки (а—в).

560

динамической оценки небольших бессимптомных аневризм и количественных изменений размеров и скорости дилатации, однако усреднение объемов в зонах с быстроменяющейся кривизной наряду с томографическими «срезами» в плоскостях, неперпендикулярных продольной оси аорты, может привести к неверной оценке диаметра аорты.
Польза трехмерной техники визуализации в рамках КТ не установлена. Теоретически трехмерное сканирование дает больше информации о протяженности аневризм, особенно для аневризм нисходящей аорты. Использование указанной методики дает возможность прецизионной визуализации и количественной оценки мешковидных образований.
Наиболее современным из методов КТ в диагностике аневризм восходящей аорты является электронно-лучевая томография. Благодаря современным технологиям формирования изображения и его обработки метод при меньшей дозе рентгеновского излучения обеспечивает получение достоверных данных о состоянии аортальной стен-

ки, форме и протяжености аневризмы. Электронно-лучевая томография позволяет моделировать трехмерное изображение аорты, наиболее точно отражающее ее реальное состояние (рис. 5.21, а—в).
Магнитно-резонансная томография (МРТ) дает информацию, подобную по своей сути той, которую получают при КТ, однако обладает рядом преимуществ, главными из которых представляется отсутствие необходимости введения рентгено-контрастных препаратов и использования ионизирующей радиации. Стенки сердца и сосудов имеют до-
561

Рис. 5.22. MPT: сагиттальный срез.
статочное количество натуральных контрастов. Во время МРТ могут быть получены четкие срезы в различных плоскостях (рис. 5.22; 5.23). Современные технологии позволяют оценить направление и скорость кровотока не только в аорте, но и в коронарных артериях. Теоретически МРТ можно использовать не только для визуализации и оценки кровотока в коронарных артериях и аорте, но и для получения информации о клапанах и функции сердца. МРТ в настоящее время менее распространена, чем КТ, так как является более дорогостоящей и нередко недоступна для пациентов.
Хирургическое лечение аневризмы восходящей аорты. Хирургическое лечение аневризмы восходящей аорты по-прежнему остается сложной, но при современном уровне развития кардиохирургии решаемой задачей. История хирургии аневризмы восходящей аорты исчисляется десятилетиями и тесно связана с начальным периодом становления хирургии открытого сердца в целом.
Первые записи об артериальных аневризмах принадлежат Галену (II в.). Aetius в VI в. описал разрыв
562
аорты во время родов. Везалию по праву принадлежит клиническое первенство в диагностике мешковидной аневризмы грудного отдела аорты, о которой он сообщил в 1557 г. В 1757 г. William Hunter представил клиническое наблюдение аневризмы грудной аорты, определяющейся через стенку грудной клетки. Кроме того, им подробно были описаны симптомы компрессии грудной клетки и ее органов, а также четкие дифференциальные критерии, позволяющие отличить аневризму от псевдоаневризмы.
Несмотря на многовековую историю, хирургическое лечение аневризм аорты было предпринято лишь в XX столетии и в «доперфу-зионный» период ограничивалось укреплением аорты путем ее оборачивания (окутывания) теми или иными материалами, а в случае ограниченных мешковидных аневризм — латеральной резекцией с последующим восстановлением целости аортальной стенки.

Рис. 5.23. МРТ: фронтальный срез при расслоении аневризмы I типа.
Первые резекции аневризмы восходящей аорты с замещением аортальным аллографтом осуществили D.Cooley и M.DeBakey. Результаты этих операций были опубликованы в 1956 г. Протезирование супрако-
ронарного сегмента восходящей аорты в сочетании с восстановлением несостоятельности аортального клапана описано W.Mueller и со-авт. в 1960 г. Комбинированное протезирование супракоронарного отдела аорты синтетическим сосудистым протезом и аортального клапана механическим протезом выполнено A.Starr и соавт. в 1963 г. Протезирование восходящей аорты в целом, за исключением небольшого сегмента, содержащего коронарные артерии и аортальный клапан, с изолированным протезированием последнего осуществили M.Wheat и соавт. в 1964 г. В том же году L. Groves и соавт. высказали идею о необходимости реимпланта-ции устьев коронарных артерий в сосудистый протез аорты.
В 1968 г. H.Bentall и A.DeBono впервые сообщили об использовании «кондуита», состоящего из тефлонового сосудистого протеза и вшитого в него шарового протеза Старра-Эдвардса для одномоментного протезирования восходящей аорты и аортального клапана. В 1970 г. W.Edwards и A.Kerr использовали подобную методику для коррекции расслоения восходящей аорты, сопровождающегося аортальной регургитацией. Авторами использовалась техника окутывания, которая подразумевала погружение и окутывание (оборачивание) сосудистого протеза тканью пораженной патологическим процессом стенки аорты с последующим ушиванием ее над протезом с целью профилактики послеоперационного кровотечения.
Последующие работы были посвящены модификации методик выделения устьев коронарных артерий и имплантации их в стенку протеза, а также профилактике сдавливания стенкой аорты сосудистого протеза. Указанные исследования проводили с целью уменьшить вероятность формирования псевдоаневризм, которые нередко
наблюдались при использовании техники окутывания. В 1981 г. C.Cabrol и соавт. предложили методику полного замещения восходящей аорты с реимплантацией коронарных артерий при помощи дополнительного 8—10-миллиметрового дакронового протеза.
Как уже было указано, первыми заменителями резецируемых сег ментов аорты были аортальные ал- лографты. Заготовку аллографтов производили путем забора в усло виях стерильности фрагмента аорты у недавно погибших людей с после дующей экспозицией их в стериль ном, обогащенном антибиотиками солевом растворе, содержащем сы воротку. Проблемы, связанные с совместимостью, сохранением,
структурными изменениями и отдаленной функцией этих протезов в конечном итоге привели к экспериментальным работам по созданию синтетических протезов, имеющих в своем составе стекло, золото, ме-тилметакрилат и полиэтиленовые пластмассы. Первое протезирование аорты тканевым протезом Viny-on N предприняли A.Blakemore и A.Voorhees в 1954 г. В дальнейшем наиболее широкое распространение получил синтетический материал дакрон. В настоящее время импрег-нированные коллагеном или желатином дакроновые протезы, характеризующиеся высокой резистентностью к проницаемости элементов крови, являются, пожалуй, наиболее распространенными заменителями пораженной аорты.
Альтернативой им в последние годы становятся ксеноперикардиа-льные кондуиты (так называемые биокондуиты), впервые предложенные группой авторов из Бразилии.
В России первую успешную резекцию мешковидной аневризмы восходящей аорты с наложением краевого шва аорты в условиях искусственного кровообращения выполнил 28 декабря 1962 г. А.В.Покровский. Первые успешные опера-
563
ции супракоронарнои резекции аневризмы восходящей аорты с раздельным протезированием аорты и аортального клапана, а также вмешательства по методикам Бентал-ло—Де Боно и Каброля при СМ выполнил Г.И.Цукерман соответственно в 1973, 1978 и 1983 гг. Био-кандуит впервые в России использовал А.И.Малашенков в декабре 1989 г.
Показания к операции. Клинические и диагностические симптомы. Наличие симптомов аневризмы восходящей аорты и выраженной или клинически значимой аортальной регургитации является прямым показанием к хирургическому лечению этой патологии. При подозрении на острое расслоение аорты и тем более при верифицированном диагнозе требуется срочное, а при надрыве или разрыве аорты — экстренное оперативное вмешательство.
Прогрессирующее расширение аорты. Аневризмы с прогрессирующим течением, т.е. постепенным увеличением диаметра аорты, что устанавливается в результате динамического наблюдения за пациентом по данным серии рентгенограмм, эхокардиограмм, компьютерных и/или магнитно-резонансных томограмм, требуют хирургической коррекции. Резкое увеличение размеров нередко предшествует разрыву аорты. В настоящее время считается, что скорость расширения аневризмы, превышающая 1 см в год, — прямое показание к операции.
Размер аневризмы. Бессимптомные аневризмы более 5,5—6 см в диаметре в сочетании с аортальной регургитацией или без нее следует подвергать хирургической коррекции, поскольку риск разрыва аневризмы при прогрессировании ее размера увеличивается, тогда как летальность и частота осложнений после хирургических вмешательств невысоки. Как показывают резуль-
таты ретроспективных исследований по оценке естественного течения неоперированных грудных аневризм, средний диаметр разорвавшихся аневризм составил 6— 10 см.
Ряд авторов считают, что пациентов с СМ необходимо оперировать во всех случаях, когда диаметр аорты превышает 5,5—6 см. Пациентов, в семейном анамнезе которых отмечены расслоение аорты или случаи внезапной гибели родственников, рекомендуется оперировать при достижении аортой диаметра 5—5,5 см. Другие авторы показанием к операции считают прогрессивное увеличение диаметра аорты или удвоение диаметра в сравнении с исходным. Пациентам с тяжелой аортальной регургитацией или симптомами расслоения аорты необходимо проводить коррекцию аневризмы и пластику либо протезирование аортального клапана.
Сочетание патологии аортального клапана с расширением восходящей аорты. Недостаточность аортального клапана при СМ является признаком нарушения коаптации его створок. Клинические симптомы и/или прогрессирование регургитации часто делают необходимой операцию до того, как диаметр аорты достигнет значительного размера (5—6 см). P.Michael отмечает, что у 25 % пациентов с аортальной регургитацией, диаметр аорты у которых превышает 4 см, в дальнейшем требуются повторные операции с целью протезирования аорты. Частота расслоения аорты после протезирования аортального клапана довольно высока и составляет около 27 % среди пациентов с диаметром аорты более 5 см. Описанные исследования свидетельствуют о необходимости протезирования восходящей аорты во время операций по коррекции клапанных нарушений в том случае, когда диаметр аорты превышает 4—5 см.
564
Аневризмы синусов Вальсалъвы могут развиваться после протезирования восходящей аорты у пациентов с СМ или кистозным медионекро-зом. Коррекция этой патологии показана при прогрессирующей дила-тации аорты на уровне синусов Ва-льсальвы, надрыве интимы либо превышении диаметра аорты более 6 см.
Виды операций при аневризме восходящей аорты. Из всего многообразия операций, предложенных для хирургического лечения аневризм восходящей аорты, лишь немногие могут быть с успехом использованы при СМ. Это обусловлено как характером патологических изменений в аортальной стенке и аортальном клапане, так и многолетним опытом хирургического лечения восходящей аорты. На сегодняшний день методом выбора при необходимости хирургической коррекции патологии восходящей аорты и аортального клапана при СМ является имплантация клапансо-держащего кондуита. У части больных при сохранных створках аортального клапана возможно выполнение того или иного вида клапансох-раняющей операции, предусматривающей протезирование восходящей аорты с реимплантацией устьев коронарных артерий и укреплением кольца аортального клапана.
Супракоронарное протезирование восходящей аорты — изолированное или в сочетании с раздельным протезированием аортального клапана — оказалось несостоятельным из-за неблагоприятных отдаленных результатов. У значительного числа пациентов (до 38 % при СМ) возникал рецидив аневризмы ниже проксимальной линии шва аорты и сосудистого протеза (на уровне синусов Вальсальвы), что требовало повторной операции или приводило к разрыву аневризмы. На сегодняшний день такая методика, равно как и изолированное
супракоронарное протезирование восходящей аорты без замены аортального клапана, сохранили свое значение при расслаивающей аневризме восходящей аорты атероскле-ротического генеза.
