
2 курс / Гистология / Источники_ошибок_при_морфологических_исследованиях
.pdf
Рис 7 «Пространства Грюнхагена» в ворсинках |
тонкой кишки |
|
женщины, погибшей |
от тропической малярии |
Вскрытие через |
|
2 часа после смерти |
|
Формалин, |
целлоидин, гематоксилин эозин, |
xlOO |
Рис. 8 Отслойка эпителия толстой кишки у обезьяны. убитой эфиром.
Формалин Парафин. Гематоксилин-эозин, Х130.
20
V
служит сокращение мышечных волокон стромы ворсинок, указывает, что субэпителиальные полости чаще появляются в кусочках, состоящих из всех слоев кишки, чем в одной слизистой оболочке, получаемой при аспирационной биопсии.
На нашем секционном материале (у больных, погибших не от кишечных заболеваний) пространства под эпителием, заполненные белковой жидкостью, обнаруживались в ворсинках тонкой кишки почти во всех случаях, если вскрытие делали через 1—3 часа после смерти. Позднее они встречались реже, но лишь потому, что ворсинки очень быстро лишаются своего эпителиального покрова (см. гл. V). Если же эпителий хотя бы местами уцелел, то типичные «пространства» удается найти и на довольно поздно сделанных вскрытиях (см. рис. 21), когда возможность суправитальных реакций становится весьма маловероятной. Stoerk (1916) наблюдал, что при наличии в ворсинках щелевидных пространств, заполненных жидкостью, мышечные волокна этих ворсинок оставались длинными, расслабленными, без намека на сокращение. Поэтому он полагал, что в таких случаях речь идет о простом сморщивании рыхлой соединительной ткани ворсин во время фиксации. Все же так можно объяснить лишь появление пустых щелей под эпителием, показанных, например, на рис. 8. Но тканевая жидкость сама легко свертывается и едва ли может быть выдавлена при одновременном сморщивании остова ворсин. Приходится допустить, что жидкость, содержащая белок, иногда накапливается под эпителием еще до того, как кусочки кишки попадают в фиксатор. Когда и почему это происходит — сказать трудно. Вопрос о природе «пространств Грюнхагена» пока нельзя считать вполне выясненным.
Спадение легочной ткани
Это явление, послужившее причиной многих недоразумений и ошибок, также не принадлежит к числу суправитальных реакций, хотя наиболее резко оно бывает выражено в ранние сроки после смерти человека или животного. В момент вскрытия плевральной полости с присущим ей отрицательным давлением объем легких, сохранивших свою эластичность, может уменьшиться на 7з—2/3 (Rahn, 1961). С таким осложнением можно было бы и примириться, если бы легочная ткань повсюду сжималась равномерно. Но альвеолы сильнее всего спадаются по соседству с неподатливыми образованиями — бронхами, очагами пневмонии, опухолевыми узлами. Это создает видимость участков ателектаза. Очень легко возникает ложный ателектаз, сопровождающийся мнимым утолщением межальвеолярных перегородок с «гиперплазией» септальных клеток, на местах,
21
подвергавшихся сдавливанию во время осмотра органа и иссечения из него кусочков для исследований. Предотвратить такие артефакты сравнительно легко в опытах, производимых на мелких лабораторных животных, и гораздо труднее при вскрытии трупа человека.
У животных лучше всего, перевязав трахею, целиком иссекать грудную клетку с частью позвоночника (не повредив диафрагмы!) и фиксировать ее, не вскрывая. Через несколько часов или на другой день легкие можно без опасений извлечь, осмотреть и продолжить фиксацию. Удовлетворительные результаты дает и простое перевязывание трахеи перед вскрытием плевральной полости. Тогда можно осмотреть наружную поверхность легких до воздействия фиксатора, сама фиксация происходит быстрее, но легкие все же слегка спадаются (что особенно заметно в прикорневых отделах).
Безукоризненное изучение легких человека требует фиксации их in situ путем введения за 3—10 часов до вскрытия фиксирующей жидкости в легочные сосуды через правый желудочек сердца, осторожно обнажаемый разрезом брюшной стенки и сухожильного центра диафрагмы. Н. И. Володин (1966) предложил для этой цели простой и удобный аппарат. Rahn рекомендует применять фиксатор, мало изменяющий естественную окраску тканей (раствор формалина с карлсбадской солью и хлоралгидратом).
Казалось бы, что первоначальный объем спавшихся легких можно восстановить, нагнетая в бронхи воздух или фиксатор. Но это лишь усугубит артефакты: малейшие препятствия по ходу дыхательных путей (слизь, экссудат) помешают расправлению участков ателектаза, а остальная ткань вздуется. Кроме того, возможно смывание и перемещение содержимого бронхов.
Bignon и др. (1966) рекомендуют тщательно отсасывать содержимое бронхов перед заполнением дыхательных путей фиксирующей жидкостью. Такой способ едва ли достигнет цели и лишит возможности изучать патологические изменения самих бронхов.
В прозекторской работе затруднительно использовать приемы, необходимые для сохранения естественного объема легких, но, если это не сделано, то при оценке находимых под микроскопом изменений следует считаться с результатами специально производившихся исследований. Так, Rahn установил, что прижизненная закупорка бронха не ведет к полному спадению легочной ткани, обнаруживаемому в таких случаях при обычной методике вскрытия. На самом деле в участке, дренируемом выключенным бронхом, альвеолы лишь уменьшаются в размерах, отчасти заполняясь отечной жидкостью («дистелектаз»). Rahn указывает также, что в легких, фиксированных in situ, нет ни-
каких «физиологических ателектазов», описанных Verzar и Jeker'. Впрочем, ошибку этих исследователей уже раньше вскрыл Mollendorff (1942).
Другие артефакты, возникающие как в живых, так и в мертвых тканях
Внимательный осмотр органов простым глазом (или с помощью лупы) является важным этапом большинства морфологических исследований. Но чем подробнее и дольше он делается, тем хуже для дальнейшего микроскопического изучения. Особенно чувствительны к пребыванию на воздухе ткани, сохранившие жизнеспособность. Так, цилиндрический эпителий обнаженных на раннем вскрытии или иссеченных на операции слизистых оболочек буквально в первые же минуты становится низким и пикнотичным. Совсем непонятно, почему некоторые прозекторы приступают к вырезанию кусочков для микроскопического исследования лишь в конце вскрытия, когда органы вдобавок испачканы или помяты.
Совершенно губительное действие оказывает на эпителиаль-
ные покровы пищеварительного тракта |
и |
дыхательных путей |
п р о м ы в а н и е в о д о й (см. гл. V). |
В |
прозектурах нередко |
промывают струей из шланга и поверхность разреза паренхиматозных органов, что уже совсем бессмысленно, так как здесь загрязнения, мешающие осмотру, проще соскоблить, не рискуя вызвать гемолиз и другие артефакты.
Поверхность разреза живой или переживающей ткани, особенно если он сделан недостаточно острым ножом (а тем более— ножницами), наименее пригодна для гистологических исследований. При пункционных и аспирационных биопсиях, когда весь получаемый кусочек очень невелик, с этим приходится мириться. Но вырезать маленькие кусочки, необходимые для электронной микроскопии, лучше после предварительной
фиксации материала |
(Д. |
С. Саркисов и Б. В. Втюрин)2. |
|
|
В некоторых случаях |
наблюдаются особые артефакты, обу- |
|||
словленные р а з н о с о м |
по п о в е р х н о с т и |
р а н ы |
о б - |
|
р ы в к о в т к а н е й |
и к л е т о к . Прежде это |
отмечали |
глав- |
|
ным образом в кусочках, содержащих кость и полученных путем выпиливания, где опилки могут оказаться в самых неожиданных местах. Беспорядочность их расположения и отсутствие какой-либо реакции вокруг позволяют догадаться об артефакте
1 О «физиологических |
ателектазах» |
писали и раньше, в частности |
Г. Е. Земан (1925), Gerlach |
и Finkelday |
(1926), Lauche (1931). |
2 Теперь для такой предварительной фиксации с успехом применяют глутаральдегид.
22 |
23 |
|
(Т. В. Виноградова). Однако для электронной микроскопии и разрез органа бритвой может оказаться слишком грубым приемом. Muller (1966), изучая надпочечники, наблюдал разрывы плазматических мембран клеток и попадание гранул катехоламинов, лизосом, митохондрий и других цитоплазматических образований в периваскулярные пространства, в просвет кровеносных сосудов и даже внутрь соседних клеток. Сам Muller считает это следствием сдавливания нежных клеток глубокой зоны (граничащей с мозговым слоем) коры надпочечника, а не прямого их повреждения при вырезании кусочка. Он указывает на ошибки, допущенные другими исследователями, не догадавшимися о возможности таких артефактов.
При вырезании кусочков из органов с трубчатым строением (например, почек) частицы поврежденной ткани могут вдавливаться в просвет трубок. Не удивительно, пожалуй, что через перерезанные почечные канальцы детрит и целые эпителиальные клетки иногда проникают даже внутрь капсул, окружающих клубочки. Но почти неправдоподобным кажется сообщение Sakaguchi и Dachs (1965): в кусочках почек, полученных путем пункционной биопсии, они дважды наблюдали заполнение клеточным детритом к а п и л л я р о в клубочков. Исследование срезов под электронным микроскопом подтвердило наличие внутри неизмененных капилляров остатков ядер, митохондрий и обрывков щетковидной каймы почечного эпителия. Попасть сюда эти частицы могли только через поврежденные при биопсии артериолы.
Не менее оригинальным и способным поставить в тупик исследователя артефактом является описываемое во второй части нашей книги вдавливание клеток кроветворной ткани под мягкую оболочку мозга. Но чаще всего поводом для недоразумений н споров служат самые простые образования, например кровоизлияния при биопсиях или периваскулярные геморрагии в мозгу, «кровяные озера» в хрупкой пульпе селезенки и т. д., которые могут быть и следствием патологических процессов, и результатом неосторожного обращения с органами на вскрытии.
Таким образом, уже на самом первом этапе работы морфолога— во время получения материала для микроскопических исследований — возникают разнообразные артефакты. Проявляя бережность, пользуясь очень острыми инструментами и применяя некоторые специальные приемы, удается уменьшить вред, наносимый тканям (особенно живым), подлежащим исследованию. Но полностью избежать повреждений и артефактов, пожалуй, нельзя. Остается, следовательно, помнить об их возможности, критически оценивая результаты последующих наблюдений. ,. . ,
Глава И
ТЕРМИНАЛЬНЫЙ ПЕРИОД ЖИЗНИ, АГОНИЯ, СМЕРТЬ
Морфологические изменения, описанные в предыдущей главе, являются настоящими артефактами; они создаются искусственно (хотя и без умысла) и в известной мере могут быть предотвращены.
Следующая группа помех возникает уже вне зависимости от опыта и аккуратности исследователя. Их привносят особые процессы, происходящие в заключительном периоде жизни больного или здорового организма.
Патофизиологи, изучавшие процесс умирания, выделяют 3 его этапа: преагональное состояние, агонию и клиническую смерть (В. А. Неговский и В. М. Шапиро, 1966). Но чаще говорят просто об агонии, или терминальном периоде жизни, включая сюда и грозные состояния комы, коллапса и шока, если они неотвратимо ведут к гибели. Пусть это не вполне правильно, но и мы в соответствии с поставленными задачами не можем строго ограничить понятие агонии. Если морфолог интересуется не самим механизмом наступления смерти (или развития шока), то все предшествовавшие ей нарушения функций организма лишь мешают изучать ранее протекавшие нормальные и патологические явления.
В подлинном смысле слова «агония» означает «борьба., между жизнью и смертью». Несмотря на архаичность такого определения, оно показывает, что в терминальном периоде не просто нарушается деятельность жизненно важных органов и возни- ^ают те или иные повреждения, но возможны напряженные дадагенсаторные процессы, отдаляющие смертельный исход. Они также оставляют свои следы, обнаруживаемые при микроскопических исследованиях. Конечно, меньше всего терминальных наслоений должно быть при быстрой гибели здорового организма, но даже мгновенная смерть не фиксирует с абсолютной точностью прижизненное состояние органов и клеток. Разрушен продолговатый мозг, и смерть несомненна, но в мертвом теле какое-то время продолжается жизнь — хаотичная, ничем не регулируемая. Внезапно остановилось сердце, однако кровеносные сосуды могут некоторое время беспорядочно сокращаться (А. И. Левин, 1933). Возможны также судорожные спазмы гладкой мускулатуры кишок, бронхов и т. д., в той или иной степени искажающие нормальные морфологические картины.
При разных видах случайной смерти наблюдаются и особые' изменения, тщательно изучаемые судебными медиками. Но наряду с этим экспериментаторы, убивая подопытных животных электрическим током, ударом по затылку, отравляя их
24
25
хлороформом и т. д., далеко не всегда учитывают побочные результаты таких воздействий. Для некоторых биохимических, микробиологических и даже морфологических исследований (например, при изучении развития опухолей или отложения липоидов в стенках сосудов) привходящие изменения, связанные с механизмом смерти, не столь уж важны, но во многих других работах весьма нежелательны и даже недопустимы.
О б е з г л а в л и в а н и е животных сопровождается не |
только |
кровопотерей, но и значительным затеканием крови в |
бронхи |
и легочные альвеолы, что обычно происходит (вследствие по-
вреждения |
основания |
черепа) и |
при |
р а з р у ш е н и и |
п р о - |
||
д о л г о в а т о г о м о з г а |
ударом |
по затылку или |
сильным |
||||
растягиванием тела. |
М е х а н и ч е с к а я |
а с ф и к с и я |
и от - |
||||
р а в л е н и е |
у г а р н ы м |
г а з о м |
оставляют такие |
же |
следы |
||
(в частности, мелкие кровоизлияния в органах и под серозными
покровами), как и соответственные виды |
смерти у человека. |
То же можно сказать и об умерщвлении |
э л е к т р и ч е с к и м |
т о к о м — способ, рекомендованный А. И. Метелкиным (1938), но наименее, пожалуй, пригодный для микроскопических исследований. При удушении х л о р о ф о р м о м и э ф и р о м может успеть проявиться токсическое действие этих веществ на клетки печени, миокарда, дыхательных путей, но особенно резко выраженными бывают расстройства кровообращения. Этого не случается при гибели от в о з д у ш н о й э м б о л и и , которую совсем напрасно хулит М. Б. Раппопорт (1967), указывая, что после введения воздуха в вену бывает длительная агония. У мышей точное введение в хвостовую вену 0,25—0,5 мл воздуха вызывает мгновенную смерть почти без судорог. Однако у кроликов так происходит не всегда, а кроме того, им ввести воздух в ушную вену иногда бывает затруднительно из-за внезапно наступающего (особенно у альбиносов) спазма кровеносных сосудов. Лучше всего прижизненное состояние тканей должно сохраняться у животных, неожиданно падающих в дюаров сосуд с инертным газом, сжиженным при очень низкой температуре. Но этот прием, используемый иногда в гистохимии, применим только на мелких животных (при замедленном промерзании тканей появляются свои артефакты) и, обладая целым рядом неудобств, не получил распространения.
В общем, способ умерщвления животных нужно выбирать в соответствии с основными целями опыта. Выбирать приходится эмпирическим путем, так как никто еще не проделал очень нужной работы — сравнительного всестороннего изучения всех тех приемов, которые используются на практике1. Веро-
1 Отчасти сюда могут быть отнесены исследования А. Ю. Рудницкой (1953), выполненные в нашей лаборатории, но они касались только распределения лейкоцитов в кровеносной сети кролика при разных способах умерщвления.
ятно, полезной была бы и разработка новых. Д. С. Саркисов и Б. В. Втюрин, рассмотрев целый ряд существующих способов забоя лабораторных животных, находят, что ни один из них не дает возможности сохранить в достаточно полной мере прижизненную ультраструктуру миокарда.
Морфологические следствия функциональных расстройств,
происходящих в терминальном периоде жизни
Одним из наиболее частых проявлений агонии служит расстройство циркуляции крови в организме. Оно зависит от нарастающей слабости сердца или от особых патологических реакций, лежащих в основе шоковых состояний и коллапса. На вскрытии признаком ослабления сердечной деятельности может служить застой крови, подчиняющийся, в общем, физическим законам. В некоторых случаях по преимущественному накоплению крови в венозной сети тех или иных органов можно догадываться о механизме наступления смерти. Г. В. Шор (1925) описал признаки, характеризующие слабость правого и левого отдела сердца. Судебные медики и военные патологи большое внимание уделили локализации крови трупа при шоковых состояниях, для которых характерна задержка крови в отдельных участках кровяного русла — так называемых «депо». Но это наблюдается главным образом в опытах на животных, ча не у людей, погибших при явлениях шока (Н. А. Краевский, 1944, 1955).
Наиболее понятным (и частым) следствием терминальных расстройств кровообращения служит о т е к л е г к и х , особенно задних их отделов. Его объясняют гипоксией и нарушением проницаемости стенок сосудов при застое крови. Popper (1948, 1954, 1957) считает, что сходные причины лежат и в основе д и с с о -
ц и а ц и и п е ч е н о ч н ы х |
к л е т о к , |
а |
также некроза |
цен- |
|
тральных участков |
долек |
печени и |
р а с ш и р е н и я |
п р о - |
|
с т р а н с т в Диссе. |
Странно, однако |
(и |
малоправдоподобно), |
||
что, по его мнению, эти патологические явления развиваются очень быстро — уже спустя 10 минут от начала агонии. Но, не-
сомненно, |
быстро могут возникнуть г е м о р р а г и и |
п о д с е - |
р о з н ы м и |
о б о л о ч к а м и л е г к и х и с е р д ц а . |
Первона- |
чально они были описаны Tardieu в качестве признака асфиксии, однако нередко встречаются и при других видах смерти (М. И. Авдеев, 1957).
Особые причины (спазм сосудов?) лежат в основе развития г е м о р р а г и и и э р о з и й в с л и з и с т о й о б о л о ч к е ж е - л у д к а и кишок, наблюдающихся при поражениях головного мозга, шоковых состояниях и различных интоксикациях. Selye
26 |
27 |
(1960) относит их к побочным результатам «реакции напряжения», но Hulse (1961) находил такие же кровоизлияния и у белых лабораторных мышей, погибших от голода или старости. Наши исследования о генезе «гранулем Дюрка» (М. В. ВойноЯсенецкий, 1947) не подтверждают гипотезы Cammermeyer (1953), по которой агональную природу имеют и своеобразные мелкие кольцевидные кровоизлияния в белом веществе мозга, возникающие при жировой эмболии, уремии, малярийной коме, энцефалитах и некоторых других патологических состояниях. Не прошли должной проверки наблюдения Christeller (1920), обнаружившего в 45% больничных вскрытий атональные кровоизлияния в тканях шеи вблизи верхней полой вены, хотя этот факт (или артефакт) мог бы иметь серьезное значение в некоторых случаях судебно-медицинской экспертизы.
Большинство отечественных патологов считают агональным явлением ф р а г м е н т а ц и ю м и о к а р д а , особенно в тех случаях, когда она диффузно захватывает волокна сердечной мышцы (М. И. Авдеев, 1938; А. И. Абрикосов, 1940, и др.). Полагают, что ее причиной служат беспорядочные судорожные сокращения здоровой сердечной мышцы во время бурной кратковременной агонии. При более продолжительной агонии развитию фрагментации способствуют предшествовавшие патологические изменения миокарда (А. И. Абрикосов). Но другие исследователи относят фрагментацию к числу артефактов, указывая, что против ее прижизненного или атонального происхождения говорит отсутствие кровоизлияний. Aschoff (1937) видит причину разрыва волокон миокарда в травматических повреждениях (сминание руками, ножом) окоченевшего сердца на вскрытии.
Проявления и следствия компенсаторных реакций
С терминальными реакциями связано довольно много ошибок и разногласий, возникающих между морфологами. Это происходит главным образом потому, что, изучая гистологические препараты, мы видим не столько непосредственные проявления реактивных процессов, сколько их следствия, сами по себе недостаточно характерные. К числу таких следствий относятся прежде всего признаки усиленного, но не пополняемого р а с х о - д о в а н и я в н у т р и к л е т о ч н ы х з а п а с о в п и т а т е л ь - ных в е щ е с т в .
Обе микрофотографии, представленные на рис. 9, сделаны со срезов печени совершенно здоровых людей, погибших случайно. Такие же парные иллюстрации приводит в своей работе Popper (1948), доказывая, что столь поразительная разница зависит от продолжительности атонального периода: если он
Рис. 9. Печень случайно погибших здоровых людей
„ - п р и мгновенной смерти, Х410, б - при |
затянувшейся агонии, Х435 Гематоксилин- |
эозин. |
|
Рис. 10. Клетки коркового слоя надпочечника здоровых людей.
о-при мгновенной смерти, б - при гибели через 21/2дня после случайной травмы, Х165 (по W. F. Enos и сотр , 1955).
29
28
длился не более 10. минут или смерть наступила мгновенно, то печень на обычных гематоксилин-эозиновых препаратах имеет такой вид, как на рис. 9, а. Светлые и как бы пустые и четко очерченные клетки здесь напоминают растительную клетчатку. Если же агония затянулась, то клетки печени становятся мельче и темнее, благодаря чему лучше различима структура долек, но границы между самими клетками менее ясны; кроме того, возле синусоидов появляются широкие щели (рис. 9, б).
Конечно, на рис. 9 показаны крайние, наиболее резко выраженные изменения нормальной печеночной ткани, обусловленные различным содержанием гликогена внутри клеток. Чаще наблюдаются промежуточные картины. Они больше соответствуют общеизвестным схематическим изображениям структуры печени и специально подбираемым учебным препаратам. Поэтому светлые, богатые гликогеном печеночные клетки могут даже показаться ненормальными, подвергшимися гидропической дегенерации (Soo&tmeyer, 1940).
В связи с изложенным возникает подозрение, что так называемые очаговые дистрофии и некрозы клеток печени (часто находимые у лабораторных животных при различных вредных воздействиях, реже — при шоковых состояниях у человека) не всегда на самом деле служат проявлением дегенерации или некроза. Это могут быть просто участки ткани, сохранившей по каким-то причинам высокое содержание гликогена (Soostmeyer, A. M. Вахуркина, 1964). Во всяком случае, описания «водяночного перерождения» (Apitz, 1933) или «боллонирующей дистрофии» печеночных клеток (новый не совсем удачный термин), равно как и микрофотографии некоторых «некрозов», иногда очень напоминают светлый мозаичный рисунок богатой
гликогеном |
нормальной |
печеночной ткани. Настораживает и |
. сравнение |
таких очагов |
с растительной клетчаткой (Popper, |
*.1954; В. Л. Бялик и М. И. Шейнис, 1950, и др.), сходство с которой как раз характерно для нормальной ткани печени, а установить наличие в них гликогена может помешать посмертный аутолиз.
При многих заболеваниях отмечается обеднение липоидами коркового слоя надпочечников. По данным Enos, Beyer и Holmes (1955), это может произойти и в терминальном периоде жизни. На парафиновых и целлоидиновых срезах клетки коры надпочечника здоровых, внезапно погибших людей выглядят так, словно они подверглись вакуольной дегенерации (рис. 10, а). После длительной агонии, когда липоиды исчезают, цитоплазма этих клеток становится однородной и хорошо окрашивается (рис. ГО»б). Словом, происходит почти то же самое, что и в печени, теряющей гликоген. Однако в надпочечниках, занимающих центральное место в концепции Selye, «stress», вызывает и более сложные изменения, отображающие не просто утрату
липоидов, но и усиленную выработку гормонов (см. Б. П. Угрюмов, 1963). Возможна и истинная вакуолизация, доказываемая отрицательными результатами контрольной окраски на жир.
Какую-то не совсем еще ясную роль в синдроме напряжения играет усиленный р а с п а д к л е т о к л и м ф о и д н о г о т и п а . Это особенно ясно можно видеть в корковом слое вилочковой железы животных, погибших при явлениях интоксикации или подвергшихся действию проникающих излучений. Прежде думали о прямом повреждении клеток, но Selye (1936) указывает, что, удаляя предварительно надпочечники, удается предотвра-
тить «атрофию» вилочковой железы. Это |
подтвердилось и |
в опытах, делавшихся в нашей лаборатории |
(Л. С. Бибинова |
и др., 1962). Вероятно, распад лимфоидных клеток имеет характер какой-то реакции, нужной организму и осуществляемой при участии кортикостероидных гормонов надпочечника (которые сами по себе вызывают резкую «атрофию» тимуса).
Агонаяьный лейкоцитоз и распределение лейкоцитов в кровяном русле
Увеличение числа лейкоцитов в крови умирающих людей впервые наблюдал Litten (1883). В дальнейшем это явление (отнюдь, впрочем, не обязательное) было подтверждено многими исследователями, расходившимися, однако, в его оценке и объяснениях (Arnet, 1904; П. П. Движков, 1926; Ф. С. Волченок, Ш32, и др.).
to По мнению Ehrlich и Lazarus, агональный лейкоцитоз — всего лишь артефакт, причиной которого является краевое стояние белых кровяных телец в периферических сосудах, вызванное ослаблением циркуляции крови. Так это или не так, но важно, что клинические исследования крови, получаемой из пальца, несмотря на их большую ценность, не всегда отображают действительное содержание лейкоцитов в организме. Даже в капле крови, добытой уколом из участка, где капилляры заполнены лейкоцитами, может оказаться лейкопения (И. В. Давыдовский и П. П. Движков, 1925; Hoff, 1935). Истинное представление о содержании и распределении белых кровяных телец в организме, очевидно, можно получить путем гистологических исследований, если этому не препятствует агональное или посмертное их перемещение.
Некоторые сведения о распределении полиморфноядерных лейкоцитов в кровяном русле здоровых людей при случайной смерти и боевых травмах имеются в работах Herxheimer (1927), Н. А. Краевского (1944, 1945), С. С. Вайля (1943), Ю. В. Гулькевича (1948), В. Л. Бялика (1955). Специальные исследования, ограниченные, однако, одним или немногими органами,
30
31
проводили Lex (1931), В. Н. Марголин (1935), Л. Б. Шейнина (1935), Л. Г. Шамесова (1940), Н. Н. Гольдбурт (1964, 1965). Наиболее подробно и тщательно этот вопрос изучал Д. М. Логойда (1954, 1959). Невзирая на кое-какие расхождения этих авторов в деталях, можно считать установленным следующее:
1. Посмертные (гипостатические) перемещения крови не затрагивают лейкоцитов, находящихся в мелких сосудах и капиллярах. Благодаря своей липкости (или по иным причинам) они,
впротивоположность эритроцитам, остаются на своих местах.
2.Распределение лейкоцитов в разных участках сосудистого русла всегда неравномерно, но не беспорядочно.
3.Критерием «нормы», очевидно, может служить локализация лейкоцитов в кровеносной сети быстро погибших здоровых людей.
4.При затянувшейся агонии (или, вернее, при длительном терминальном периоде жизни) содержание лейкоцитов в сосудах большинства органов (особенно легких, печени, почек) увеличивается, а в селезенке и стенках пищеварительного тракта уменьшается, причем вне зависимости от степени кровенаполнения того или иного органа.
Д.М. Логойда считает, что в спорных случаях судебно-меди- цинской экспертизы распределение зернистых лейкоцитов в сосудах трупа дает возможность судить о времени, прошедшем между нанесением травмы и смертью пострадавшего. По Enos и др. (1955), весьма показательно содержание в пульпе селезенки эозинофилов: при внезапной смерти их насчитывается 10—20 в каждом поле зрения микроскопа (под большим увеличением), а если агония длилась от 30 минут до 5 часов, то не более 1—2. Позже эозинофилы отсюда совсем исчезают. Менее ясна зависимость терминального лейкоцитоза от характера повреждений. Данные В. Л. Бялика и Д. М. Логойды противоречат указанию Н. Н. Гольдбурта (1965) о том, что больше всего лейкоцитов в сосудах внутренних органов бывает при повреждениях мозга. Но какая-то связь между механизмом смерти и распределением зернистых лейкоцитов в разных участках кровяного русла все же, по-видимому, существует.
В материале, изученном Д. М. Логойдой, был случай, когда сразу погибла от асфиксии группа людей одинакового возраста, находившихся в одинаковых условиях, в том числе и через одно и то же время после приема одинаковой пищи. Исследования, сделанные у 4 из них, показали удивительное сходство распределения и содержания зернистых лейкоцитов в капиллярной сети всех внутренних органов. При других видах быстрой смерти подсчеты лейкоцитов иногда давали почти такие же, но чаще несколько иные результаты, хотя разница и не всегда выходила за пределы точности методики исследований. Более заметным оказывалось иногда различие в распределении лейкоцитов в некоторых отделах кровяного русла при общем лейкоцитозе, наступавшем через 1 час и позже после смертельной травмы.
Сложна, конечно, оценка содержания и распределения лейкоцитов в органах трупа при смерти от болезней, которые сами по себе вызывают общие лейкоцитарные реакции. Однако и в таких случаях, если учитывать изменения, происходящие при «простой агонии», и исследовать разные органы и ткани, можно получить ценные сведения о прижизненных реактивных процессах. Напротив, изучение одного только органа способно привести к ошибкам. Так, наблюдая терминальный лейкоцитоз в сосудах легких, трудно отделаться от мысли о начале развития пневмонии, если не знать, что то же самое произошло и в других отделах кровяного русла. Как указывают С. С. Вайль (1943), Д. М. Логойда (1954) и Н. Н. Гольдбурт (1965), аналогичную ошибку допустили А. И. Абрикосов и Е. А. Рудик, принявшие накопление полинуклеаров в сосудах почек за раннюю стадию гломерулонефрита.
Поскольку у человека для развития терминального лейкоцитоза внутренних органов требуется некоторый срок (по данным Д. М. Логойды, около 1 часа), то это явление, казалось бы, нет необходимости принимать в расчет при умерщвлении животных при экспериментальных работах. Однако специальные исследования, выполненные А. Ю. Рудницкой (1953) на кроликах, призывают к осторожности. У этих животных клеточный состав крови (вообще не отличающийся постоянством) легко изменяется при разных воздействиях, в том числе и ведущих к быстрой смерти (удар по затылку, отравление эфиром и др.). Наиболее пригодной для изучения локализации лейкоцитов оказалась воздушная эмболия, прекращающая циркуляцию крови вследствие тампонады воздухом правого желудочка сердца. Этот способ оправдал себя и в других работах, выполнявшихся в нашей лаборатории на разных животных, но он требует безупречной техники. Так, например, в капиллярах 100 легочных альвеол быстро убитых здоровых мышей насчитывается 20—40 зернистых лейкоцитов, а в 100 почечных клубочках — около 10. После повторных неудачных попыток ввести воздух в хвостовую вену эти цифры могут возрасти в 2—3 раза.
Г.. Е. Земан (1925), Gerlach и Finkeldey (1926) допустили явную ошибку, указывая, что легочные капилляры мышей и морских свинок весьма богаты лейкоцитами. Эти исследователи применяли удушение животных хлороформом, а при таком способе (как и при смерти от вдыхания эфира) возникает резкий общий лейкоцитоз.
32

Отображение агонии в морфологии патологических процессов. Осложнения, возникающие в терминальном периоде
Для морфолога, занятого изучением патологических процессов, изменения, возникающие во время агонии, важны по двум причинам. Во-первых, они во многом сходны с тем, что связано с самой болезнью. Так, лейкоцитоз, обнаруживаемый в кровеносных сосудах умершего человека или животного, совсем не
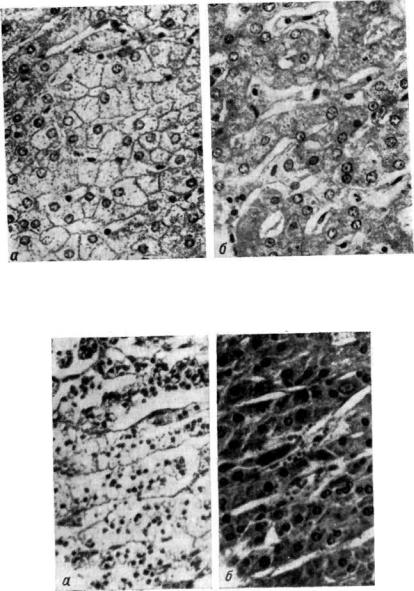
Рис. 11. Экспериментальная пневмония у мышей
Животные, убитые через сутки после заражения, находились а — в удовлетворительном и б — в атональном состоянии. Судан-альфанафтол, XI10.
обязательно бывает атональным Уменьшение внутриклеточных резервов питательных веществ может произойти задолго до наступления терминального периода жизни, если они недостаточно пополняются извне или почему-либо нарушена деятельность пишеварительных органов. Здесь разобраться не легко, но всетаки можно, если иметь полноценные клинические данные, знать особенности «чистой» агонии и пользоваться методом исключений.
Вторая причина не менее серьезна. В терминальном периоде нередко изменяется характер самих патологических процессов. Клиницисты не совсем ошибаются, высказывая подчас сомнение в познавательной роли «атональных картин болезни», обна-
руживаемых на вскрытии умершего человека. Жаль, что такие сомнения не всегда возникают у самих морфологов. А это видно хотя бы из того, что во многих экспериментальных работах они изучают только органы животных, погибших по ходу опыта, или описывают, не разграничивая, результаты наблюдений, сделанных на животных, убитых во время болезни и у павших. Нельзя, конечно, ожидать, чтобы особенности терминального периода жизни заметно сказывались на развитии опухоли, но заживление ран, компенсация недостаточности органов или течение инфекционных процессов могут быть нарушены.
На рис. 11—фотографии со срезов из легких двух мышей, убитых через 24 часа после интраназального введения дизентерийных бактерий. Одна из них находилась в более или менее удовлетворительном состоянии, другая явно погибала. Окраска срезов судан-альфанафтолом очень наглядно показывает разницу в защитной реакции организма. У первой (см. рис 11, а) зернистые лейкоциты заполняют альвеолы, где они (как видно при других способах окраски) успешно фагоцитируют микробов. У второй (см. рис. 11,6) произошло явное торможение эмиграции лейкоцитов: они задерживаются на стенках кровеносных сосудов, а те, что раньше проникли в альвеолы, разрушаются, не справляясь с беспредельно растущими бактериями.
Возможно, что в приведенном примере не агония повлекла за собой столь явную недостаточность защитных функций организма, а животное потому и гибнет, что осуществление этих функций нарушилось. Бывает и иначе. Известно, что легко присоединяются и своеобразно текут вторичные «аутоинфекционные» осложнения в последние дни жизни больных. У лабораторных животных в терминальном периоде очень нередки вспышки какой-нибудь латентно протекавшей инфекции. Во всяком случае, «агональные картины болезни» существуют и с ними приходится считаться.
Глава III
ПОСМЕРТНЫЕ ИЗМЕНЕНИЯ
Принятое подразделение трупных изменений на «ранние» и «поздние» отображает не только последовательность, но и различие в причинах их развития. К р а н н и м относятся изменения, связанные с физическими и химическими процессами (охлаждение, гипостазы, окоченение, свертывание крови и т. д.), и явления аутолиза клеток и тканей. П о з д н и м и называют глав-
ным образом последствия роста в |
мертвых тканях гнилост- |
ных микробов — последствия, весьма |
ощутимые и обычно не |
34 |
35 |
вызывающие сомнений. А ранние трупные изменения, начинающиеся уже в первые минуты после смерти, сплошь и рядом приводят к серьезным просчетам в работе не только патологоанатомов, но также гистологов и цитологов. Кроме того, они имеют и большое самостоятельное значение в связи с все расширяющимся применением тканей и даже органов трупа для пересадок.
Перемещение крови
Постепенное перемещение крови в сосуды нижних (или зад-
них— при обычном лежании трупа |
на спине) частей |
тела |
хо- |
||
рошо известно. Все |
же лечащие врачи, придя |
на |
вскрытие, |
||
иногда удивляются |
почти полному |
отсутствию |
экзантем |
или |
|
тех ярких признаков рожистого воспаления, которые они наблюдали при жизни больных. И прозектора не всегда учитывают, что прижизненная гиперемия довольно быстро ослабевает не только на наружных покровах верхней поверхности тела, но и во внутренних органах. Это может затруднить распознавание некоторых патологических процессов, например острого катара кишечника (Siegmund, 1929). Вместе с тем гипостазы, сопровождающиеся другими посмертными изменениями (например, аутолизом в поджелудочной железе), могут дать повод для ошибочного диагноза каких-нибудь патологических процессов.
В главе II указывалось, что посмертное перемещение содержимого кровеносных сосудов не затрагивает белые кровяные тельца, находящиеся в капиллярной сети. Но в более крупных сосудах лейкоциты все же оседают, располагаясь сплошным слоем поверх опустившихся вниз эритроцитов. Поэтому случается— особенно при высоком лейкоцитозе,— что на небольшом протяжении просвет какой-нибудь вены или артерии бывает густо заполнен белыми кровяными тельцами. Такие картины не раз описывали под видом лейкоцитарных тромбов. Оседание же лейкоцитов возле стенки кровеносного сосуда может навести на мысль о прижизненном их краевом стоянии. По мнению Fischer-Wasels (1929), именно такой артефакт лежит в основе ошибки Mollendorff (1927), описавшего образование лейкоцитов из эндотелия яремной вены.
В самых полных руководствах по патологической анатомии, где подробно описаны разные формы отека легких и изложены существующие гипотезы о механизмах его развития, совсем ничего не сказано о возможности посмертного выхождения жидких составных частей крови из сосудов в альвеолы. Довольно обычная отечность, сопутствующая на вскрытиях гипостазам в задних отделах легких, по традиции признается за агональное явление. Так расценивают даже отек резко полнокровных лег-
36
ких, постоянно находимый у людей, удавившихся в петле1. Это не кажется удивительным, поскольку сердце может некоторое время сокращаться, нагнетая кровь в легочные сосуды после остановки дыхания. Странно только, почему за такой, несомненно короткий, период столь резко повышается проницаемость кровеносных сосудов. Но дело, по-видимому, вообще обстоит иначе.
Durlacher и сотр. (1950) наблюдали, что у кроликов, убитых разными способами, легочная ткань непосредственно после смерти воздушна и кровенаполнение ее равномерно. Но если вскрывать трупы животных спустя 3 часа, то обнаруживается не только перемещение крови в нижележащие отделы легких, но альвеолы здесь, как правило, заполняются белковой жидкостью. Позже трупный отек усиливается, захватывая большие участки легочной ткани. Отека легких не было лишь при умерщвлении животных обескровливанием. Эти наблюдения затем подтвердил Morada (1968), отметивший, что у новорожденных кроликов, в противоположность взрослым, посмертный отек легких не развивался.
Если правы Durlacher и Morada, то описания отека легких, обнаруживаемого по ходу тех или иных опытов у лабораторных животных, вскрывавшихся спустя некоторое время после их гибели, должны быть признаны недостоверными. Но, что еще важнее, пересмотру подлежат и аналогичные находки, обнаруживаемые на вскрытиях трупов людей. "Поэтому, по нашей просьбе, В. И. Парусов провел еще одну проверку изложенных данных, использовав разных животных. Он нашел, что не только
укроликов, а также у здоровых морских свинок и крыс в первые же часы после смерти (кроме смерти от обескровливания) развивается обширный сплошной или очаговый отек легких. Но
умышей посмертного отека легких не возникало, даже если их трупы хранились при +37° С в течение 24—48 часов. Следует отметить, что у здоровых мышей в таких условиях не наблюдалось и трупной отслойки эпителия бронхов, обычно происходившей у кроликов. Однако у мышей с искусственно вызванными инфекционными и токсическими поражениями легких
после смерти определенно усиливалась отечность в области повреждений и отмечалось слущивание эпителия2.
1К посмертным явлениям у повешенных Mueller (1953) относит лишь накопление жидкости в плевральных полостях, постепенно просачивающейся, по его мнению, из легочной ткани.
1При искусственном отеке, вызванном промыванием легочных сосудов физиологическим раствором, Lange (1909) наблюдал массивное слущивание клеток, выстилающих альвеолы («альвеолярного эпителия»). Возможность такого артефакта не учли Janssen и Bartschi (1964), полагающие, что при посмертном отеке легких у морских свинок, погибших от асфиксии, происхо-
дит «резкая мобилизация альвеолярных клеток>, образующих «целые колонии» в отечных участках.
37

С результатами опытов на животных совпадают и данные, полученные Heikel (1967) путем рентгенологических исследований трупов 58 новорожденных я маленьких детей. Он делал повторные снимки грудной клетки и обнаружил, что через 6 часов после смерти, а еще яснее — через 12—24 часа, заметно увеличивается плотность легочной ткани одной или нескольких долей. Гистологические исследования показали, что в таких затемненных участках альвеолы содержали отечную жидкость. Непонят-
ным осталось, |
почему |
трупный |
отек |
развился |
не |
во |
всех, |
а только в 46 |
случаях, |
и почему |
он |
захватывал |
не |
все |
доли. |
Но Heikel, в соответствии с наблюдениями В. И. Парусова, отметил, что посмертное увеличение рентгенологической плотности (иначе — появление отека) было сильнее выражено в тех долях легких, где имелись очаги пневмонии.
Таким образом, патологические процессы, повышающие проницаемость кровеносных сосудов, должны способствовать развитию посмертного отека легких. Это необходимо иметь в виду, оценивая результаты вскрытий.
Оноченение сердца
имышечного слон артерий
Всвязи с обсуждаемыми вопросами можно не касаться трупHdro окоченения скелетной мускулатуры. Оно имеет значение главным образом для судебных медиков и подробно ими изучено. Иначе обстоит дело с окоченением мышцы сердца.
С давних пор дряблость, расслабленное состояние сердечной мышцы на вскрытии расценивалось как свидетельство прижизненной ее дегенерации. И не менее давно критически мыслящие исследователи указывали, что такая дряблость может быть просто результатом разрешившегося уже окоченения миокарда. Однако до сих пор она дает! повод для диагноза «паралича болезненно измененного сердца», довольно часто фигурирующего в заключениях о причине смерти. Этим же признаком нередко руководствуются, описывая поражения сердца при различных болезнях. Между тем, только при очень резко выраженной дегенерации мышечных волокон сердце не способно к трупному окоченению (А. И. Абрикосов, 1940).
В момент смерти сердце, по-видимому, всегда расслаблено (Volkhard, 1916). Но затем очень быстро — примерно в течение часа (т. е. быстрее, чем в скелетных мышцах)—в нем развивается окоченение (А. И. Абрикосов, 1940). Отсюда —характер- ная плотность мышцы и сокращение объема желудочков. Однако позже, когда окоченение проходит, сердце снова становится дряблым. Следовательно, оценивая состояние сердечной мышцы, совершенно необходимо учитывать (и указывать при публикации работ) время, прошедшее между смертью и вскрытием.
Иначе нельзя решить, от чего зависела ее дряблость — от дистрофии мышечных волокон, препятствовавшей сокращению, или от того, что окоченение просто уже разрешилось. А разрешается оно также довольно скоро.
Для иллюстрации приведу пример из прежних своих наблюдений. Табл. 1 показывает, что то или иное состояние сердечной мышцы на вскрытии обусловлено в основном трупными процессами.
ТАБЛИЦА 1
Дряблость миокарда при злокачественной, малярии в зависимости от времени, прошедшего между смертью больного и вскрытием трупа
|
Срок |
между смертью |
Число |
Дряблость |
|
|
|
и вскрытием |
случаев |
миокарда |
|
До |
5 часов |
|
21 |
1 |
|
От |
5 до |
10 часов |
16 |
3 |
|
» |
10 » |
20 |
» |
37 |
17 |
Свыше 20 часов |
20 |
17 |
|||
Труднее решить, от чего зависит сокращение артерий, столь часто обнаруживаемое при гистологических исследованиях: от окоченения их мышечного слоя, спазма сосудов в момент смерти или контрактуры мышечных волокон (долго сохраняющих раздражимость) при иссечении кусочков артерий и действии на них фиксаторов.
MacWilliam и Mackie (1908) и MacCordik (1913), исследуя вырезанные фрагменты артерий, применяли перед фиксацией термические и химические воздействия, расслабляющие сократившиеся гладкие мышечные волокна, а затем нагнетали фиксирующую жидкость в просвет перевязанного отрезка сосуда под давлением в 150 мм рт. ст. (MacCordik). Для изучения размеров просвета артерий целого органа или части тела можно ограничиться внутриартериальным введением раствора формалина под давлением 70—80 мм рт. ст. (Э. Э. Кикайон, 1960).
При сокращении артерий и окоченении мышцы сердца вытесняется содержавшаяся в них кровь, если она не успела свернуться. Из желудочков сердца кровь поступает в аорту и в легочную артерию, обычно растягивая предсердия, обладающие сравнительно слабой мускулатурой. Аорта и крупные артерии эластичного типа сокращению не подвергаются и на вскрытиях обычно бывают почти пустыми лишь потому, что кровь из них вытекает через перерезаемые ответвления (Л. М. Шабад, 1927).
Биохимические процессы, лежащие в основе окоченения мышечной ткани, очевидно, не оказывают на нее вредного влияния: изолированное сердце можно заставить ритмически сокращаться по прошествии многих часов после смерти человека (С. В. Андреев, 1955).
38 |
39 |
|
