
- •ГБОУ ВПО УГМУ Минздрава РФ Кафедра биохимии
- •план
- •1.Оксигеназный путь использования О2
- •Токсичные метаболиты – вещества, участвующие в метаболизме и токсичные в высоких концентрациях.
- •Классификация загрязнителей продовольственного сырья и продуктов питания:
- •Биотрансформация
- •Локализация биотрансформации
- •Виды биотрансформации
- •Пути биотрансформации в организме
- •Монооксигеназные реакции:
- •1.Микросомальные монооксигеназные системы
- ••Открыто 150 генов, кодирующих различные изоформы цитохрома Р450 у животных, растений, грибов и
- •Б. Цепь НАДН2-цитохром b5 редуктаза – Цитохром b5 – стеароил-КоА-десатураза
- •Биологическая роль микросомального окисления:
- •2. Митохондриальные монооксигеназные системы
- •Факторы, влияющие на активность ферментов биотрансформации
- •Диоксигеназные реакции
- •L-триптофандиоксигеназа печени, содержит гем, участвует в катаболизме триптофана:
- •ПЕРОКСИДАЗНЫЙ И РАДИКАЛЬНЫЙ ПУТИ ИСПОЛЬЗОВАНИЯ КИСЛОРОДА
- •Образование АФК
- •Основная часть АФК образуются в
- •Неферментативные реакции образования АФК
- •Ферментативные реакции образования АФК
- •Первичные радикалы
- •Вторичные радикалы
- •Использование АФК в организме
- •Повреждающее действие АФК в организме
- •Субстраты ПОЛ – полиненасыщенные ЖК
- •РЕАКЦИИ П О Л
- •Схема развития оксидативного стресса в митохондриях
- •Антиоксидантная защита
- •АНТИОКИСЛИТЕЛЬНЫЕ
- •пероксидазы
- ••Фосфолипаза в мембране отщепляет от фосфолипидов окисленные жирные кислоты, содержащие гидроперекисную группу (ROOH),
- •Неферментативная антиоксидантная система
- •Токоферол (верх) и синтетический АО ионол (низ)
- •Антирадикальный механизм действия витамина Е
- •Антиоксиданты крови и цитоплазмы
- ••Глутатион- восстановает пероксиды
- •Спасибо за внимание!

Схема развития оксидативного стресса в митохондриях
Активация процессов ПОЛ
Снижение |
|
Повреждение |
АОЗ |
|
мембранных структур |
|
|
|
Дефицит восстановленных |
|
Разобщение окисления |
коферментов НАДН2, ФАДН2 |
|
и фосфорилирования |
Дефицит энергии
Антиоксидантная защита
•В нормальных условиях процесс СРО находится под строгим контролем ферментативных и неферментативных систем клетки, от чего скорость его невелика.
•Химические соединения и физические воздействия, влияющие на скорость СРО, делят на прооксиданты и антиоксиданты
•Прооксиданты усиливают процессы СРО. Это высокие концентрации кислорода (например, при длительной гипербарической оксигенации больного), ферментные системы, генерирующие супероксидные радикалы (например, ксантиноксидаза, ферменты плазматической мембраны фагоцитов и др.), ионы двухвалентного железа.
•Антиоксиданты тормозят СРО. Антиоксиданты, находящиеся в организме, образуют его ферментативную и неферментативную антиоксидантную систему
АНТИОКИСЛИТЕЛЬНЫЕ
ФЕРМЕНТЫ
Супероксиддисмутаза (СОД)
О*2 + О*-2 + 2Н+ → Н2О2 + О2
Каталаза
2Н2О2 → 2Н2О + О2
пероксидазы
Пероксидаза
Н2О2 + НО-S-ОН → 2Н2О + О= S=О
Глутатионпероксидаза (Se )
2GSH + ROOH → GSSG + ROH+ Н2О
(Удаляет пероксид водорода, гидроперекиси липидов)
Глутатионредуктаза
GSSG + НАДФН + Н+ →2GSH + НАДФ+
(Восстанавливает окисленный глутатион)
•Фосфолипаза в мембране отщепляет от фосфолипидов окисленные жирные кислоты, содержащие гидроперекисную группу (ROOH), тем самым разрушаются гидроперекиси липидов, предотвращается разветвление цепей окисления липидов в мембранах.

Неферментативная антиоксидантная система
|
CH2OH |
|
|
|
|
|
|
|
|
|
CH OH |
|
|
|
|
|
|
|
||||||||
|
|
CHOH |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
O |
|
- 2H |
|
|
|
CHOH |
O |
|||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
+2H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
OH |
|
|
|
|
|
|
|
|
O |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||||
Àñê î ðáè í î âàÿ ê -òà |
|
Äåãè äðî àñê î ðáè í î âàÿ ê -òà |
||||||||||||||||||||||||
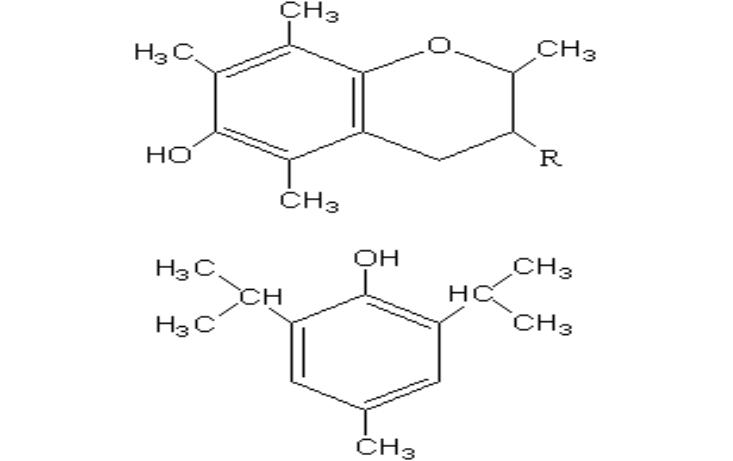
Токоферол (верх) и синтетический АО ионол (низ)

Антирадикальный механизм действия витамина Е
CH3 |
ROO |
ROOH |
|
HO |
|||
|
O |
||
|
CH3 |
|
|
H3C |
O Фитил |
H C |
|
|
|
3 |
|
CH3 |
Í Î -àñêî ðáàò-Î |
Í Î -àñêî ðáàò-Î Í |
Òî êî ôåðî ë
|
CH3 |
|
|
|
O |
|
ROO |
ROOH |
O |
|
CH3 |
|
|
|
H C |
O Фитил |
H2O |
|
H3C |
3 |
|
|
|
|
|
|
|
|
CH3
То ко ф ерилрадикал
CH3
 CH3
CH3
O Фитил
CH3
То ко ф ерилрадикал
CH3
 CH3
CH3
O Фитил
OH
CH3
Òî êî ô åðî ëõèí î í
Антиоксиданты крови и цитоплазмы
•Церулоплазмин (плазма крови) - окисляет Fe2+ до Fe3+ молекулярным кислородом
•Апо-белок трансферрина (плазма крови) - связывает Fe3+
•Ферритин (цитоплазма)- окисляет Fe2+ и депонирует Fe3+
•Карнозин - связывает Fe2+
•Глутатион- восстановает пероксиды
•Аскорбиновая кислота - регенерирует окисленные токоферол и убихинон
•Глутатионредуктаза - восстанавливает окисленный глутатион
