Метаболизм гема и обмен железа. Л.
Содержание железа (Fe) в организме:
~25% в запасной форме (в комплексе с ферритином) – селезенка, красный костный мозг, печень
Hb~65%
Mb + др. внутриклеточные гемопротеины ~1%
0,1% в плазме крови
Суточная норма поступления железа : ~10 мкг у мужчин,
~20 мкг у женщин (репродуктивного возраста),
до 50 мкг – у женщин во время беременности и лактации.
Пищеварение.
В желудке под воздействием HCl – Fe- высвобождается из пищевой массы. В тонком кищечнике ~15% пищевого Fe2+ всасывается. В основном, железо пищи 3х-валентное, а под воздействием HCl и аскорбиновой кислоты превращается в 2х-валентное. (Fe мясных продуктов - «2+», в других случаях – «3+»). Фитиновая кислота (сухие завтраки), кофеин, танин(чай), фосфаты, оксалаты образуют нерастворимые комплексы с Fe.
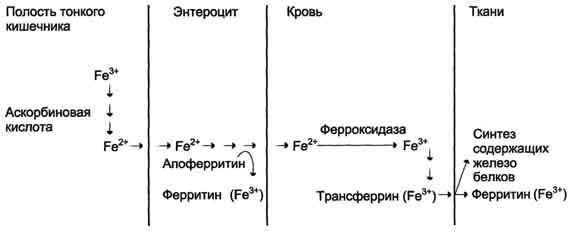
Поступление экзогенного железа в ткани. В полости кишечника железо освобождается из белков и солей органических кислот пищи. Усвоению железа способствует аскорбиновая кислота, восстанавливающая железо. В клетках слизистой оболочки кишечника избыток поступившего железа соединяется с белком апоферритином с образованием ферритина, при этом ферритин окисляет Fe2+ в Fe3+. Поступление железа из клеток слизистой оболочки кишечника в кровь сопровождается окислением железа ферментом сыворотки крови ферроксидазой. В крови Fe3+ транспортирует белок сыворотки крови трансферрин. В тканях Fe2+ используется для синтеза железосодержащих белков или депонируется в ферритине.
Метаболизм железа.
После всасывания Fe откладывается в клетках кишечника в составе ферритина или сразу попадает в кровоток в комплексе с трансферрином, переносится в клетки печени, красного костного мозга, где связываются с ферритином. Вне связи с белками железо токсично, запускает свободно-радикальные реакции с образованием активных форм O2.
Поступление Fe с пищей 10-20 мг/сутки
Всасывание в кишечник 1-2 мг/сутки
Ферритин кишечника Трансферин
Ферритин печени образование Hb Др. потребности - 10-20%
и др.5 – 15% в кр.костн.мозге 75%
Выведение железа из организма: до 1-2 мг/сутки:
С желчью
Эпителий ЖКТ
Кровотечение
Выпадение волос
Железосодержащие белки
Гем является небелковой частью:
Гемопротеинов:
Hb – до 85% общего количества гема организма (эритроциты (RBS-red blood cells) и клетки красного костного мозга),
Mb – до 17% в скелетных мышцах и миокарде,
Цитохромы дыхательной системы и P4SO –до 1%:
- цитохромокидаза
- гомогентизатоксидаза
- пероксидаза
- миелопероксидаза
- каталаза
- тиреопероксидаза
II) железофлавопротеинов:
цитохром – с –редуктаза
сукцинатдегидрогеназа
НАДФ-оксидаза (в гранулоцитах)
ацетил-SКОА-дегидрогеназа
ксантиноксидаза
пролил-гидроксиназа
III) железосвязывающие белки:
трансферрин
ферритин
гемосидерин
Синтез гемоглобина:
Протекает в предшеств. RBC, клетках печени, почек, слизистой кишечника и т.д.
Происходит в митохондриях (первая реакция), и цитозоле (вторая реакция):
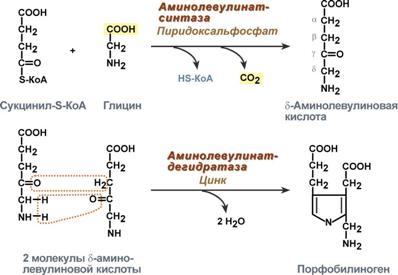
Третья реакция: 4 молекулы порфобилиногена конденсируются в тетрапиррол
4 молекулы порфобилиногена
Первый путь. Ферменты:
уропорфириноген-1-синтаза, Второй путь. Копропорфириноген 1
уропорфириноген-3-косинтаза
уропорфириноген 3
декарбоксилаза (-CO2)
копропорфириноген 3
оксидаза
протопорфириноген 9
оксидаза
протопорфирин 9
Fe2+
Гем
Регуляция:
скорость синтеза глобинов зависит от наличия гема
Основной регуляторный фермент – аминолевулинат-синтаза, при этом необходимо достаточное количество Fe
Положительная регуляция: гипоксия тканей индуцирует синтез фермента
В печени стероиды и жирорастворимые токсины усиливают работу системы и активность фермента
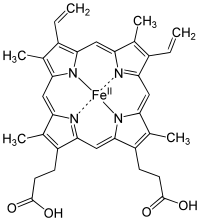
Формулы: гем протопорфирин 9
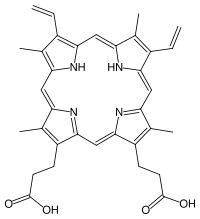
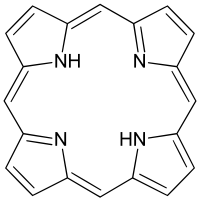 порфин
порфин
Распад гема:
За сутки распадается около 9гр. гемопротеинов, в основном Hb из RBC(время жизни 120 суток).
При разрушении RBC в кровяном русле Hb образует комплекс с белком переносчиком гаптоглобином (фракция α2- глобулинов крови) и переносится в клетки ретикуло-эндотелиальный системы (РЭС) селезенки, печени и красного костного мозга, где гем (в составе гемоглобина) окисляется молекул.O2. В реакциях последовательно происходит разрыв мостика между 1 и 2 пирольными кольцами с их восстановлением, отщепление Fe и белковой части, и образованием оранжевого пигмента – билирубина

М - (-СН3) - метильная группа; В - (-СН=СН2) - винильная группа;
П - (-CH2-CH2-COOH) - остаток пропионовой кислоты.
Неконъюгированный билирубин токсичный, оранжевого цвета, гидрофобный, липофильный неконъюгированный билирубин, легко растворяясь в липидах мембраны и проникая вследствие этого в митохондрии, разобщает в них дыхание и окислительное фосфорилирование, нарушает синтез белка, поток ионов калия через мембрану клетки и органелл. Это отрицательно сказывается а состоянии ЦНС, вызывая у больных ряд характерных неврологических симптомов.
Выведение билирубина:
Из клеток РЭС билирубин попадает в кровь. Здесь он находится в комплексе с альбумином плазмы и в меньшем количестве: с металлами, аминокислотами, пептидами и др. малыми молекулами. Образование таких комплексов не позволяет выделяться билирубину с мочой.
Билирубин в комплексе с альбумином называется свободным( неконьюгированным) или непрямым билирубином.
Из сосудистого русла в гепатоциты билирубин попадает с помощью белка-переносчика лигандина.
Конъюгация билирубина в гладком ЭР
В гладком ЭР гепатоцитов к билирубину присоединяются (реакция конъюгации) полярные группы, главным образом от глюкуроновой кислоты. Кроме глюкуроновой кислоты в реакцию могут вступать сульфаты, фосфаты, глюкозиды. Билирубин имеет 2 карбоксильные группы, поэтому может соединяться с 2 молекулами глюкуроновой кислоты, образуя хорошо растворимый в воде конъюгат - диглюкуронид билирубина (конъюгированный, или прямой, билирубин).
Билирубин – глюкоуронид получил название связанный(коньюгированный) или прямой билирубин.
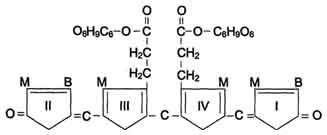
Структура билирубиндиглюкуронида (конъюгированный, "прямой" билирубин). Глюкуроновая кислота присоединяется эфирной связью к двум остаткам пропионовой кислоты с образованием ацилглюкуронида.
Донором глюкуроновой кислоты служит УДФ-глюкуронат. Специфические ферменты, УДФ-глюкуронилтрансферазы (уридиндифосфоглюкуронилтрансферазы) катализируют образование моно- и диглюкуронидов билирубина. Индукторами синтеза УДФ-глюкуронилтрансфераз служат некоторые лекарственные препараты, например, фенобарбитал.

Секреция билирубина в жёлчь
Секреция конъюгированного билирубина в жёлчь идёт по механизму активного транспорта, т.е. против градиента концентрации. Активный транспорт является, вероятно, скорость-лимитирующей стадией всего процесса метаболизма билирубина в печени. В норме диглюкуронид билирубина - главная форма экскреции билирубина в жёлчь, однако не исключается присутствие небольшого количества моноглюкуронида. Транспорт конъюгированного билирубина из печени в жёлчь активируется теми же лекарствами, которые способны индуцировать конъюгацию билирубина. Таким образом, можно сказать, что скорость конъюгации билирубина и активный транспорт билирубинглюкуронида из гепатоцитов в жёлчь строго взаимосвязаны
После образования билирубин-глюкоурониды АТФ-зависимым переносчиком секретируются в желчные протоки и далее в кишечник, где при участии бактериальной β-глюкуронидазы превращаются в свободный билирубин .
Одновременно некоторое количество билирубин-глюкуронидов может попадать из желчи в кровь по межклеточным щелям. Т.о., в крови в норме имеется свободный билирубин (из РЭС, 80%) и связанный билирубин (из желчных протоков, 20%).
Превращение в кишечнике:
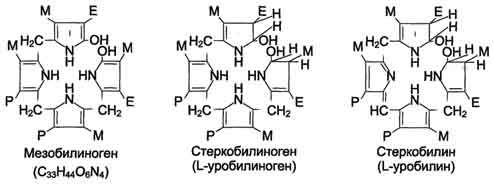
Билирубин восстанавливается под действием микрофлоры до мезобилирубина и мезобилирубиногена (уробилиногена). Из них часть всасывается и с током крови вновь попадает в печень, где окисляется до ди- и три – пироллов. Мезобилирубин и уробилиноген задерживаются гепатоцитами, не попадая в кровь и мочу. Оставшаяся в кишечнике часть пигментов ферментами бактериальной флоры толстого кишечника восстанавливается до стеркобилиногена и выделяется из организма, окрашивая кал.
Незначительное количество стеркобилиногена через геморроидальные вены попадает в большой круг кровообращения, далее в почки и выделяется с мочой. На воздухе стеркобилиноген и уробилиноген превращаются, соответственно в стеркобилин и уробилин.
Токсичность билирубина состоит в его липофильности, ситуации при которых в крови накапливается билирубин, в зависимости от причин деляться на 3 вида:
Гемолитическая – в результате гомолиза при избыточном превращении Hb в билирубин
Печеночно-клеточные – печень не в состоянии «обезвредить» билирубин
Механические – билирубин не может попасть из печени в кишечник из-за механического перекрытия желчевыводящих путей.
Накопление билирубина более 43 мкммоль/л ведет к связыванию его эластичныи волокнами кожи и конъюктивы, что проявляется в виде желтух. Т.к. свободный билирубин липофилен, то он легко накапливается в подкожном жире и нервной ткани. Это опасно для детей, особенно для новорожденных.
Катаболизм билирубин-диглюкуронида.
В кишечнике поступившие билирубинглюкурониды гидролизуются специфическими бактериальными ерментами β-глюкуронидазами, которые гидролизуют связь между билирубином и остатком глюкуроновой кислоты. Освободившийся в ходе этой реакции билирубин под действием кишечной микрофлоры восстанавливается с образованием группы бесцветных тетрапиррольных соединений – уробилиногенов.
В подвздошной и толстой кишках небольшая часть уробилиногенов снова всасывается, попадает с кровью воротной вены в печеНb. Основная часть уробилиногена из печени в составе жёлчи выводится в кишечник и выделяется с фекалиями из организма, часть уробилиногена из печени поступает в кровь и удаляется с мочой в форме уробилина. В норме большая часть бесцветных уробилиногенов, образующихся в толстой кишке, под действием кишечной микрофлоры окисляется в прямой кишке до пигмента коричневого цвета уробилина и удаляется с фекалиями. Цвет фекалий обусловлен присутствием уробилина.
Структура некоторых жёлчных пигментов. Мезобилиноген - промежуточный продукт катаболизма билирубина в кишечнике.