

Строение и обмен углеводов |
200 |
|
|
8. Активная фосфорилаза "а" гликогена расщепляет α1,4-гликозидные связи в гликогене с образованием глюкозо-1-фосфата.
Кроме гормонов, влияющих на активность аденилатциклазы через G-белки, существуют иные способы регуляции этого механизма. Например, после воздействия инсулина активируется фермент фосфодиэстераза, которая гидролизует цАМФ и, следовательно, ликвидирует развитие аденилатциклазного механизма действия глюкагона и адреналина, со всеми вытекающими последствиями.
Кальций-зависимая активация
Активация ионами кальция заключается в активации киназы фосфорилазы не протеинкиназой, а ионами Ca2+ и кальмодулином. Этот путь работает при инициации кальцийфосфолипидного механизма (см "Гормоны") либо при отсутсвии стимуляции аденилатциклазы. Это оправдывает себя, например, в мышцах при умеренной нагрузке, когда влияние адреналина через аденилатциклазу еще не произошло или недостаточно, но в цитоплазму под влиянием нервных импульсов поступают ионы Ca2+.
Аллостерическая активация
Также существует активация фосфорилазы гликогена с помощью АМФ – аллостерическая активация благодаря присоединению АМФ к молекуле фосфорилазы "b". Способ работает в любой клетке – при увеличении расхода АТФ и накоплении продуктов его распада АДФ и АМФ.
ГЛИК ОГЕ НО ВЫ Е БОЛЕ ЗН И
Это наследственные заболевания, обусловленные недостаточностью каких-либо ферментов, отвечающих за метаболизм гликогена. Средняя частота встречаемости составляет
1:40000.
ГЛИК ОГЕНОЗЫ
Синдром гликогеноза возникает в результате дефекта фермента синтеза или мобилизации гликогена, что приводит к накоплению или изменению структуры гликогена в разных тканях, чаще в печени и мышцах. В настоящее время гликогенозы делят по патогенетиче-
скому признаку на печеночные, мышечные и смешанные формы.
Всего существует 12 типов гликогенозов. По патогенетическому признаку гликогенозы делят:
•печеночные – 0, I, III, IV, VI, VIII, IX, Х, ХI типов,
•мышечные – V и VII типов,
•смешанные – II типа.

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
201 |
|
|
|
Печеночные гликогенозы
Гликогеноз I типа или болезнь фон Гирке обусловлен аутосомно-рецессивным дефектом глюкозо-6-фосфатазы. Из-за того, что этот фермент есть только в печени и почках, преимущественно страдают эти органы, и болезнь носит еще одно название – гепаторенальный гликогеноз. Даже у новорожденных детей наблюдаются гепатомегалия и нефромегалия, обусловленные накоплением гликогена не только в цитоплазме, но и в ядрах клеток. Кроме этого, активируется синтез липидов с возникновением стеатоза печени. Так как фермент необходим для дефосфорилирования глюкозо-6-фосфата с последующим выходом глюкозы в кровь, у больных отмечается гипогликемия, и, как следствие, ацетонемия, метаболический ацидоз, ацетонурия.
Гликогеноз III типа или болезнь Форбса-Кори или лимит-декстриноз – это ауто-
сомно-рецессивный дефект амило-α1,6-глюкозидазы, "деветвящего" фермента, гидролизующего α1,6-гликозидную связь. Болезнь имеет более доброкачественное течение, и частота ее составляет примерно 25% от всех гликогенозов. Для больных характерна гепатомегалия, умеренная задержка физического развития, в подростковом возрасте возможна небольшая миопатия.
При гликогенозе IV типа (болезнь Андерсена, 1% всех гликогенозов), связанного с дефектом ветвящего фермента, образуется гликоген с короткими цепочками и резко уменьшается скорость гликогенолиза.
Гликогеноз VI типа (болезнь Херса, 25% всех гликогенозов), связан с дефицитом печеночной фосфорилазы гликогена. При этом отсутствует мобилизация гликогена, развивается гепатомегалия и гипогликемия.
Мышечные гликогенозы
Для этой группы гликогенозов характерны изменения ферментов мышечной ткани. Это приводит к нарушению энергообеспечения мышц при физической нагрузке, к болям в мышцах, судорогам.
Гликогеноз V типа (болезнь Мак-Ардля, 1% всех гликогенозов) – отсутствие мышечной фосфорилазы. При тяжелой мышечной нагрузке возникают судороги, миоглобинурия, хотя легкая работа не вызывает каких-либо проблем.

Строение и обмен углеводов |
202 |
|
|
Смешанные гликогенозы
Эти заболевания касаются и печени, и мышц, и других органов.
Гликогеноз II типа (болезнь Помпе, 10% всех гликогенозов) – поражаются все гликогенсодержащие клетки из-за отсутствия лизосомальной α1,4-глюкозидазы. Происходит накопление гликогена в лизосомах и в цитоплазме. Заболевание является наиболее злокачественным. Больные умирают в грудном возрасте из-за кардиомегалии и тяжелой сердечной недостаточности.
АГ ЛИК ОГЕНОЗЫ
Агликогенозы – состояния, связанные с отсутствием гликогена.
В качестве примера агликогеноза можно привести наследственный аутосомнорецессивный дефицит гликоген-синтазы. Симптомами является резкая гипогликемия натощак, особенно утром, появляется рвота, судороги, потеря сознания. В результате гипогликемии наблюдается задержка психомоторного развития, умственная отсталость. Болезнь несмертельна при адекватном лечении (частое кормление), хотя и опасна.
ОК ИСЛЕ Н ИЕ ГЛЮК ОЗЫ
Окисление глюкозы в клетках происходит по двум направлениям:
1.Окисление с образованием пентоз: рибозы, рибулозы, ксилулозы. Этот путь называется пентозофосфатный шунт и не связан с получением энергии
2.Окисление с образованием пировиноградной кислоты (пирувата) и получением энергии. Второй путь, по которому глюкоза окисляется до пировиноградной кислоты, называет-
ся гликолизом. В зависимости от дальнейшей судьбы пирувата различают аэробное и анаэробное окисление глюкозы. Целью аэробного и анаэробного путей окисления глюкозы является получение АТФ.
Ваэробном процессе пировиноградная кислота превращается в ацетил-SКоА и далее
сгорает в реакциях тканевого дыхания до СО2 и Н2О. Вместе с этим, существенное значение также имеет способность пирувата карбоксилироваться в оксалоацетат (см "Регуляция ЦТК"), особенно эта реакция активна в печени. Наличие избытка оксалоацетата "подталкивает" реакции ЦТК, ускоряет связывание ацетильной группы, ее окисление и синтез АТФ.
Ванаэробном процессе пировиноградная кис-
лота восстанавливается до молочной кислоты (лактата), поэтому в микробиологии анаэробный гликолиз называют молочнокислым брожением. Лактат является метаболическим тупиком и далее ни во что не превращается, единственная возможность утилизовать лактат – это окислить его обратно в пируват.
Многие клетки организма способны к анаэробному окислению глюкозы. Для эритроцитов он является единственным источником энергии. Клетки скелетной мускулатуры за счет бескислородного
расщепления глюкозы выполняют мощную, быструю, интенсивную с предельным напряжением, работу (до 60 секунд), как, например, бег на короткие дистанции, напряжение в силовых видах спорта. Также анаэробное окисление глюкозы усиливается при нарушении работы митохондрий (митохондриальные болезни, гиповитаминозы В1, В2, В3, В5), во время гипоксии клеток при различных анемиях, при нарушении кровообращения в тканях и при заболеваниях бронхолегочной системы.

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
203 |
Г Л И К О Л И З
Анаэробное превращение глюкозы локализуется в цитозоле и включает 2 этапа из 11 ферментативных реакций (см стр.226).
Суммарное уравнение анаэробного гликолиза имеет вид:
Глюкоза + 2 АДФ + 2 Фн 2 Лактат + 2 АТФ + 2 H2O
Первый этап гликолиза
Первый этап гликолиза (греч. glykos — сладкий и греч. lysis — растворение) – подготовительный, здесь происходит затрата энергии АТФ, активация глюкозы и образование из нее триозофосфатов.
Первая реакция гликолиза сводится к превращению глюкозы в реакционноспособное соединение за счет фосфорилирования 6-го, не включенного в кольцо, атома углерода. Эта реакция является первой в любом превращении глюкозы, катализируется гексокиназой.
Вторая реакция необходима для выведения еще одного атома углерода из кольца для его последующего фосфорилирования (фермент изомераза). В результате образуется фрук- тозо-6-фосфат.
Третья реакция – фермент фосфофруктокиназа фосфорилирует фруктозо-6-фосфат с образованием почти симметричной молекулы фруктозо-1,6-дифосфата.
В четвертой реакции фруктозо-1,6-дифосфат разрезается пополам альдолазой с образованием двух фосфорилированных триоз-изомеров – альдозы глицеральдегида (ГАФ) и кетозы диоксиацетона (ДАФ).
Пятая реакция подготовительного этапа – переход глицеральдегидфосфата и диоксиацетонфосфата друг в друга при участии триозофосфатизомеразы. Равновесие реакции сдвинуто в пользу диоксиацетонфосфата, его доля составляет 97%, доля глицеральдегидфосфата – 3%. Эта реакция, при всей ее простоте, определяет дальнейшую судьбу глюкозы:
oпри нехватке энергии в клетке и активации окисления глюкозы диоксиацетонфосфат превращается в глицеральдегидфосфат, который далее окисляется на втором этапе гли-
колиза,
oпри достаточном количестве АТФ, наоборот, глицеральдегидфосфат изомеризуется в диоксиацетонфосфат, и последний отправляется на синтез жиров (см "Синтез триацилглицеролов").
Второй этап гликолиза
Второй этап гликолиза – это освобождение энергии, содержащейся в глицеральдегидфосфате, и запасание ее в форме АТФ.
Шестая реакция гликолиза (фермент глицеральдегидфосфат-дегидрогеназа) – окис-
ление глицеральдегидфосфата и присоединение к нему фосфорной кислоты приводит к образованию макроэргического соединения 1,3-дифосфоглицериновой кислоты и НАДН.
В седьмой реакции (фермент фосфоглицераткиназа) энергия фосфоэфирной связи,
заключенная в 1,3-дифосфоглицерате тратится на образование АТФ. Реакция получила дополнительное название – реакция субстратного фосфорилирования, что уточняет источник энергии для получения макроэргической связи в АТФ (субстрат) в отличие от окислительного фосфорилирования (электрохимический градиент ионов водорода на мембране митохондрий).
Восьмая реакция – синтезированный в предыдущей реакции 3-фосфоглицерат под влиянием фосфоглицератмутазы изомеризуется в 2-фосфоглицерат.
Девятая реакция – фермент енолаза отрывает молекулу воды от 2-фосфо– глицериновой кислоты и приводит к образованию макроэргической фосфоэфирной связи в составе фосфоенолпирувата.

Строение и обмен углеводов |
204 |
|
|
Десятая реакция гликолиза – еще одна реакция субстратного фосфорилирования --
заключается в переносе пируваткиназой макроэргического фосфата с фосфоенолпирувата на АДФ и образовании пировиноградной кислоты.

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
205 |
|
|
|
Последняя реакция бескислородного окисления глюкозы, одиннадцатая – образование молочной кислоты из пирувата под действием лактатдегидрогеназы. Важно то, что эта реакция осуществляется только в анаэробных условиях. Эта реакция необходима клетке, так как НАДН, образующийся в 6-й реакции, в отсутствие кислорода не может окисляться в митохондриях. У плода и детей первых месяцев жизни преобладает анаэробный распад глюкозы, в связи с чем уровень лактата у них выше по сравнению со взрослыми.
При наличии кислорода пировиноградная кислота переходит в митохондрию и превращается в ацетил-SКоА.
ГЛ И К О Л И Т И Ч Е С К А Я О К С И Д О Р Е Д У К Ц И Я
Ванаэробных условиях образуемый в шестой, ГАФ-дегидрогеназной реакции, НАДН используется в одиннадцатой реакции для восстановления пирувата до лактата. Образуемый этим образом НАД опять возвращается в шестую реакцию. Процесс циклического восстановления и окисления НАД в реакциях анаэробного окисления глюкозы получил название
гликолитическая оксидоредукция.
Ваэробных условиях гликолитической о ксидоредукции не происходит, НАДН отдает свои атомы водорода на челночные системы (см ниже) для их передачи в дыхательную цепь митохондрий.
Э Ф Ф Е К Т П А С Т Е Р А
Эффект Пастера – это снижение потребления глюкозы и прекращение продукции молочной кислоты клеткой в присутствии кислорода.
Биохимическая основа эффекта Пастера заключается в конкуренции между пируватдегидрогеназой, превращающей пируват в ацетил-SКоА, и лактатдегидрогеназой, превращающей пируват в лактат.
При отсутствии кислорода реакции окислительного фосфорилирования не идут, моментально накапливающийся НАДН тормозит ЦТК и ПВК-дегидрогеназу, ацетил-SКоА, не попадающий в ЦТК, также ингибирует ПВК-дегидрогеназу. В этой ситуации пировиноградной кислоте не остается ничего иного как под влиянием ЛДГ превращаться в молочную.
При наличии кислорода ингибирование ПВК-дегидрогеназы прекращается и она, обладая большим сродством к пирувату, выигрывает конкуренцию.

Строение и обмен углеводов |
206 |
|
|
Ч Е Л Н О Ч Н Ы Е С И С Т Е М Ы
Молекулы НАДН, образованные в шестой реакции гликолиза, в зависимости от наличия кислорода имеют, как минимум, два пути дальнейшего использования:
o либо остаться в цитозоле и вступить в лактатдегидрогеназную реакцию (анаэробные условия),
o либо проникнуть в митохондрию и окислиться в дыхательной цепи (аэробные условия), Так как сама молекула НАДН через митохондриальную мембрану не проходит, то существуют системы, принимающие от нее атомы водорода в цитоплазме и отдающие их в
матриксе митохондрий. Такие системы называются челночными.
Определены две основные челночные системы – глицеролфосфатная и малат-
аспартатная.
Глицеролфосфатный челночный механизм
Ключевыми ферментами глицеролфосфатного челнока являются изоферменты глице- рол-3-фосфат-дегидрогеназы – цитоплазматический и митохондриальный. Они отличаются своими коферментами: у цитоплазматической формы – НАД, у митохондриальной – ФАД.
В цитозоле метаболиты гликолиза – диоксиацетонфосфат и НАДН образуют глицерол- 3-фосфат, поступающий в матрикс митохондрий. Там он окисляется с образованием ФАДН2. Далее ФАДН2 направляется в дыхательную цепь и используется для получения энергии.

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
207 |
|
|
|
Работа глицеролфосфатного челночного механизма актуальна при необходимости получить энергию из глюкозы при работе клетки. Однако в гепатоците и адипоците в состоянии покоя и после еды глицерол-3 фосфат будет использоваться в цитозоле для синтеза жиров (см "Синтез триацилглицеролов").
Малат-аспартатный челночный механизм
Этот механизм более сложен. Постоянно идущая в цитоплазме реакция трансаминирования аспартата с α-кетоглутаратом превращает его в оксалоацетат, который под действием цитозольного пула малатдегидрогеназы и "гликолитического" НАДН восстанавливается до яблочной кислоты. Последняя антипортом с α-кетоглутаратом проникает в митохондрии и, являясь метаболитом ЦТК, окисляется в оксалоацетат с образованием НАДН. Так как мембрана митохондрий непроницаема для оксалоацетата, то оксалоацетат вступает в реакцию трансаминирования с глутаминовой кислотой и превращается в аспарагиновую кислоту. Последняя, при участии соответствующей транслоказы, в обмен на глутамат выходит в цитозоль и снова вовлекается в трансаминирование.
Расчет энергетической ценности и коэффициента Р/О при окислении глюкозы
Для расчета количества АТФ, образованной при окислении глюкозы необходимо знать: o реакции, идущие с затратой или образованием АТФ и ГТФ,
o реакции, продуцирующие НАДН и ФАДН2 и использующие их,
oтак как глюкоза образует две триозы, то все соединения, образующиеся ниже ГАФдегидрогеназной реакции, образуются в двойном (относительно глюкозы) количестве.
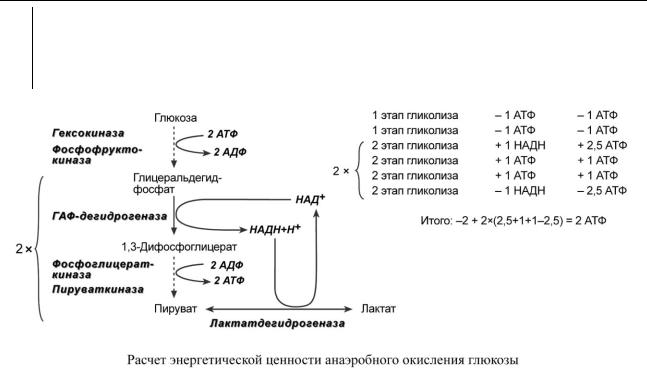
Анаэробное окисление
На подготовительном этапе на активацию глюкозы затрачивается 2 молекулы АТФ, фосфат каждой из которых оказывается на триозе – глицеральдегидфосфате и диоксиацетонфосфате. В следующий второй этап входят две молекулы глицеральдегидфосфата, каждая из которых окисляется до пирувата с образованием 2-х молекул АТФ в седьмой и десятой реакциях – реакциях субстратного фосфорилирования. Таким образом, суммируя, получаем, что на пути от глюкозы до пирувата в чистом виде образуется 2 молекулы АТФ.
Строение и обмен углеводов |
208 |
Ранее при расчете эффективности окисления коэффициент P/O для НАДH принимался равным 3,0, для ФАДH2 – 2,0.
По современным данным значение коэффициента P/O для НАДH соответствует
2,5, для ФАДH2 – 1,5.
Однако надо иметь в виду и шестую, глицеральдегидфосфат-дегидрогеназную, реакцию, из которой выходит НАДН. Если условия анаэробные, то он используется в лактатдегидрогеназной реакции, где окисляется для образования лактата и в получении АТФ не участвует.
Аэробное окисление
Если в клетке имеется кислород, то молекула НАДН из шестой реакции гликолиза направляется в митохондрию, на процессы окислительного фосфорилирования. Там его окисление приносит дивиденды в виде 2,5 молей АТФ.
Образовавшийся в гликолизе пируват в аэробных условиях превращается в ПВК-дегидрогеназном комплексе в ацетил-SКоА, при этом образуется 1 молекула НАДН (2,5 моля АТФ).
Ацетил-SКоА вовлекается в ЦТК и, окисляясь, дает 3 молекулы НАДН, 1 молекулу ФАДН2, 1 молекулу ГТФ. Молекулы НАДН и ФАДН2 движутся в дыхательную цепь, где при их окислении в сумме образуется 9 молекул АТФ. В целом при сгорании одной ацетогруппы в ЦТК образуется 10 молекул АТФ.
Суммируя результаты окисления "гликолитического" и "пируватдегидрогеназного" НАДН, "гликолитический" АТФ, энергетический выход ЦТК и умножая все на 2, получаем
32 молекулы АТФ.
Для расчета коэффициента P/O (см "Окислительное фосфорилирование/Коэффициент P/O") подсчитываем
oколичество АТФ образованного в митохондриях АТФ-синтазой – это соответствует значению P,
oколичество НАДН и ФАДН2, поступивших в дыхательную цепь – это значение соответствует числу восстановленных атомов кислорода (O), включенных в молекулу воды.
После расчетов получаем P=28 и O=12. Таким образом, величина P/O для аэробного
окисления глюкозы равна 2,33.
Общее уравнение аэробного окисления глюкозы имеет вид:
C6H12O6 + 6 O2 + 32 АДФ + 32 Фн 6 CO2 + 44 H2О + 32 АТФ

biokhimija.ru |
Тимин О.А. Лекции по общей биохимии (2018г) |
209 |
|
|
|
ГЛ Ю К О Н Е О Г Е Н Е З
Вклетках организма всегда существует потребность в глюкозе:
o для эритроцитов глюкоза является единственным источником энергии,
oнервная ткань потребляет около 120 г глюкозы в сутки, что составляет до 70% глюкозы образующейся в печени, притом эта величина практически не зависит от интенсивности ее работы. Только в экстремальных ситуациях (длительное голодание) она способна получать энергию из неуглеводных источников (из кетоновых тел),
oглюкоза играет весомую роль для поддержания необходимых концентраций метаболитов цикла трикарбоновых кислот (в первую очередь оксалоацетата).
Таким образом, при определенных ситуациях – при низком содержании углеводов в
пище, голодании, длительной физической работе – организм должен иметь возможность получить глюкозу. Это достигается процессом глюконеогенеза.
Глюконеогенез – это синтез глюкозы из неуглеводных компонентов: лактата, пирувата, глицерола, кетокислот цикла Кребса и других кетокислот, из аминокислот. Процесс включает все обратимые реакции гликолиза, и особые обходные пути, т.е. он не полно-
стью повторяет реакции окисления глюкозы. Его реакции проходят во всех тканях, кроме последней глюкозо-6-фосфатазной реакции, которая может идти только в печени и почках. Поэтому, строго говоря, глюконеогенез идет только в этих двух органах.
Как указывалось, в гликолизе существуют три необратимые реакции: пируваткиназ-
ная (десятая), фосфофруктокиназная (третья) и гексокиназная (первая). На этих реакциях существуют энергетические барьеры, которые при глюконеогенезе обходятся с помощью дополнительных реакций.
