
- •Введение
- •Тема 1. Кристаллическое строение металлов и его влияние на механические свойства. Полиморфизм. Дефекты в кристаллах, теоретическая прочность.
- •1.1 Кристаллическое строение металлов и его влияние на механические свойства.
- •1.2 Дефекты в кристаллах, теоретическая прочность.
- •Тема 2. Наклеп и рекристаллизация металлов.
- •2.1. Явление наклепа в металлах.
- •2.2. Влияние нагрева на структуру и свойства деформированного металла. Возврат и рекристаллизация.
- •Тема 3 Строение сплавов
- •3.1. Типы сплавов
- •3.2. Диаграммы состояния сплавов.
- •3.3. Построение диаграммы состояния.
- •3.4. Правила чтения диаграммы состояния.
- •3.5. Диаграмма для неограниченных твердых растворов.
- •Тема 4 Производство чугуна и стали
- •4.1 Металлургия чугуна
- •Исходные материалы для доменного производства
- •Доменное производство
- •Продукты доменного производства
- •4.2 Металлургия стали
- •Кислородно-конвертерный процесс.
- •Выплавка стали в мартеновских печах
- •Выплавка стали в электропечах
- •Разливка стали в слитки
- •4.3 Кристаллизация стали
- •Строение стального слитка
- •4.4 Методы повышения качества стали
- •Переплавные процессы
- •Внепечная обработка стали («ковшевая металлургия» или «вторичная металлургия»)
- •Тема 5 Система сплавов железо – углерод
- •Превращения при охлаждении стали
- •Влияние содержания углерода на механические свойства сталей.
- •Критические точки в сталях.
- •Хладноломкость стали.
- •Классификация и маркировка углеродистых сталей.
- •Тема 6 Чугуны
- •Графитизация в чугунах.
- •Структура и свойства белых чугунов.
- •Структура и свойства серых чугунов.
- •Ковкие и высокопрочные чугуны.
- •Тема 7 Термическая обработка
- •7.1 Основы термической обработки
- •Параметры термообработки
- •Основные превращения в стали при термической обработке
- •7.2 Технология термической обработки
- •Закалка
- •Поверхностная закалка
- •7.3 Химико-термическая обработка
- •Цементация
- •Азотирование
- •Цианирование
- •Диффузионная металлизация
- •Тема 8 Легированные стали
- •Влияние легирующих элементов на диаграмму Fe - c.
- •Кристаллическое строение легированных сталей.
- •Особенности структурных превращений в легированных сталях.
- •Отпускная хрупкость.
- •Маркировка легированных сталей.
- •Конструкционные стали.
- •Инструментальные стали.
- •Стали со специальными свойствами.
- •Тема 9 Цветные сплавы
- •9.1 Сплавы на основе меди
- •9.2 Сплавы на основе алюминия.
- •9.3 Сплавы на основе титана
- •Тема 10. Неметаллические конструкционные материалы
- •Тема 11. Композиционные материалы.
- •Тема 12. Материалы с особыми электротехническими и магнитными свойствами.
Введение 2
Тема 1. Кристаллическое строение металлов и его влияние на механические свойства. Полиморфизм. Дефекты в кристаллах, теоретическая прочность. 2
1.1 Кристаллическое строение металлов и его влияние на механические свойства. 2
1.2 Дефекты в кристаллах, теоретическая прочность. 7
Тема 2. Наклеп и рекристаллизация металлов. 14
2.1. Явление наклепа в металлах. 14
2.2. Влияние нагрева на структуру и свойства деформированного металла. Возврат и рекристаллизация. 17
Тема 3 Строение сплавов 20
3.1. Типы сплавов 20
3.2. Диаграммы состояния сплавов. 22
3.3. Построение диаграммы состояния. 23
3.4. Правила чтения диаграммы состояния. 24
3.5. Диаграмма для неограниченных твердых растворов. 26
Тема 4 Производство чугуна и стали 27
4.1 Металлургия чугуна 27
4.2 Металлургия стали 32
4.3 Кристаллизация стали 39
4.4 Методы повышения качества стали 42
Тема 5 Система сплавов железо – углерод 46
Тема 6 Чугуны 53
Тема 7 Термическая обработка 57
7.1 Основы термической обработки 57
7.2 Технология термической обработки 65
7.3 Химико-термическая обработка 76
Тема 8 Легированные стали 80
Тема 9 Цветные сплавы 88
9.1 Сплавы на основе меди 88
9.2 Сплавы на основе алюминия. 96
9.3 Сплавы на основе титана 107
Тема 10. Неметаллические конструкционные материалы 113
Введение
Науку о строении и свойствах технических материалов, изучающую связь между составом, строением и свойствами, называют материаловедением.
Используемые в технике металлы принято подразделять на две основные группы — черные и цветные. К черным металлам относят железо и его сплавы (чугун, сталь, ферросплавы). Остальные металлы и их сплавы составляют группу цветных.
Из металлов особое значение имеют железо и его сплавы, являющиеся до настоящего времени основным машиностроительным материалом. В общемировом производстве металлов свыше 90% приходятся на железо и его сплавы. Это объясняется ценными физическими и механическими свойствами черных металлов, а также и тем, что железные руды широко распространены в природе, а производство чугуна и стали сравнительно дешево и просто.
Наряду с черными металлами широкое применение в технике имеют цветные металлы. Это объясняется рядом важных физико-химических свойств, которыми не обладают черные металлы. Наиболее широко используют в судостроении, самолетостроении, радиотехнике, электронике и в других отраслях промышленности медь, алюминий, магний, никель, титан, вольфрам, бериллий и другие цветные металлы.
Особое развитие за последние годы получило производство композиционных и неметаллических материалов (пластмасс, резины, стекол, клеев, лакокрасочных покрытий и т. д.). Применение композиционных материалов дает возможность создавать новые материалы с заранее заданными свойствами, высокой эффективностью по массе и технологичностью. Пластмассы и другие неметаллические материалы используют в конструкциях машин и механизмов взамен металлов и сплавов. Такие материалы позволяют повысить сроки службы деталей и узлов машин и установок, снизить массу конструкций, сэкономить дефицитные цветные металлы и сплавы, снизить стоимость и трудоемкость обработки.
Рациональный выбор материалов и совершенствование технологических процессов их обработки обеспечивают надежность конструкций, снижают себестоимость и повышают производительность труда.
Тема 1. Кристаллическое строение металлов и его влияние на механические свойства. Полиморфизм. Дефекты в кристаллах, теоретическая прочность.
1.1 Кристаллическое строение металлов и его влияние на механические свойства.
Все вещества в твердом состоянии могут иметь кристаллическое или аморфное строение. В аморфном веществе частицы (атомы, молекулы) расположены хаотично, сохраняют лишь так называемый ближний порядок, т.е. в пространстве закономерно расположено небольшое количество атомов, а не атомы всего объема. Кристаллическое состояние прежде всего характеризуется определенным, закономерным расположением частиц в пространстве всего объема вещества, т. е. сохраняется так называемый дальний порядок. Это обусловливает то, что в кристалле каждый атом имеет одно и то же количество ближайших атомов — соседей, расположенных на одинаковом от него расстоянии.
Стремление атомов (ионов) металла расположиться возможно ближе и плотнее друг к другу, приводит к тому, что число встречающихся комбинаций взаимного расположения атомов металла в кристаллах невелико. Расположение атомов в кристалле весьма удобно изображать в виде пространственных схем, в виде так называемых элементарных кристаллических ячеек, узлы которой являются местом расположения атомов (ионов). Под элементарной кристаллической ячейкой подразумевается наименьший комплекс атомов, который при многократном повторении в пространстве позволяет воспроизвести пространственную кристаллическую решетку.
Кристаллическая структура может быть представлена изображением одной элементарной ячейкой (выделена жирными линиями на рис. 1.1), повторяющейся в трех измерениях. Трансляцией этого наименьшего объема можно полностью воспроизвести структуру кристалла.

Рис. 1.1. Кристаллическая структура, элементарная ячейка
В кристалле элементарные частицы (атомы, ионы) сближены до соприкосновения. Для упрощения пространственное изображение принято заменять схемами, где центры тяжести частиц представлены точками. В точках пересечения прямых линий располагаются атомы; они называются узлами решетки. Расстояния a, b и c между центрами атомов, находящихся в соседних узлах, называют параметрами или периодами решетки. Периоды решетки выражаются в ангстремах (А=110-10м). Периоды решетки для большинства металлов находятся в пределах 0,3 – 0,7 нм. Параметр решетки - чрезвычайно важная характеристика. Современные методы рентгеноструктурного анализа позволяют измерять параметр с точностью до одной стотысячной доли ангстрема.
Общим свойством металлов и сплавов является их кристаллическое строение.
Три типа элементарных ячеек кристаллических решеток, наиболее характерных для металлов: объемно-центрированная кубическая (ОЦК) гранецентрированная кубическая (ГЦК), и гексагональная плотноупакованная (ГП), а также схемы упаковки в них атомов показаны на рис.1.2.
В кубической объемно-центрированной решетке (ОЦК) атомы расположены в вершинах куба, а один – в центре его объема (рис.1.2б). ОЦК решетку имеют металлы: Feα, Tiβ, W, V, Cr, Nb и др.
В кубической гранецентрированной решетке (ГЦК) атомы расположены в вершинах куба и в центре каждой грани (рис.1.2а). Решетку такого типа имеют металлы Pb, Ni, Ag, Au, Pt, Feγ, Cu и др.
В гексагональной плотноупакованной решетке (ГПУ) атомы расположены в вершинах и центре шестигранных оснований призмы, а три атома – в средней плоскости призмы (рис.1.2в). Такую упаковку атомов имеют металлы: Mg, Tiα, Zn, Cd, Be и др.
Существенное значение для свойств данного металла или сплава имеет число атомов, находящихся в непосредственном контакте и компактность решетки. Поэтому для характеристики кристаллических решеток введены понятия базиса решетки, координационного числа, коэффициента компактности.
Базисом решетки называют количество атомов, приходящихся на элементарную ячейку.
На одну элементарную ячейку ОЦК решетки приходится два атома (рис.1.3): один в центре куба и другой вносят атомы в вершине куба (каждый атом в вершине куба одновременно принадлежит восьми сопряженным элементарным ячейкам, и на данную ячейку приходится лишь 1/8 массы этого атома, а на всю ячейку 1/8 х 8 = 1 атом).
На элементарную ячейку ГЦК решетки приходится четыре атома; из них один вносят атомы в вершинах куба (1/8 х 8 = 1 атом), а три суммарно (1/2 х 6 = 3 атома) вносят атомы из числа центрирующих грани, так как каждый из таких атомов принадлежит двум решеткам.
На элементарную ячейку гексагональной плотноупакованной решетки приходится шесть атомов (3 + 1/6 х 12 + 1/2 х 2 =6)

Рис. 1.2. Типы элементарных ячеек кристаллических решеток металлов и схемы упаковки в них атомов: а – гранецентрированная кубическая (ГЦК); б – объемно центрированная кубическая (ОЦК); в – гексагональная плотноупакованная (ГП) решетка.
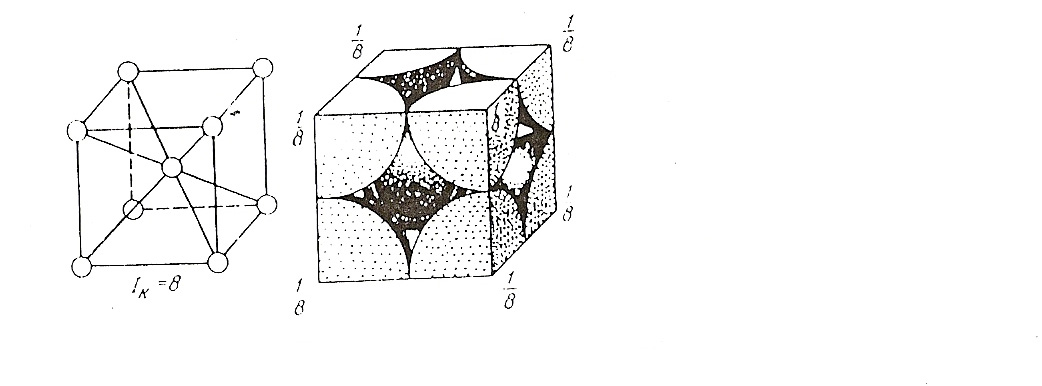
Рис. 1.3. Схема определения базиса ОЦК решетки.
Координационным числом (К) называют число ближайших атомов, равноудаленных «соседей», находящихся на расстоянии наиболее близком от данного атома. В решетке ОЦК каждый атом имеет всего 8 ближайших соседей, а в решетках ГЦК и ГП их 12 (рис.1.4). Таким образом, для ОЦК решетки координационное число равно 8, для решетки ГЦК оно составляет 12. ГП решетка, для которой c/α = 1,633, также имеет координационное число 12.
Таким образом, решетка ОЦК менее компактна, чем решетки ГЦК и ГП. У многих металлов, кристаллизующихся в гексагональной системе, отношение c/α находится в пределах 1,57 - 1,633, т.е. может отклоняться от плотной упаковки, для которой c/α = 1,633. Если отношение c/α значительно отличается от 1,633 (например, для цинка и кадмия), то координационное число гексагональной упаковки соответствует 6.
Коэффициент компактности(Q) определяется отношением объема, занимаемого атомами Vа, ко всему объему решетки Vp, т. е. Q =Va/Vp. Для ОЦК решетки Q= 68 %, а для решеток ГЦК и ГП Q = 74%.

Рис. 1.4. Схема, показывающая число атомов находящихся на равном и наименьшем расстоянии от данного атома в разных кристаллических решетках (С.С. Штейнберг): а) – К8; б) – К12; в) – Г12.
Некоторые металлы при разных температурах могут иметь различную кристаллическую решетку. Способность металла в твердом состоянии при различных температурах (или давлении) иметь различные типы кристаллических форм называют полиморфизмом или аллотропией. Низкотемпературную полиморфную модификацию называют α, а высокотемпературные - β, затем γ, δ и т.д., которые в виде индекса добавляют к символу, обозначающему элемент.
Известны полиморфные превращения железа: Feα ↔ Feγ↔Feδ, Tiα↔Tiβ, Snα↔ Snβ и др. При полиморфном превращении меняется форма и тип кристаллической решетки. Это явление называется перекристаллизацией. Так, при температуре ниже 911ºC устойчиво Feα, в интервале 911 – 1392ºC устойчиво Feγ. При нагреве выше 911ºC атомы решетки ОЦК перестраиваются, образуя решетку ГЦК.
Явление полиморфизма в металлах имеет большое практическое значение. Достаточно отметить, что только благодаря полиморфизму железа имеется возможность широкого изменения свойств сплавов на основе железа посредством термической обработки (закалки и отжига).
При переходе из одной полиморфной формы в другую меняются свойства, в частности плотность и соответственно объем вещества. Например, плотность Feγ на 3% больше плотности Feα, а удельный объем соответственно меньше. Эти изменения объема необходимо учитывать при термообработке.
При рассмотрении схемы элементарных ячеек (рис.1.2) выясняется, что плотность упаковки атомов в разных направлениях в кристалле разная. Поэтому и свойства кристаллического тела в разных направлениях будут разные. Такое явление, когда свойства вещества зависят от направления, называется анизотропией.
Разница в физико-химических и механических свойствах в разных направлениях может быть весьма существенной. При измерении в двух взаимно перпендикулярных направлениях кристалла железа значения температурного коэффициента линейного расширения различаются в 3 - 4 раза, а прочности – более чем в два раза.
Анизотропия свойств характерна для одиночных кристаллов (монокристаллов). Большинство же технических литых металлов имеют поликристаллическое строение. Они состоят из большого числа кристаллов или зерен, которые по ряду причин не имеют возможности принять правильную форму. При этом каждое отдельное зерно анизотропно. Различная ориентировка отдельных зерен приводит к тому, что в целом свойства поликристаллического металла являются усредненными, т.е. поликристаллическое тело является псевдоизотропным. Такая мнимая изотропность металла не будет наблюдаться, если кристаллы имеют одинаковую преимущественную ориентацию в каких-то направлениях. Эта ориентированность, или текстура, создается, например, в результате значительной холодной деформации. В этом случае поликристаллический металл приобретает анизотропию свойств. Свойства деформированного металла вдоль и поперек направления деформации могут существенно различаться.
Чтобы понять явление анизотропии, необходимо выделить (обозначить) кристаллографические плоскости и кристаллографические направления в кристалле. Плоскости, проведенные в кристаллографической решетке через узлы (атомы), называются кристаллографическими плоскостями. Прямые, проведенные через узлы кристаллической решетки, называются кристаллографическими направлениями. Для обозначения кристаллографических плоскостей и направлений пользуются индексами Миллера.
Чтобы установить индексы Миллера, элементарную ячейку кристалла вписывают в пространственную систему координат, как показано на рис.1.5. Оси координат X, Y и Z называют кристаллографическими осями. За единицу измерения вдоль каждой оси принимается период решетки, т.е. длина ребер элементарной ячейки.
Индицирование кристаллографических плоскостей рассмотрим на примере простой кубической решетки (рис.1.5а). В данном случае единица измерения вдоль осей – длина ребра куба а.
Для определения индексов кристаллографических плоскостей необходимо: определить координаты точек пересечения плоскости с осями координат в единицах периодов решетки; взять обратные значения этих величин; привести их к наименьшим целым числам, умножая или деля на общий множитель. Полученные значения простых целых чисел (в круглых скобках) и являются индексами Миллера плоскости.
Рассмотрим индексы Миллера плоскости, пересекающей оси координат в точках: х = 1/2а, у = 1а, z = 1/3а (где а – период решетки, рис.1.5). Обратные значения этих чисел: 2, 1, 3. Эти числа являются простыми. Поэтому индексы этой плоскости будут (213). Следует читать: два, один, три. Индекс по оси показывает, на сколько равных частей плоскость делит осевую единицу по данной координатной оси.
Плоскость, параллельная какой-либо координатной оси, имеет по этой оси индекс нуль, так как 1/∞ = 0. Так, например, плоскость qmrn (рис.1.5) имеет индексы (110).
Если плоскость пересекает ось в области отрицательных значений координат, то соответствующий индекс будет отрицательным, и знак минус ставится над индексом.
Непараллельные плоскости, имеющие одинаковое атомное строение, кристаллографически эквивалентны (например, (001), (100) или (110) и (011) и т.д.). Зная индексы (hkl) плоскости, можно подсчитать межплоскостное расстояние d между плоскостями данного семейства для кубических кристаллов с периодом решетки а по формуле (1.1)
![]() (1.1)
(1.1)
Эта зависимость широко используется при рентгеноструктурном анализе кристаллических тел, имеющих кубическую решетку.

Рис. 1.5. Плоскости и направления в кристаллах: а – индицирование кристаллографических плоскостей; б - индицирование кристаллографических направлений.
Индицирование кристаллографических направлений рассмотрим на рис.1.5,б. Ориентация прямой определяется координатами двух ее точек. При определении индексов направлений необходимо, чтобы одна точка направления совпадала с началом координат (если прямая не проходит через начало координат, то необходимо путем параллельного переноса совместить ее с началом координат или перенести начало координат на прямую); установить координаты любой другой точки, лежащей на данной прямой в единицах периода решетки; привести отношения этих координат к отношению трех наименьших целых чисел. Заключив полученные числа в квадратные скобки, получим индексы кристаллографического направления.
Например, индексы направления о а (рис.1.5,б) будут [111].
Для получения индексов прямой, проходящей через точки l и центр грани k(рис.1.5,б), необходимо перенести линию lk параллельно самой себе так, чтобы она проходила через начало координат, и определить новые координаты точки k по формулам х = - ½, у = + 1.
Для получения индексов прямой, проходящей через точки l и центр грани k (рис.1.5,б), необходимо перенести линию lk параллельно самой себе так, чтобы она проходила через начало координат, и определить новые координаты точки k по формулам х = - ½, у = + 1, z = ½. Наименьшие целые числа без общего множителя будут – 1, 2, 1. Знак минус у индекса ставится над ним. Тогда индексы направления [hkl] будут [Ī21].
В кубической решетке индексы направления, перпендикулярного плоскости (hkl), имеют те же индексы, т.е. [hkl].
После открытия лучей Рентгена, длина волны которых соизмерима с периодом решетки, появилась возможность непосредственного исследования расположения атомов в кристаллической решетке.
Как известно из курса физики, основой рентгеноструктурного анализа является формула Вульфа – Брэгга, показывающая условия интерференции отраженных рентгеновских лучей от атомов в параллельных кристаллографических плоскостях кристалла. Лучи, отраженные от этих плоскостей, будут усиливать друг друга при условии, когда разность пути Δ для лучей равна целому числу длин волн λ:
![]() , (1.2)
, (1.2)
где n – целое число; λ – длина волны рентгеновских лучей; d – межплоскостное расстояние; θ– угол падения и отражения рентгеновских лучей.
Формула для расшифровки линий рентгенограмм, снятых с материалов с кубической решеткой, получится из формул (1.1) и (1.2):
![]() (1.3)
(1.3)
По промерам рентгенограммы устанавливают sinθ. Зная длину волны λ и параметр решетки а, устанавливают индексы плоскости (hkl), от которых получены соответствующие линии на рентгенограмме.
