
книги / Технология термического производства. Способы наноструктурирования материалов
.pdf2. НАГРЕВ И ОХЛАЖДЕНИЕ ПРИ ТЕРМИЧЕСКОЙ ОБРАБОТКЕ СТАЛИ
Термическая обработка включает три основных технологических перехода: нагрев с определенной скоростью до заданной температуры, выдержку для полного прогрева садки и полного протекания фазовых и структурных превращений и охлаждение с требуемой для данного вида обработки
скоростью. |
|
Нагрев |
при термической обработке можно провести |
в печах с |
воздушной атмосферой (печи сопротивления), |
в среде дымовых газов (топливные печи), в контролируемой защитной атмосфере, в расплавах солей и металлов (печи с жидкими теплоносителями), в кипящем слое псевдоотожженных дисперсных частиц (печи с кипящим слоем), токами высокой частоты (индукционный нагрев на установках ТВЧ) и др.
Основные виды термической обработки (отжиг, нормализация, закалка) требуют сквозного нагрева изделий с переходом исходной структуры сталей в аустенит и измельчением зерна. Известно, что указанные превращения протекают быстрее в процессе выдержки, нежели в самом процессе нагрева. Следовательно, выгодно увеличивать скорость нагрева. Выгодно это и экономически: повышается производительность печного оборудования (нагрев занимает от 40 до 80 % времени всего технологического цикла), сокращается угар металла, экономится расход топлива на единицу нагреваемого металла, сокращается парк печей и т.д.
2.1. Требования к нагреву. Взаимодействие газовой атмосферы со сталью при нагреве
Термические печи должны удовлетворять требованиям технологического процесса, обеспечивать заданную температуру и высокое качество нагрева, т.е. скорость нагрева, рав-
11
номерность нагрева, отсутствие окисления и обезуглероживания поверхности нагреваемых изделий.
В печной атмосфере могут присутствовать О2, Н2, N2, СО2, СО, Н2О, различные углеводороды (СН4 и др.), сернистые соединения SO2 и Н2S, и, следовательно, неизбежно взаимодействие этих компонентов с нагреваемым металлом. Эти же составляющие могут присутствовать и в защитных (контролируемых) атмосферах.
Диффузионный процесс взаимодействия между кислородом воздуха и содержащими кислород компонентами газовой атмосферы, с одной стороны, и железом, а также легирующими элементами, с другой стороны, называют окислением стали. Газами, которые не только окисляют но и обезуглероживают поверхность стали, являются углекислый газ (СО2) и водяной пар (Н2О).
Железо с кислородом образуют ряд химических соединений: FеО – закись железа, Fе3О4 – окись-закись железа, Fe2O3 – окись железа. При температурах ниже 570 °С образование закиси железа исключено. При температурах выше 570 °С образуются окислы Fе2О3, Fe3O4, FеО. Слой окалины растет вследствие диффузии железа и легирующих элементов к поверхности металла и встречной диффузии кислорода во внутренние слои металла.
Основными реакциями взаимодействия газов со сталью являются:
2Fe + O2 = 2FeO |
(1) |
3Fe + 2О2 = Fe3O4 |
(2) |
4Fe + 3O2 = 2Fe2O3 |
(3) |
Возможны также реакции |
|
4FeO + O2 = 6Fe2O3 |
(4) |
4Fe3O4 + O2 = 6Fe2O3 |
(5) |
12
Взаимодействие водяного пара с железом при температурах ниже 570 °С протекает по реакциям
H2O + 2Fe3O4 = 3Fe2O3 + H2 |
(6) |
4H2O + 3Fe ↔ Fe3O4 + 4H2 |
(7) |
При температурах выше 570 °С – по реакциям |
|
H2O + 2Fe3O4 = 3Fe2O3 + H2 |
(8) |
H2O + 3FeO ↔ Fe3O4 + H2 |
(9) |
H2O + Fe ↔ FeO + H2 |
(10) |
Взаимодействие двуокиси углерода с железом при тем- |
|
пературах ниже 570 °С – по реакциям |
|
CO2 + 2Fe3O4 ↔ 3Fe2O3 + CO |
(11) |
4CO2 + 3FeO ↔ Fe3O4 + 4CO |
(12) |
А при температурах выше 570 °С – по реакциям |
|
CO2 + 2Fe3O4 ↔ 3Fe2O3 + CO |
(13) |
CO2 + 3FeO ↔ Fe3O4 + CO |
(14) |
CO2 + Fe ↔ FeO + CO |
(15) |
Реакция взаимодействия железа с водяным паром (Н2О) сопровождается выделением тепла, т.е. является экзотермической. Реакция взаимодействия двуокиси углерода с железом сопровождается поглощением тепла, т.е. является эндотермической.
На рис. 2.1 приведены теоретические кривые равновесия реакций окисления – восстановления железа с двуокисью и окисью углерода (реакция 15) и водяным паром и водородом (реакция 10).
Кривые 1 и 2 представлены так, что в левой части от кривых расположены области восстановления железа, а в правой части – области окисления железа.
13

|
Окислительная |
способ- |
||||
|
||||||
|
ность |
двуокиси |
углерода |
|||
|
с понижением |
температуры |
||||
|
уменьшается, а с повышением |
|||||
|
температуры |
увеличивается |
||||
|
(см. рис. 2.1, кривая 1). При |
|||||
|
температуре ниже 500 °С дву- |
|||||
|
окись |
углерода |
не |
может |
||
|
окислять железо. |
Константа |
||||
|
равновесия, представляющая |
|||||
|
отношение парциальных дав- |
|||||
|
лений |
двуокиси |
углерода |
|||
|
к окиси углерода, изменяется |
|||||
|
от 0,27 до единицы при сни- |
|||||
|
жении |
температуры |
газовой |
|||
Рис. 2.1. Кривые равновесия ре- |
||||||
атмосферы с 1300 до 500 °С. |
||||||
акций Fe + H2O ↔ FeO + H2 (2) |
Окислительная |
способность |
||||
и Fe + CO2 ↔ FeO + CO |
водяных паров с понижением |
|||||
|
||||||
температуры увеличивается, а с повышением температуры уменьшается (см. рис. 2.1, кривая 2). Константа равновесия, представляющая отношение парциальных давлений водяного пара к водороду, при снижении температуры с 1300 до 370 °С изменяется от 0,85 до 0,07.
В сложной газовой атмосфере, имеющей в своем составе окись углерода, двуокись углерода, водород и водяной пар,
протекают реакции |
|
СО + Н2 ↔ С + Н2О |
(16) |
СО + Н2О ↔ СО2 + Н2 |
(17) |
На рис. 2.2 приведена кривая равновесия реакции 17, имеющая важное значение при регулировании печной газовой атмосферы. По оси ординат отложена константа равнове-
сия этой реакции К3 = РН2О РСО , по оси абсцисс – темпера-
РН2 РСО2
14

тура. Реакция (17) характери- |
|
зует суммарный результат ре- |
|
акций (10) и (15). |
|
Величина константы рав- |
|
новесия реакции (17) не позво- |
|
ляет непосредственно устано- |
|
вить, является ли сложная га- |
|
зовая смесь окислительной или |
|
восстановительной по отноше- |
|
нию к железу и его окислам. |
|
Для этого необходимо проана- |
|
лизировать условия равновесия |
|
слагаемых реакций (10) и (15). |
Рис. 2.2. Кривые равновесия |
Для безокислительного на- |
|
грева необходимо иметь отно- |
реакций CO + H2O ↔ CO2 + H2 |
шение газов-окислителей к га- |
|
зам-восстановителям в защитной атмосфере (в объемных процентах) во всем интервале рабочих температур в соответствии с кривыми равновесия, представленными на рис. 2.1.
Например, при нагреве железа до 850 °С для безокислительного нагрева необходимо, чтобы константы равновесия были
1 = РСО2 ≤ 0,487,
К5 РСО
1= РНО2 ≤ 0,564.
К4 РН2
Отсюда константа равновесия водяного газа
К3 = К4 К5 = РН2О РСО .
РН2 РСО2
Константы равновесия К3, К4, К5 имеют определенное значение для каждой температуры газовой смеси [1, 9, 10].
15
Большое влияние на степень окисления железа оказывает присутствие в атмосфере сернистых соединений SO2
иH2S. Если содержание SO2 в контролируемой атмосфере увеличивается от 0,1 до 0,5 %, то окислительная способность
этой атмосферы увеличивается примерно в 3 раза. SO2 и H2S понижают точку плавления окалины железа, вследствие чего оплавляющаяся окалина обнажает все новые слои металла, что сильно увеличивает потери металла. Необходимо тщательно очищать контролируемые атмосферы от SO2 и H2S
ине допускать их остаточного содержания в газе свыше
0,005 %.
Помимо окисления стальные детали могут науглероживаться или обезуглероживаться. Обезуглероживание стали – это диффузионный процесс взаимодействия кислорода воздуха или кислородсодержащих компонентов газовой среды с углеродом стали, приводящий к частичному или полному удалению углерода из поверхностных слоев стали.
Диффузионный процесс, при котором поверхностные слои стали насыщаются углеродом, называется науглероживанием или цементацией. Этот процесс протекает в три этапа: 1) диффузия молекул цементующего газа к поверхности стальных деталей; 2) химический процесс адсорбции аустенитом углеродсодержащих молекул с образованием атомов
углерода в результате диссоциации молекул СО и СН4 при температурах выше верхней критической точки; молекулы
СО и СН4 образуют с аустенитом прочную связь; 3) дальнейшая диффузия атомов углерода в глубинные слои стали.
При цементации имеют место следующие реакции:
2CO ↔ C(Feγ) + CO2 |
(18) |
CH4 ↔ C(Feγ) + 2H2 |
(19) |
При насыщении углеродом γ-твердого раствора железа– аустенита сверх предела растворимости протекают реакции с образованием карбида железа–цементита:
16

PNRPU
3Fe + 2CO ↔ Fe3C + CO2 |
(20) |
3Fe + CH4 ↔ Fe3C + 2H2 |
(21) |
3Fe + CO + H2 ↔ Fe3C + H2O |
(22) |
Одновременно в газовой атмосфере могут протекать реакции с образованием углерода (сажи).
На рис. 2.3 показаны типичные теоретические равновесные кривые реакции (18) для углеродистых сталей с различным содержанием углерода.
Рис. 2.3. Кривые равновесия реакции
3Fe + 2CO ↔ Fe3C + CO2 (Остин и Дей) I – науглероживание, II – феррит+аустенит, III – обезуглероживание
17
Если известны температура нагрева стали и заданная концентрация углерода, то по кривым равновесия можно найти соответствующую точку на оси ординат, по которой
|
Р2 |
|
определяется константа равновесия К6 = |
СО |
, и вычислить |
Р |
||
|
СО2 |
|
процентное содержание окиси и двуокиси углерода в равновесной газовой атмосфере.
При анализе взаимодействия по реакции (21) необходимо учитывать, что диффузия углерода в железо при взаимодействии метана с железом протекает активнее, чем окиси углерода с железом по реакции (20). Активность метана по сравнению с активностью окиси углерода при взаимодействии их с железом в температурном интервале от 800 до 1100 °С возрастает в 8–400 раз (табл. 2.1).
Кроме этого, условия равновесия между газовой фазой и сталью, сильно изменяются при различной степени насыщения углеродом аустенита стали. При постоянном значении константы равновесия обезуглероживающая способность атмосферы СО – СО2 увеличивается с повышением температуры, науглероживание железа при этих условиях уменьшается
(см. рис. 2.3).
Таблица 2.1
Сравнительная степень активности углерода, выделяющегося из окиси углерода и метана, при диффузии в железо
|
Максимальное количество |
Соотношение |
|
Температура |
активного углерода, г/м3 |
||
цементации, °С |
|
|
активности газов |
из оксида |
из метана |
||
|
углерода (СО) |
(СН4) |
СН4/СО |
|
|
||
800 |
64,2 |
513 |
8 |
900 |
13,9 |
525,6 |
38 |
1000 |
4,3 |
530,6 |
123 |
1100 |
1,34 |
532,7 |
400 |
18
Таким образом, взаимодействия компонентов газовых сред со сталью являются атомно-молекулярными процессами, направление которых определяется законами химической термодинамики. Основные факторы, влияющие на ход процессов окисления (восстановления) и обезуглероживания (науглероживания) стали: состав печной атмосферы, температура, время, состав стали, состав окалины. Однако термодинамические уравнения и теоретические кривые равновесия не учитывают скорость протекания процессов взаимодействия, поскольку они не включают такой параметр, как время процесса. Поэтому на практике разрабатываются и используются эмпирические диаграммы равновесия, эмпирические кривые равновесия, построенные по экспериментальным данным для различных систем и различных газовых атмосфер применительно к конкретным условиям. В практике термической обработки для защиты от окисления и обезуглероживания широко используют контролируемые атмосферы (эндо-, экзоатмосферы), состав которых оценивают и регулируют по содержанию водяного пара или по содержанию двуокиси углерода. Непосредственное измерение содержания водяных паров в атмосфере затруднительно, поэтому используют косвенный параметр «точку росы».
Точка росы – это температура, при которой начинается конденсация содержащихся в атмосфере водяных паров. Возможность использования этого параметра вытекает из однозначной зависимости между точкой росы и содержанием
водяных паров n в атмосфере: |
|
|
|
|
||
Точка росы, °С |
–20 |
–10 |
–5 |
0 |
+10 |
+20 |
n, г/м3 |
0,81 |
2,05 |
3,18 |
4,84 |
9,73 |
18,5 |
n, % (объем.) |
0,101 |
0,256 |
0,395 |
0,602 |
1,21 |
2,30 |
Науглероживающую (обезуглероживающую) способность атмосферы определяет ее углеродный потенциал, под которым понимают концентрацию углерода в стали, находящейся в равновесии с данным составом атмосферы. Это значит, что
19
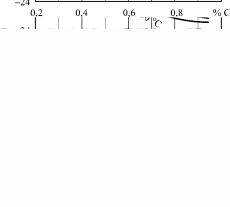
если, например, значение углеродного потенциала атмосферы при данной температуре составляет 0,6 % С, то низкоуглеродистая сталь будет науглероживаться, а высокоуглеродистая – обезуглероживаться в пределе до этого содержания углерода. Для стали с 0,6 % С атмосфера будет нейтральной.
При выборе состава атмосфер для различных операций термической обработки наряду с характером взаимодействия атмосферы со сталью следует учитывать также температуру процесса. Дело в том, что атмосферы, содержащие свыше 4 % горючих компонентов (окиси углерода и водорода), взрывоопасны и их можно вводить в печь и использовать только при температуре не ниже 760 °С. При более низких температурах
впечи может образоваться гремучая смесь и достаточно пламени и даже искры, чтобы вызвать взрыв этой смеси. Только атмосферы с суммарным содержанием горючих газов меньше 4 % безопасны при любых температурах и количестве воздуха
всмеси, и поэтому их можно использовать для низкотемпературных процессов термической обработки.
Экспериментальные кривые равновесия между сталями и эндотермической атмосферой приведены на рис. (2.4–2.7) [9].
Рис. 2.4. Кривые равновесия углеродистой стали с эндотермической атмосферой
20
