- •Міністерство охорони здоров'я України
- •Модуль 2. Кількісний хімічний аналіз цілі модуля:
- •Заняття 14
- •Актуальність теми
- •Цілі навчання
- •Орієнтовна основа дій
- •1. Послідовність аналітичних операцій в гравіметричному методі осадження
- •2. Правила роботи з аналітичними терезами
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Еталони рішення типових розрахункових задач
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття №15
- •Актуальність теми
- •Зміст навчання
- •Орієнтовна основа дій
- •1. Метод відгонки. Схема визначення вологи в лікарських сполуках
- •2. Алгоритм визначення масової частки вологи методом непрямої відгонки
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття №16
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •Короткі методичні вказівки до роботи на практичному занятті
- •Граф логічної структури теми: Титриметричні методи аналізу. Титранти, їх приготування, розрахунки в титриметрії. Приготування розчинів 0,1м NaOh та 0,1м нСl
- •Заняття № 17
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •1. Алгоритм стандартизації розчину hCl за розчином натрію тетраборату
- •2. Алгоритм стандартизації розчину NaOh за оксалатною кислотою
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №18
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії Алгоритм визначення масової відсоткової частки натрію гідроксиду та натрію карбонату в суміші
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття №19
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття № 20
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •1. Алгоритм визначення загальної твердості води
- •2. Схема зворотного комлеконометричнеого визначення свинцю
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття №21
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії Алгоритм приготування та стандартизації 0,1 м розчину AgNo3
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Еталон рішення завдання №7.
- •Короткі методичні вказівки до роботи на практичному занятті
- •Граф логічної структури теми: Осаджувальне титрування. Аргентометрія, меркурометрія. Визначення масової частки галогенідів в препараті осаджувальним
- •Заняття № 22
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •1. Алгоритм стандартизації розчину йоду за тіосульфатом натрію
- •2.Алгоритм стандартизації розчину калію перманганату за розчином натрію оксалату
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Еталон рішення завдання №7
- •Еталон рішення завдання №8
- •Заняття № 23
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа дії
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 27
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа діяльності Цифрові значення крітерія стьюдента
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 25
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Приклади завдань колоквіуму:
- •Заняття № 26
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Питання до підсумкового модульного контролю за темою «Кількісний хімічний аналіз»
- •Приклади ситуаційних завдань до підсумкового модульного контролю:
- •Модуль 3. Кількісний інструментальний аналіз Цілі модуля:
- •Заняття № 27
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм кількісних фотометричних визначень методом градуювального графіка
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №28
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Реєстрація спектру поглинання кофеїну
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №30
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм вимірювання показника заломлення на рефрактометрі
- •Фактори показників заломлення f розчинів лікарських речовин
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 30
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм вимірювання інтенсивності флуоресценції
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 31
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм потенціометричного визначення рН розчину
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Граф логічної структури теми:Електрохімічні методи аналізу. Потенціометрія
- •Заняття № 33
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №33
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм полярографічних визначень
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття №34
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії Алгоритм проведення висхідної паперової або тонкошарової хроматографії
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Граф логічної структури теми: Хроматографічні методи. Паперова та тонкошарова хроматографія
- •Заняття № 35
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтована основа дії
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Короткі методичні вказівки до роботи на практичному занятті
- •Заняття № 37
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Орієнтовна основа діяльності Класифікація методів спектрального аналізу
- •Приклади питань колоквіуму:
- •Заняття № 36
- •Актуальність теми
- •Цілі навчання
- •Зміст навчання
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Заняття № 38
- •Набір завдань для перевірки досягнення конкретних цілей навчання
- •Приклади ситуаційних завдань для підсумкового модульного контролю
Набір завдань для перевірки досягнення конкретних цілей навчання
Тест 1
Для кількісного визначення іонів Fe3+ провели фотометричну реакцію з сульфосаліциловою кислотою. При фотометричному визначенні Fe3+ вимірюють:
A. Питоме обертання;
B. показник заломлення;
C. оптичну густину;
D. довжину хвилі;
E. потенціал напівхвилі.
Тест 2
При проведенні кількісного визначення фотометричним методом готується серія з 6-8 стандартних розчинів. Це необхідно для:
A. побудови градуювального графіку;
B. оцінки методики визначення;
C. спрощення методики роботи;
D. вибору кювет;
E. вибору світлофільтру.
Тест 3
Поглинання світла підкоряється об’єднаному закону світо поглинання. Він називається законом:
A. Нернста;
B. Гейровського-Ільковича;
C. Ленгмюра;
D. Бугера -Ламберта-Бера;
E. Менделєєва-Клапейрона.
Тест 4
Методи спектрофотометрії засновані на поглинанні:
A. поліхроматичного випромінювання;
B. монохроматичного випромінювання;
C. відбитого світла;
D. переломленого променю світла;
E. розсіяного випромінювання.
Тест 5
Колориметричним методом можна дослідити розчини:
A. марганцю сульфату;
B. плюмбуму нітрату;
C. натрію форміату;
D. калію перманганату;
E. алюмінію хлориду.
Тест 6
Молекулярно-абсорбційний метод ґрунтується на:
A. поглинанні світла вільними атомами;
B. випромінюванні світла збудженими атомами та іонами;
C. поглинанні світла молекулами;
D. випромінюванні світла молекулами;
E. поглинанні світла збудженими атомами та іонами.
Тест 7
Фізико-хімічні методи використовують для кількісного визначення лікарських речовин. Який з наведених нижче методів ґрунтується на визначенні оптичної густини розчину?
A. спектрофотометрія;
B. полярографія;
C. потенціометрія;
D. кулонометрія;
E. електрогравіметрія.
Тест 8
Яке рівняння, згідно закону Бугера-Ламберта-Бера, дає змогу розрахувати оптичну густину (D) розчину залежно від молярної концентрації (С)?
A. D = I/K*C;
B. D = lgС/К;
C. D = К/С;
D. D = lgK*C;
E. D = К * C.
Тест 9
Що означає термін "калібровочний графік" в методі фотометрії?
A. графік залежності оптичної густини розчину (D) від інтенсивності І світла, що пройшло крізь розчин;
B. графік залежності оптичної густини розчину (D) від інтенсивності падаючого світла І0;
C. графік залежності оптичної густини розчину (D) від концентрації C;
D. графік залежності молярної концентрації C від інтенсивності падаючого світла І0;
E. графік залежності молярної концентрації C від інтенсивності світла І , що пройшло крізь розчин.
Тест 10
Розрахуйте концентрацію Fe3+ в досліджуваному розчині за наступними даними фотометричного визначення його з сульфосаліциловою кислотою. Стандартний розчин з концентрацією 2,00 мг/дм3 мав оптичну густину 0,285; розчин з концентрацією 4,00 мг/л — 0,56. Оптична густина досліджуваного розчину дорівнювала 0,45. Товщина кювети складала 2 см. Розрахуйте молярний коефіцієнт поглинання забарвлених розчинів, отриманих при даних умовах.
Тест 11
Провізор проводить фотометричне визначення сполук купрума за допомогою реакції комплексоутворення. Визначте величину молярного коефіцієнта поглинання аміачного комплексу купрума (II), якщо оптична густина його розчину з концентрацією 0,005 моль/дм3 дорівнює 0,545, товщина шару – 3 см.
Тест 12
Коефіцієнт молярного поглинання комплексної сполуки алюмінію з алізарином дорівнює 1,6 · 104 дм3∙моль-1∙см-1 при λ= 485 нм. Яку кювету слід обрати для фотометричних вимірювань, щоб оптична густина розчину була не менше 0,3 при вмісті алюмінію 10-5 моль/дм3 в розчині, що фотометрують?
Тест 13
Розрахуйте коефіцієнт молярного поглинання комплексу купруму з 2,2 – оксихіноліном при λ = 546 нм, якщо оптична густина 2 ·10-5 М розчину цієї сполуки в кюветі з l= 5 см дорівнює 0,252?
Тест 14
Коефіцієнт молярного поглинання комплексу плюмбума з дитизоном при λ = 485 нм дорівнює 6,8 ·104 дм3∙моль-1∙см-1. Чому дорівнює оптична густина розчину, що містить 3 мкг РbО2 в 5 см3 при вимірюванні в 1- сантиметровій кюветі?
Еталони відповідей до рішення цільових навчальних задач.
1. – C, 3. – D, 7. – А.
Еталон рішення завдання №10.
Визначення концентрації Fe3+ проводили методом порівняння оптичної густини стандартного і досліджуваного розчинів. Скористаємося формулою:
Сх = (Ах∙ С0)/А0
де Ах та А0 - оптична густина досліджуваного та стандартного розчинів відповідно; С0 - концентрація стандартного розчину;
Сх1= 2∙0,45/0,285 =3,16 мг/ дм3;
Сх2= 4∙0,45/ 0,56 =3,21 мг/ дм3;
Сх серед. = (Сх1 + Сх2)/2; Сх серед. =(3,16 +3,21)/2= З,18 мг/ дм3;
Розрахуємо концентрацію Fe3+ в моль/ дм3;. М(Fe)=55,84 г/моль, тоді С(Fe)=3,18∙10-3/55,84=0,000057 моль/ дм3.
Згідно з основним законом світлополглинання оптична густина розчину дорівнює:
А= ε∙L∙С, тоді ε = А /(L∙С).
ε = 0,45/(0,000057∙2)= 3947 дм3∙моль-1∙см-1
ВІДПОВІДЬ: ε = 3947 дм3∙моль-1∙см-1
Короткі методичні вказівки до роботи на практичному занятті
На початку заняття перевіряється підготовленність студентів до заняття шляхом усного опитування або тестування, проводиться інструктаж з техніки безпеки з хімічними реактивами. Далі студенти знайомляться з методиками експериментальної роботи . Черговим пропонується організувати робоче місце для групи. Студенти працюють самостійно у відповідності до ООД, викладених у методичних вказівках. По закінченні роботи студенти записують свої спостереження, рівняння відповідних хімічних реакцій, проводять необхідні розрахунки. Далі проводиться підсумковий контроль за темою (набори тестів). Потім розглядаються результати самостійної роботи, аналізуються помилки, підводяться підсумки заняття.
Додаток
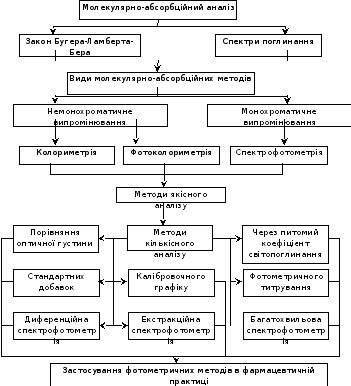
Граф логічної структури теми. Інструментальні методи аналізу. Молекулярно-абсобційний аналіз. Фотометрія