
расчет горения топлива
.docxРасчет горения топлива.
Вычислить расход воздуха, количество и состав продуктов сгорания природного газа, его калориметрическую и действительную температуру, если известно: -состав воздуха: CH4 91,6%; C2H6 1,6%; C3H8 2,0%; C4H10 1,6%; CO2 0,6%; N2 2,6%; -n=1.1; k=N2/O2=79/21=3,76; W=12 г/м3.
1.
Определение количества дутья для
горения.
1.1. Пересчет сухого газа на
влажный
Xвл.=
Xсух.* ;
Xвл.=Xсух.*
;
Xвл.=Xсух.*
 ;
Xвл.=
Xсух.*0,98;
;
Xвл.=
Xсух.*0,98;
CH4вл.=91,6*0,98=90%; C4H10вл.=1,6*0,98=1,5%; C2H6вл.=1,6*0,98=1,5%; CO2вл.=0,6*0,98=0,5%; C3H8вл.=2,0*0,98=2%; N2=2,6*0,98=2,5%;
H2O=0,1242*W; H2O=0,1242*12; H2O=1,5%.
1.2.
Расход кислорода на горение при
n=1,0:
VO2=0,01*(0,5*(CO+H2+3H2S)+∑
(m+ )*CmHn);
VO2=0,01[(m+
)*CmHn);
VO2=0,01[(m+ )*CH4+(m+
)*CH4+(m+ )*C2H6+(m+
)*C2H6+(m+ )*C3H8+(m+
)*C3H8+(m+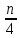 )*C4H10];
VO2=0,01*[(1+
)*C4H10];
VO2=0,01*[(1+ )*90+(2+
)*90+(2+ )*1,5+(3+
)*1,5+(3+ )*2+(4+
)*2+(4+ )*1,5];
VO2=2,045
м3/м3.
)*1,5];
VO2=2,045
м3/м3.
1.3. Расход воздуха на горение при n=1,1: Vв.=n*(1+k)*VO2; Vв.=1,1*(1+3,76)*2,045; Vв.=10,70 м3/м3.
2. Определение состава продуктов сгорания. 2.1. Состав продуктов сгорания. VCO2=0,01*(CO2+SO2+CO+H2S+∑ m*CmHn); VCO2=0,01*(CO2+CH4+m*C2H6+m*C3H8+m*C4H10); VCO2=0,01*(0,5+90+2*15+3*2+4*1,5); VCO2=1,055 м3/м3.
VH2O=0,01*(H2O+H2+H2S+0,5*∑n*CmHn); VH2O=0,01*(H2O+0,5*(n*CH4+n*C2H6+n*C3H8+n*C4H10); VH2O=0,01*(1,5+0,5*(4*90+6*1,5+8*2+10*1,5)); VH2O=2,015 м3/м3.
VN2=0,01*N2+n*k*VO2; VN2=0,01*2,6+1,1*3,76*2,045; VN2=8,815 м3/м3.
VO2=(n-1)*VO2; VO2=(1,1-1)*2,045; VO2=0,204 м3/м3.
2.2. Определение общего количества продуктов сгорания (дыма). Vп.с.=VRO2+VH2O+VN2+VO2; Vп.с.=VCO2+VH2O+VN2+VO2; Vп.с.=1,055+2,015+8,815+0,204; Vп.с.=12,089 м3/м3.
2.3.
Определение процентного состава
продуктов сгорания.
CO2=
 ;
N2=
;
N2= ;
CO2=
;
CO2= ;
N2=
;
N2=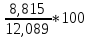 ;
CO2=8,73%.
N2=72,92%.
;
CO2=8,73%.
N2=72,92%.
H2O=
 ;
O2=
;
O2= ;
H2O=
;
H2O= ;
O2=
;
O2= ;
H2O=16,67%.
O2=1,69%.
;
H2O=16,67%.
O2=1,69%.
2.4.
Определение плотности продуктов
сгорания.
ρп.с.
= ;
где
44; 28; 18; 32 – молекулярная масса; 22,4 – 1
моль.
ρп.с.
=
;
где
44; 28; 18; 32 – молекулярная масса; 22,4 – 1
моль.
ρп.с.
= ;
ρп.с.
=
;
ρп.с.
= ;
ρп.с.
=
1,24 км/м3.
;
ρп.с.
=
1,24 км/м3.
3.
Теплота сгорания газа составит:
 =
358*CH4+636*C2H6+913*C3H8+1185*C4H10;
=
358*CH4+636*C2H6+913*C3H8+1185*C4H10;
 = 358*90+636*1,5+913*2+1185+1,5;
= 358*90+636*1,5+913*2+1185+1,5;
 =
36777 кДж/м3.
=
36777 кДж/м3.
4. Определение калориметрической температуры.
4.1.
При горении природного газа в обычном
воздухе энтальпия продуктов сгорания
определяется:
 =
=
 ;
;
 =
=
 ;
;
 кДж/м3.
кДж/м3.
4.2.
Для определения калориметрической
температуры природного газа зададимся
сначала
 =
= и определим при этой калориметрической
температуре энтальпию.
и определим при этой калориметрической
температуре энтальпию.
 =
=
 ;
;
 =
=
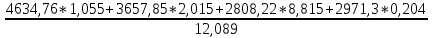 ;
;
 =3111,99
кДж/м3
т.к.
=3111,99
кДж/м3
т.к.
 , принимаем температуру
, принимаем температуру
 и рассчитаем энтальпию при этой
температуре.
и рассчитаем энтальпию при этой
температуре.
 =
= ;
;
 кДж/м3;
т.к.
кДж/м3;
т.к.
 <
< определим
определим

 ;
;
 ж
ж
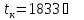 .
.
5.
Определение действительной температуры
в печи:
 ,
где
,
где
 – коэффициент, зависящий от конструкции
печи;
– коэффициент, зависящий от конструкции
печи;
 ;
;
 .
.
Вывод:
при полученном расходе воздуха, равном
10,70 м3/м3
,
образуется дыма 12,089 м3/м3.
Калорийность топлива равна 36777 кДж/м3
, что при его горении позволяет создать
в рабочем пространстве печи температуру
равную
 .
.
