
КР3 ответы
.pdf
Вопрос№1: Иммунотоксичность.Строениеособенности иммуннойсисте,понятиеымунотокс.Действиечности токсикантовнаиммуннуюсисте.Иммуносупрессия.
Гиперчувствительность.Характеристикагиперчувствительности. Иммунотоксикантымеханизмыихдействия.
Участие иммунной системы в реализации механизмов токсического действия ксенобиотиков.
Иммунная система – высоко специализированная, сложно регулируемая система, её клеточныеэлементы находятся в состоянии постоянной пролиферации.
Строение иммунной системы: кровеносное русло и лимфатические сосуды, пронизывающие все ткани организма, по которым перемещаются мириады иммунокомпетентных клеток.
Мириады – это бесчисленное множество. Функция системы-выявить антигены (чужеродные элементы),проникшие во внутренние среды, изолировать их и уничтожить.
Иммунокомпетентные клетки: лимфоциты (Т-лимфоциты, В-лимфоциты), Фагоцитирующие клетки( Макрофаги, микрофаги)
Органы и ткани иммунной системы: Тимус, селезенка, лимфатические узлы, печень. Характерными особенностями функционирования иммунной системы являются:
1.Специфичность (способность иммунной системы выявлять и особым образом реагировать на чужеродные элементы).
2.Память (повторные контакты с антигеном →усиленная или "адаптированная" реакция (позитивная память); иногда ослабленная реакция (проявление толерантности или негативная память).
3.Кооперативность
4.Подвижность (иммунокомпетентные клетки, модуляторы их активности и антитела циркулируют в организме).
5.Клональность (в организме миллионы оседлых и подвижных иммунокомпетентных клеток. Но только небольшая их часть →распознование специфического антигена и вступление в фазу пролиферации (клонообразования)).
6.Регуляция (эффективный иммунный ответ регулируется от начала до конца).
Иммунокомпетентность – это функциональное состояние иммунной системы, при котором обеспечивается эффективная защита организма от инфекционных агентов и опухолевых клеток, а также химических веществ, обладающих антигенными свойствами.
Иммунотоксичность – это свойство ксенобиотиков вызывать нарушения функций организма, проявляющиеся неадекватными иммунными реакциями. Неадекватными могут быть реакции на антигены, сам токсикант, его метаболиты и на комплексные антигены, образующиеся в организме при интоксикациях.
Следствиями иммунотоксического действия ксенобиотиков являются:
• угнетение иммунного ответа (иммуносупрессия);
•формирование гиперчувствительности к антигенам (аллергизация);
•инициация аутоиммунных процессов.
Иммуносупрессия – это подавление иммунного ответа организма на антигены. Свойствами иммуносупрессоров обладают многочисленные ксенобиотики, нарушающие процессы клеточного деления, клеточной дифференцировки, тормозящие синтез белка.
Гиперчувствителность (аллергия). Характеристика состояния гиперчувствительности
Нарушения, сопровождающиеся гиперчувствительностью к антигенам, являются наиболее частой формой проявлений иммунотоксичности у человека. Гиперчувствительность – это избыточная по интенсивности реакция организма на антиген или существенное понижение порога чувствительности к данному антигену.
Аллергия– это изменённая реакция организма на повторное действие фактора. Анафилаксия –острая реакция организма на чужеродный агент, включающую как иммунный, так и воспалительный компоненты.
Атопия – это конституциональная или наследственная склонность к развитию состояний хронической гиперчувствительности.
Типы аллергических реакций: Анафилактические или атопические реакции; Реакции, опосредованные иммунным комплексом; Цитотоксические реакции; Реакции, опосредованные клеточными эффектами
Иммунотоксиканты – это вещества, нарушающие иммунные реакции организма, действуя в минимальных дозах. Be, Pt, Cr, Ni, Cd, этиленоксид, формальдегид, ПАУ, ДДТ, диоксин, метилртуть.

Вопрос№2: Токсичвлияниенар скоепродуфункци. т вную Тератоген.Характертоксик,влз настикаяющихнтов репродуфункцВыявление. действвнуютоксикантовна я репродуфункци. т вную
Репродуктивная функция - сложноорганизованная последовательность физиологических процессов, протекающих в организме отца, матери, плода. Токсиканты могут оказывать неблагоприятное воздействие на любом этапе реализации функции. Установить механизм действия почти невозможно. Нарушения могут быть связаны с конкуренцией ксенобиотика с половым гормонами, действием на рецепторы эстрогенов, нарушением скорости продукции половых гормонов и их метаболизма.
Основные проявления токсического процесса на репродуктивный функции организма
– бесплодие, тератогенез.
Тератогенным называется действие химического вещества на организм матери, отца или плода, сопровождающееся существенным увеличением вероятности появления структурно-функциональных нарушений у потомства/
Эмбриотоксическое действие токсиканта – действие, сопровождающееся гибелью эмбриона/
Основные закономерности тератогенеза: токсикокинетические, генетической предрасположенности, критических периодов чувствительности, общности механизмов формирования, дозовой зависимости
Кинетика действия тератогенов: Попали в организм – распределились по организму. Основной орган биоактивации - печень матери. После активации в печени ксенобиотик может там же и прореагировать в виде активных метаболитов и до плода уже ничего не дойдет. Чтобы дошло до плода, токсикант должен быть относительно инертным, стабильным. Активные метаболиты могут образоваться уже в организме плода. Попадают токсиканты в плод через кровоток, там распределяются по тканям, при этом чувствительность плода к токсикантам зависит от фазы развития.
Выявление действия токсикантов на репродуктивную функцию
1.Изучение оплодотворяемости и общей репродуктивности - в опытах на одном поколении животных;
2.Изучение оплодотворяемости и общей репродуктивности - в опытах на нескольких поколениях животных;
3.Изучение тератогенной активности веществ;
4.Выявление перинатальной и постнатальной токсичности. Опыты выполняются на животных, содержащихся в строго контролируемых условиях
Вопрос№3: Химическиймутагенез.Условиядейстагеноввия наклетки.Изучениемутагеннойактивностиксеноб. отиков
Мутации - это наследуемые изменения генетической информации, хранящейся в ДНК клеток. Наиболее изученными являются последствия действия ионизирующей радиации и таких веществ, как сернистый и азотистый иприты, эпоксиды, этиленимин, метилсульфонат и т.д. Химические вещества, способные вызывать мутации называются мутагенами.
Основные виды мутаций, вызываемые химическими веществами
1. Точечная мутация
Замещение нуклеотида. Если нуклеотид замещается на другой нуклеотид того же типа, например, пуриновое основание на пуриновое основание или пиримидиновое - на пиримидиновое, мутация называется транспозицией. Если пуриновое основание замещается пиримидиновым или наоборот, говорят о трансверсии.
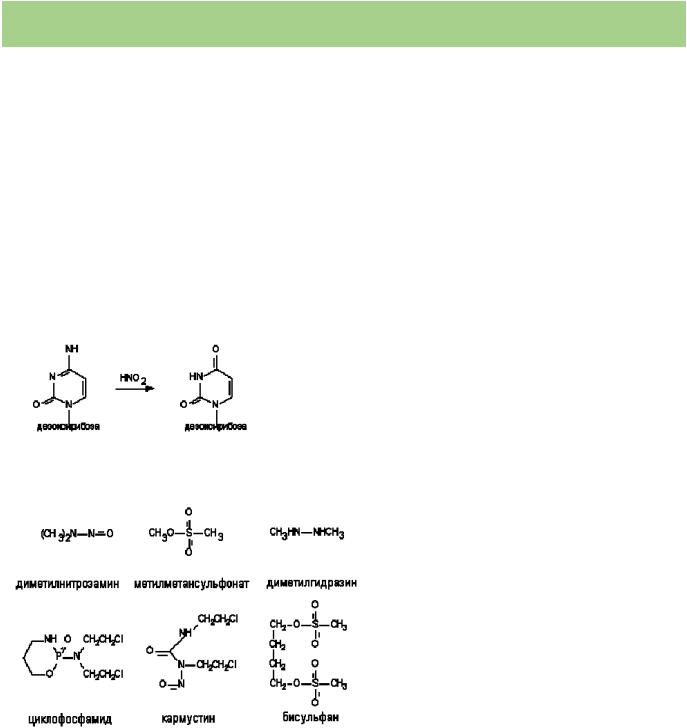
Примером химической модификации нуклеотида является изменение нуклеотида азотистой кислотой. HNO2 способна превращать цитозин в урацил или аденин в гипоксантин (см.
рисунок).
Алкилирующими агентами называются вещества, способные ковалентно присоединять алкильные радикалы к активным группам нуклеотидов ДНК. Такой способностью обладают сернистый и азотистый иприты,
многие промышленные токсиканты, лекарственные (противоопухолевые) препараты (производные дихлорэтиламина: циклофосфамид, мелфалан; производные нитрозомочевины: кармустин, ломустин; алкилсульфонаты: бисульфан; цисплатин).
Некоторые вещества, используемые в настоящее время в качестве противоопухолевых средств, являются структурными аналогами пуриновых и пиримидиновых оснований, входящих в ДНК. Поступая в организм, они включаются в синтез ДНК опухолевыми клетками, замещают нуклеотиды, вызывая летальные мутации.
Выпадение или включение дополнительного нуклеотида.
Выпадение или включение дополнительного нуклеотида в структуру ДНК кардинальным образом изменяет триплетный код, с помощью которого храниться информация о последовательности аминокислот в синтезируемом белке. Это приводит к "сдвигу" всей последовательности нуклеотидов.
Репарация ДНК. Клетки обладают способностью корректировать и устранять повреждения ДНК. Вследствие этого лишь небольшое число мутаций, инициированных токсикантом, сохраняется в процессе репликации молекулы. Гликозилазы расщепляют связи между азотом-9 пурина, подвергшегося алкилированию, образуя участки депуринизированной ДНК. Фрагменты нуклеиновой кислоты, состоящие, как правило, из 3 - 4 нуклеотидов, включая депуринизированный участок, вырезаются из цепи с помощью эндонуклеаз. В дальнейшем удаленные фрагменты заполняются при участии ферментов ДНК-полимераз и "встраиваются" в общую цепь с помощью ДНК-лигаз. Сбои в этом механизме могут приводить к повреждению генетического кода клеток.
2.Хромосомные аберрации
Для обозначения процессов, приводящих к делеции (выпадению), перестройке фрагментов хромосом или появлению дополнительных хромосом, которые выявляются с помощью световой микроскопии клеток, используют термин - кластогенез. Наиболее частой формой кластогенеза являются разрывы хромосом, которые вызываются, например, действием ионизирующего излучения и многих химических веществ. Алкилирующие агенты, особенно содержащие две функциональные группы в молекуле (сернистый, кислородный, азотистый иприты и их производные), образуя поперечные связи с обеими цепочками молекулы ДНК, могут вызвать её разрыв. В основе разрыва лежит депуринизация поврежденных нуклеотидов соседствующих фрагментов обеих нитей ДНК, с последующим их одновременным вычленением с помощью эндонуклеаз.
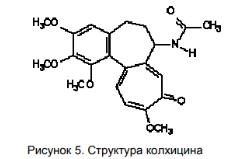
Увеличение числа хромосом в клетке может явиться следствием нарушения процесса их разделения в ходе митоза между двумя дочерними клетками. В итоге образуются клетки с большим или меньшим числом хромосом. Иногда кратно увеличивается весь набор хромосом. Это явление называется - полиплоидия. Ряд химических веществ вызывают полиплоидию. К числу наиболее изученных относится колхицин. Колхицин блокирует митоз в метафазе, вызывая полиплоидию поврежденной клетки.
Условия действия мутагенов на клетки Все клетки организма находятся в одной из фаз клеточного цикла:
1. Покоя (фаза G0): клетка функционирует или покоится (большинство соматических неделящихся клеток);
2. Синтеза клеточных компонентов, необходимых для последующего синтеза ДНК (фаза G1): идет накопление необходимого количества пуриновых и пиримидиновых оснований и других химических компонентов ДНК;
3.Синтеза ДНК (фаза S): осуществляется "сборка" новой молекулы ДНК из наличествующих в клетке компонентов;
4.Синтеза клеточных компонентов для митоза (фаза G2): в частности синтезируется мономеры и полимер тубулина и т.д.;
5.Митоза (фаза M): разделение генетического материала между вновь образующимися дочерними клетками; клеточное деление.
Циклонеспецифичные вещества вызывают мутацию лишь тех клеток, которые находятся в определенной фазе цикла; нециклоспецифичные – на все клетки, независимо от фазы.
Изучение мутагенной активности
Изучение мутагенной активности химических веществ осуществляется в опытах in vitro на прокариотических и эукариотических клетках, путем непосредственного изучения степени повреждения ДНК и выявления хромосомных аберраций у животных, подвергшихся действию токсикантов.
1. Исследования в опытах на прокариотах. Тест Эймса
В основе теста лежит способность мутагенов вызывать обратную мутацию измененного штамма Salmonella typhimurium, неспособного к биосинтезу гистидина. Микроорганизмы данного штамма не растут в среде, не содержащей гистидин, однако под влиянием мутагенов вновь приобретают эту способность.
2. Исследования в опытах на клетках млекопитающих
Исследования по оценке мутагенности обычно проводят, изучая изменения резистентности клеток к: 8-азагуанину или 6-тиогуанину (определяется активностью гипоксантин-гуанин- фосфорибозилтрансферазы - ГГФРТ); бромдезоксиуридину или трифтортимидину (определяется активностью тимидинкиназы - ТК); оуабаину (определяется активностью Na/К-АТФазы).
ГГФРТ регулирует инкорпорацию пуринов из среды в клетку. Мутация локуса ДНК, ответственного за синтез энзима, приводит к угнетению ферментативной активности, прекращению транспорта пуринов в клетку, в том числе и их токсичных аналогов. Мутация локуса ДНК, ответственного за синтез ТК, делает клетку не чувствительной к токсическому действию токсичных аналогов пиримидина.
3. Оценка индукции синтеза ДНК клетками млекопитающих
Принцип метода заключается в оценке интенсивности репаративных процессов, инициируемых химическим повреждением ДНК. В основе метода лежит авторадиографическое определение степени инкорпорации меченного тритием тимидина в ядра клеток, предварительно обработанных исследуемым веществом.
4. Исследование ковалентного связывания токсикантов
Поскольку многие мутагены способны образовывать ковалентные связи с пуриновыми и пиримидиновыми основаниями молекул ДНК, выявление аддуктов ДНК является прямым свидетельством генотоксичности ксенобиотика. Неинвазивные методы предполагают выявление аддуктов в моче животных, подвергшихся воздействию токсикантов; инвазивные - выделение органов и тканей отравленных животных, экстракцию из гомогенатов тканей ДНК и нуклеотидов, с последующим их химическим (иммунохимическим) анализом.
5. Изучение хромосомных аберраций
Хромосомные аберрации, вызванные действием химических веществ, могут быть выявлены путем окрашивания клеток и последующего изучения с помощью обычного светового микроскопа. Для исследования могут использоваться культуры клеток (например, яичника китайского хомячка), обработанные изучаемым токсикантом, клетки костного мозга или лимфоциты периферической крови млекопитающих, которым токсикант вводили in vivo.
Вопрос№4: Химическийканце.Характеристикаогенез канцерогенов, классиф.Стадиканцерогенезакация механизмыдействия.Выявлениеканцерогеннойактивности веществ.Оценрискахимическогоканцерогенеза.
Характеристика канцерогенов
Канцерогеныхимические вещества, воздействие которых достоверно увеличивает частоту возникновения опухолей или сокращает период их развития у человека или животных. Развивающиеся под их влиянием эффекты носят отсроченный характер и являются следствием, как правило, длительного кумулятивного действия в малых дозах.
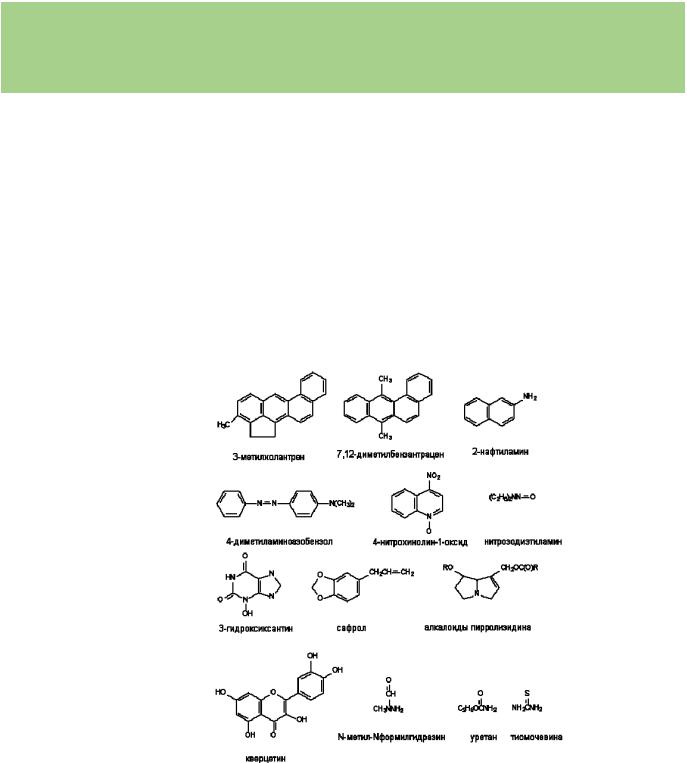
К канцерогенам относятся вещества, имеющие совершенно различное химическое строение/ Среди них ПАУ и гетероциклические соединения, ароматические азосоединения, ароматические аминосоединения, нитрозоамины и нитроамины, металлы, металлоиды и неорганические соли и др.
В ряде случаев канцерогенез есть результат сочетанного действия ксенобиотиков. Так, ведущим канцерогенным фактором для человека является табачный дым. Показано, что около 90% случаев рака лёгких есть следствие неумеренного курения. Канцерогенными свойствами обладают некоторые вещества природного происхождения, например афлатоксины (провоцируют развитие рака печени).
Классификация
Предложено классифицировать канцерогены по происхождению, химической структуре, степени участия в различных стадиях развития рака, по степени доказанности их канцерогенной активности.
По происхождению:
1)Природные канцерогены- вещества, содержание которых в среде не зависит от деятельности человека. Их вклад в онкозаболеваемость считается незначительным. Полициклические ароматические углеводороды (ПАУ), мышьяк, асбест, афлатоксины, радионуклиды и др. Иногда канцерогены естественного происхождения могут накапливаться в организмах живых существ и растениях и по пищевым цепям попадать в организм человека (токсины сине-зеленых водорослей, афлатоксины).
2)Канцерогены антропогенного происхождения
По канцерогенной активности выделяют три группы канцерогенов:
1)Вещества и факторы, для которых имеются безусловные доказательства опасности возникновения опухолей у человека.
2)факторы, которые "вероятно" (т.е. с высокой степенью доказанности) или "возможно" (с меньшей степенью доказанности) канцерогенны для человека. Эта группа делится на 2 подгруппы: 2А - 51 фактор (акрилонитрил, формальдегид, диметилсульфат, нитрозодиэтиламин и др.) и 2Б - 192 фактора (кобальт, ДДТ, акриламид, нитропирены, ПХБ и др.)
3)446 химических веществ, которые на основании имеющихся данных, не могут быть отнесены к факторам канцерогенного риска для человека.
4)агенты, для которых существуют убедительные доказательства отсутствия канцерогенной опасности для человека
Стадии канцерогенеза
Индукция опухолевого роста химическими веществами - сложный, многостадийный процесс, включающий взаимодействие факторов окружающей среды и эндогенных факторов. Особенностью химического канцерогенеза является длительный период, отделяющий воздействие вещества, вызывающего опухолевый рост от появления опухоли. Канцерогенез проходит через 3 стадии развития опухоли:
1-инициация (процесс непосредственного действия канцерогена на клетки, запускающий их трансформацию)
2- промоция (процесс, в ходе которого инициированная клетка завершает неопластическую трансформацию)
3- прогрессия (процесс приобретения клетками нормальной или патологически изменённой ткани организма (в том числе доброкачественной опухоли) свойств злокачественной опухоли).
Механизмы действия
-Увеличение скорости и объема захвата канцерогенов клетками
-Интенсификация процессов биоактивации проканцерогенов в организме
-Подавление процессов биологической детоксикации канцерогенов
-Угнетение механизмов репарации поврежденной ДНК
- Усиление процессов превращения повреждений ДНК в перманентное состояние
Также выделяют генетические и эпигенетические механизмы |
химического |
канцерогенеза. Вещества, действующие на геном клетки |
называются |
"генотоксическими агентами", вещества, провоцирующие опухолевый рост через иные механизмы (повреждение механизмов генной экспрессии, иммуносупрессию, нарушение гормонального баланса)- "эпигенетическими агентами".
Оценка риска химического канцерогенеза
Принципиальная задача оценки риска химического канцерогенеза - установление его количественных характеристик для лиц, контактирующих с малыми дозами потенциальных канцерогенов. Основным является экспериментальный подход к решению задачи. Для этого необходимы количественные характеристики увеличения частоты опухолевого роста при длительном действии вещества в малых дозах, в которых он может действовать в реальных производственных, бытовых, экологических условиях. Однако поскольку при действии в малых концентрациях положительный (канцерогенный) эффект в эксперименте выявляется редко, для получения статистически достоверного результата требуется, либо ввести в опыт очень большое количество животных, что трудно выполнимо, либо изучать зависимость "доза-эффект" при высоких дозах токсиканта, а затем математическими методами экстраполировать полученный результат к малым дозам. Опыты с "большими" дозами токсикантов могут быть выполнены на относительно малом количестве животных и в ограниченные сроки. Существует ряд математических, статистических и других подходов к анализу экспериментально полученного фактического материала, позволяющих, в известной степени, преодолеть эту трудность. После получения расчетной информации о вероятной частоте формирования новообразований при низких, реально встречающихся в практике, уровнях воздействия потенциального канцерогена, можно установит допустимую концентрацию токсиканта (ПДК) по канцерогенному эффекту либо условно безопасную дозу токсиканта (УБД).
Дополнительными подходами к процессу оценки риска канцерогенеза, являются учет времени между моментом действия токсиканта и развитием эффекта, а также фармакокинетических особенностей канцерогена.

Вопрос№5: |
Понятизбирательнойтоксичности.Раздражающее |
|
действие.Краткхарактерхимичесяф зистикаихо |
- |
|
химичетокссвойств.Паикантовх генезксического |
|
|
эффекта.Основныепроявленияраздражающегодействия. |
|
|
Избирательная токсичность- способность химич. веществ оказывать токсич. воздействие на определённые жизненно важные клетки организма, не затрагивая др. виды клеток, а также на определённые группы организмов.
Раздражающее действие- избирательное действие химических веществ на нервные окончания, разветвляющиеся в покровных тканях, сопровождающееся рядом местных и общих рефлекторных реакций и субъективно воспринимаемое, как неприятное чувство покалывания, жжения, рези, боли.
Наиболее чувствительными к раздражению являются покровные ткани, в которых плотность нервных окончаний выше, где они более доступны действию химических веществ (конъюнктива глаз, слизистая дыхательных путей). Покровные ткани этих органов имеют особенности строения, иннервации и потому неодинаково чувствительны к различным веществам. Отдельные токсиканты вызывают преимущественное раздражение органа зрения и условно обозначаются как слезоточивые (лакриматоры), другие - слизистой дыхательных путей (стерниты).
Краткая характеристика химических и физико-химических свойств токсикантов
Раздражающее действие характерно огромному количеству веществ: галогены, альдегиды, кетоны, пары кислот, ангидриды кислот и др. Выраженность эффекта в каждом конкретном случае определяется строением токсиканта, его концентрацией и местом аппликации. К веществам с избирательным раздражающим действием можно отнести лишь те, для которых концентрация местного (раздражающего) действия в тысячи раз меньше среднесмертельной. Вещества, обладающие раздражающим действием, как правило, плохо растворимы в воде, но хорошо в органических растворителях. Они могут быть газообразными, жидкими и твердыми. Боевые отравляющие вещества при обычной температуре окружающего воздуха, по большей части, находятся в твердом состоянии. Их применение сопряжено с необходимостью использования специальных устройств для создания аэрозолей.
Кчислу веществ с высокой раздражающей активностью, прежде всего, относятся:
1.Алифатические и ароматические галогенированные кетоны;
2.Производные нитрилов;
3.Ароматические мышьякорганические соединения;
4.Эфиры форбола и дитерпеновые эфиры;
5.Другие ароматические и гетероциклические соединения.
