
КР2 ответы
.pdf
1Механизмы. токсическдействия.Определениеонятияго "рецептор"втокс.Типыкологецептор.Взаимои действие токсрецепторамиикантов разныхтипов.
Механизм токсического действия – взаимодействие токсиканта (или продуктов его превращения) со структурными элементами биосистем, лежащее в основе развития токсического процесса. Физико-химическое и химическое взаимодействие.
Рецепторы – это участки относительно специфического связывания на биосубстрате ксенобиотиков (или эндогенных молекул), при условии, что процесс связывания подчиняется закону действующих масс (н/р, молекулы белков, нуклеиновых кислот, полисахаридов, липидов или их фрагменты).
Типы рецепторов:
1.1) Активный рецептор – структурный компонент биологической системы, взаимодействие которого с токсикантом инициирует токсический процесс.
1.2) "Немой" рецептор – структурный компонент биологической системы, взаимодействие которого с веществом не приводит к формированию ответной реакции (например, связывание мышьяка белками, входящими в состав волос, ногтей).
2.1) Селективные рецепторы – элементы биологических систем, обладающие наивысшим сродством к отдельным специальным биорегуляторам (гормоны, нейромедиаторы).
2.2) Постоянные рецепторы - это селективные рецепторы, строение и свойства которых кодируется с помощью специальных генов или постоянных генных комплексов
-рецепторы нейромедиаторов и гормонов
-белки-ферменты
-транспортные белки
2.3) Рецепторы с изменяющейся структурой – антитела и антигенсвязывающие рецепторы Т-лимфоцитов. Формируются в клеткахпредшественниках зрелых клеточных форм вследствие индуцированной рекомбинации генов, контролирующих их синтез. Если рекомбинация осуществилась в процессе дифференциации клеток, то в зрелых клетках будут синтезироваться рецепторы только определенного строения.
Формируются селективные рецепторы к конкретным лигандам, а пролиферация приводит к появлению целого клона клеток, содержащих эти рецепторы.
Структура-мишень – структурный элемент, взаимодействуя с которым токсикант инициирует токсический процесс.
•токсическое действие вещества выражено тем сильнее, чем большее количество активных рецепторов (структур-мишеней) вступило во взаимодействие с токсикантом.
•токсичность вещества тем выше,
- чем меньшее его количество связывается с «немыми» рецепторами,
-чем эффективнее оно действует на активный рецептор (структуру-мишень),
-чем большее значение имеет рецептор и повреждаемая биологическая система для поддержания гомеостаза.
Мишенями (рецепторами) для токсического воздействия могут быть:
•структурные элементы межклеточного пространства;
•структурные элементы клеток организма;
•структурные элементы систем регуляции клеточной активности.

2Механизмы. токсическогодейс.Действвиянаикантае элементымежклеточногопростран,действтоксикнатваентов структурэлемклеток. нтыые
Механизм токсического действия – взаимодействие токсиканта (или продуктов его превращения) со структурными элементами биосистем, лежащее в основе развития токсического процесса. Осущ за счет физхим и хим р-ий,обусловлен растворением в опр.средах (водной или липидной) клеток/тканей орг-ма. Особенность:нет четкой зависимости качества развивающегося эффекта от химических свойств молекулы токсиканта.)
Действие токсиканта на элементы межклеточного пространства:
-Электролитные эффекты: нарушение электролитного состава наблюдается при отравлении веществами, способными связывать ионы: F-, Na2ЭДТА, ДТПА, этиленгликоль;
-рН-эффекты: нарушение кислотно-основных свойств внутренней среды организма (н/р, выпил метанол → образовалась муравьиная кислота → ацидоз);
-Связывание и инактивация структурных элементов межклеточной жидкости и плазмы крови: Факторы свертывающей системы крови, гидролитические ферменты (эстеразы), разрушающие ксенобиотики и т.д. Угнетение активности карбоксилэстераз плазмы крови, разрушающих фосфорорганические соединеня (ФОС), три-окрезилфосфатом (ТОКФ), приводит к существенному повышению их токсичности;
-Нарушение осмотического давления крови и интерстициальной жидкости при интоксикациях носят вторичный характер (нарушение функций печени, почек, токсический отек легких).
Действие токсикантов на структурные элементы клеток:
Взаимодействие токсикантов с белками: денатурация белка, блокада его активных центров, связывание активаторов и молекул, стабилизирующих протеин, и т.д.
•К числу веществ, денатурирующих белки, относятся концентрированные щелочи, кислоты, окислители, ионы тяжелых металлов;
•В основе денатурации лежит повреждение внутрибелковых связей, поддерживающих вторичную, третичную структуру протеина;
•При этом наиболее часто токсиканты взаимодействуют с СООН-, NH-, OH-, SH-группами аминокислот, образующих белки
•Токсиканты, связывающиеся с SH-группами, называются тиоловыми ядами: тяжелые металлы (ртуть, мышьяк, сурьма, таллий), органические соединения этих металлов (метилртуть, люизит и т.д.)

3Механизмы. измененкаталитическойактивностиферментовя вусловияхдействтоксикантов. я Угнекаталиентической активности.
|
Механизмы |
|
I |
II |
III |
Усиление каталитической |
Угнетение каталитической |
Изменение конформации |
активности |
активности |
ферментов |
|
- угнетение синтеза ферментов |
|
- усиление синтеза ферментов |
- ускорение разрушения |
|
- блокада разрушения |
ферментов |
|
ферментов |
- угнетение специфической |
|
- активация ферментов |
активности |
|
I Усиление каталитической активности
может быть вызвано поступлением в организм токсикантов-индукторов Физиологическими индукторами синтеза энзимов являются многие субстраты и вещества, повышающие содержание коэнзимов в биосредах
Активность фермента зависит от наличия в биосредах кофакторов или простетических групп. Функции кофакторов выполняют различные витамины и ионы металлов. Их поступление в организм необходимо, однако передозировка сопровождается интоксикацией. Особенно опасно перенасыщение организма жирорастворимыми витаминами (А (ретинол), Д). Стойкое повышение содержания
ионов кальция в цитоплазме клеток, отмечаемое при интоксикациях некоторыми веществами, сопровождается чрезмерной активацией ряда ферментов.
Существенное влияние на активность ферментов оказывают вещества, блокирующие процессы их разрушения.
Разрушение SH-содержащих энзимов иногда начинается с окисления этих групп. Ксенобиотики с высоким восстановительным потенциалом, защищая сульфгидрильные группы, могут предотвращать разрушение энзимов.( карбамилфосфаты)
Разрушение SH-содержащих энзимов иногда начинается с окисления этих групп. Ксенобиотики с высоким восстановительным потенциалом, защищая сульфгидрильные группы, могут предотвращать разрушение энзимов.
механизмы активации лизосомальных ферментов, вызывающих, при выходе в цитоплазму, аутолиз клеток. Посредством такого механизма действуют на организм многочисленные вещества, например, иприты, СCl4, и т.д.
Угнетение каталитической активности:
Снижение активности энзимов при действии токсикантов может быть следствием трех эффектов: подавления процессов синтеза апофермента и кофакторов, активации разрушения, угнетения специфической активности.
К числу наиболее распространенных кофакторов, помимо металлов, относятся железопорфирины, флавины, никотинамид-адениндинуклеотид (НАД), пиридоксальфосфат, тиаминпирофосфат и др. Частично эти вещества синтезируются в организме животных и человека, частично попадают с пищей в форме витаминов.
Пример:
Дикумарол конкурентно препятствует утилизации печенью витамина К, необходимого для синтеза протромбина, поэтому через 24 - 96 ч после поступления вещества в организм в токсических дозах возможно развитие кровотечений угрожающих жизни.
Кчислу полностью синтезируемых в организме кофакторов относятся железопорфирины. Блокада их синтеза приводит к тяжелым последствиям. Так, хроническое отравление свинцом сопровождается нарушением синтеза гема, вследствие чего развивается дефицит гемопротеинов (гемоглобина, миоглобина, гем-содержащих энзимов).
Активация процесса разрушения энзимов токсикантами, как механизм их токсического действия, встречается редко. Катаболизм некоторых энзимов усиливается на фоне хронической интоксикации стероидными препаратами и их аналогами.
Механизмы ингибиторного действия ксенобиотиков:
1. Конкурентное ингибирование: конкуренция токсиканта с субстратом за активный центр фермента.
При этом реализуются две возможности:
а) токсикант вступает в превращение вместо субстрата (конкурентные субстраты ПРИМЕР :эфиры холина (пропионилхолин, бутирилхолин и др.) гидролизуются ацетилхолинэстеразой вместо ацетилхолина); б) взаимодействие токсиканта с активным центром не приводит к его метаболизму (стабильные
ингибиторы) ПРИМЕР карбаматы - ингибиторы холинэстеразы.
Конкурентный тип ингибирования развивается также при образовании прочных ковалентных связей между токсикантами и активными центрами некоторых энзимов. Этот вид ингибирования приводит к полному прекращению ферментативной активности. Таким способом фосфорорганические соединения взаимодействуют с ацетилхолинэстеразой.
Часто, конкурентные ингибиторы энзимов структурно напоминают их субстраты 2. Неконкурентное ингибирование: токсикант взаимодействует с добавочным, аллостерическим,
центром энзима, изменяя при этом конформацию активного центра и снижая, тем самым, его сродство к субстрату. (примермышьяк и его соединения - угнетает активность SH-содержащих фер-тов)
3. Прочие. Для осуществления ферментативной активности необх-мо присутствии в среде ионов металлов: Mg2+, Ca2+, K+, Mn2+, Zn2+, Co2+ и др. Связывание этих металлов токсикантами приводит к угнетению активности. Таков механизм токсического действия комплексообразователей (ЭДТА, ДТПА,
дитизона и др.), салициловой кислоты и др. Особое токсикологическое значение имеют вещества, взаимодействующие с железом, кобальтом, медью, входящими в структуру более сложных простетических групп энзимов (гем-содержащие, цитохромы, каталаза, пероксидаза, гемоглобин, миоглобин).
Кчислу подобных токсикантов относятся цианиды, сульфиды, азиды, монооксид углерода и др.

4Механизмы. токсическогодействия.Взаим действие токснуклеиниантовкислотами. выми
Взаимодействие токсиканта или продуктов его превращения в организме со структурными элементами биосистем, лежащее в основе развивающегося токсического процесса, называется
механизмом токсического действия.
Взаимодействие осуществляется за счет физико-химических и химических реакции. Токсический процесс, инициируемый физико-химическими реакциями, как правило, обусловлен растворением токсиканта в определенных средах (водной или липидной) клеток и тканей организма. При этом существенно изменяются физико-химические свойства среды-растворителя (рН, вязкость, электропроводность, сила межмолекулярных взаимодействий и т.д.). Особенность данного типа взаимодействия - отсутствие строгой зависимости качества развивающегося эффекта от химических свойств молекулы токсиканта. Таким образом, действуют на ткани все кислоты, щелочи, сильные окислители, некоторые органические растворители и лишенные специфической активности высокомолекулярные соединения.
Чаще в основе токсического действия лежат химические реакции токсиканта с определенным структурным элементом живой системы. Структурный компонент биологической системы, с которым вступает в химическое взаимодействие токсикант, называется его "рецептором" или "мишенью".
Взаимодействие токсикантов с НК
Дезоксирибонуклеиновые кислоты - основной компонент хромосомного аппарата клеток. Рибонуклеиновые кислоты представлены информационной, транспортной, рибосомальной РНК. Их функция участие в синтезе белка. Многие ксенобиотики вступают во взаимодействие с нуклеиновыми кислотами, изменяя их свойства:
1. Химическая модификация нуклеиновых кислот.
К числу веществ, вступающих в химическое взаимодействие с нуклеиновыми кислотами, относятся нитриты, этиленимин, гидразин и его производные, соединения мышьяка и др. Образуют ковалентные связи с аминогруппами пуриновых и пиримидиновых оснований. Измененные ДНК могут подвергаться дальнейшей ферментативной и неферментативной трансформации вплоть до разрушения под воздействием эндонуклеаз. Вещества с бифункциональными активными группами (иприты) могут образовывать с двунитевой молекулой ДНК перекрестные связи, при этом становиться невозможным расхождение нитей "двойной спирали", необходимое для обеспечения синтеза белков, клеточного деления.
Токсиканты (формальдегид) способны вступать во взаимодействие не только с пуриновыми и пиримидиновыми основаниями, но и с углеводно-фосфатной основой молекулы нуклеиновой кислоты. При этом происходит её денатурация.
2. Нарушение конформации нуклеиновых кислот.
Многие ксенобиотики образуют нековалентные связи с ДНК. Так, известно высокое сродство к нуклеиновым кислотам производных акридина, которые, встраиваясь в молекулу ДНК между соседними парами оснований (интеркалация), изменяют её структуру. Таков же, вероятно, механизм действия этидиумбромида, профлавина и др. Антрациклин, хлорахин, актиномицин и некоторые другие антибиотики также изменяют конформацию нуклеиновых кислот, не образуя с ними ковалентных связей.
5Механизмы. токсическогодействия.Взаим действие токслипидамикантовмембран,взаимодействиеток икантов селективнымирецеп торамембран. и
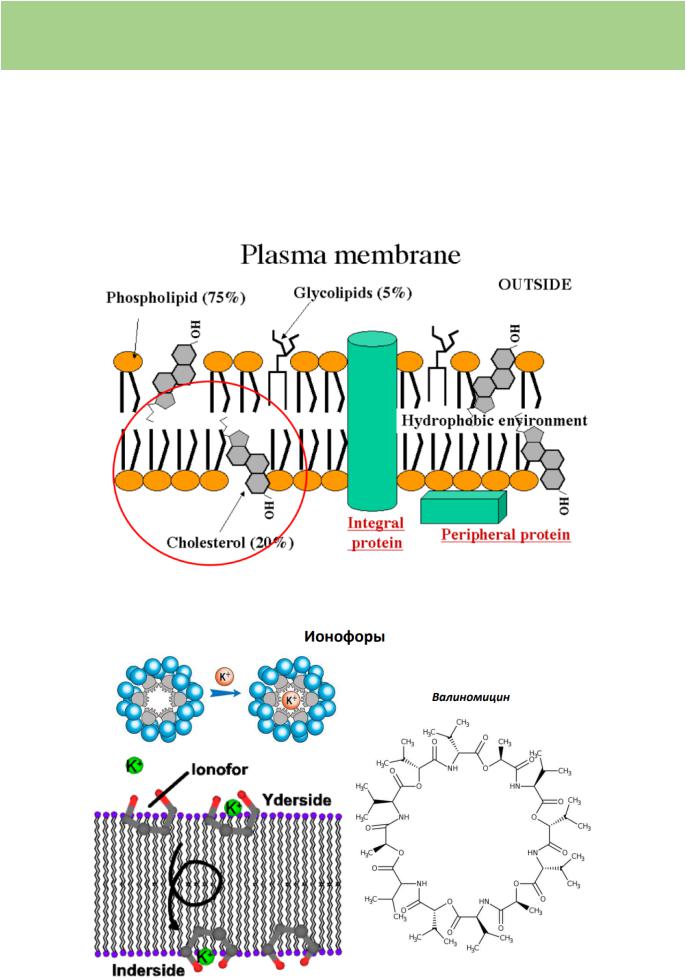
Взаимодействие токсикантов с липидами мембран
Мембранотоксиканты - вещества, разрушающие или изменяющие структуру липидов, нарушающие взаимодействие между молекулами липидов (гидрофобные связи): многие спирты, предельные и галогенированные углеводороды, детергенты (ПАВ), а также яды, обладающие фосфолипазной активностью (яды змей и т.д.). Ряд токсикантов оказывает опосредованное мембранотоксическое действие, повышая уровень внутриклеточного Са2+, активируя эндогенные фосфолипазы, свободнорадикальные процессы в клетках.
Валиномицин имеет циклическое строение и может вмещать в себя ионы K+. Связывание K+ => неконтролируемый перенос К+ в клеточной мембране => гибель бактериального патогена.
Взаимодействие токсикантов с селективными рецепторами

Селективные рецепторы клеточных мембран - это белки, встроенные в липидные бислои. Гидрофобный участок a-спирали белков обеспечивает их прочную связь с мембраной, гидрофильный участок располагается за пределами липидного бислоя и обеспечивает связь рецептора с лигандом, то есть формирует рецепторную область.
Типы селективных рецепторов мембран:
1)формирующие ионные каналы;
2)связанные с G-белками;
3)обладающие тирозинкиназной активностью;
4)образующие межрецепторные сети.
Рецепторы, формирующие ионные каналы
Участвуют в передаче нервных импульсов в ЦНС и на периферии. Рецепторы данного типа состоят из нескольких субъединиц пронизывающих всю толщу биологической мембраны. Одна-две из этих субъединиц представляют собой собственно рецепторную область, связывающуюся с лигандом. Другие субъединицы после взаимодействия рецепторной области с лигандом изменяют свою конформацию и участвуют тем самым в формировании ионного канала.
Примеры: Н-холинорецептор (Na+), ГАМК-эргический, глицинэргический рецепторы (Cl- ). Курарин, никотин, анабазин действуют на Н-холинорецепторы; бициклофосфаты, норборнан действуют на ГАМК-рецепторы, стрихнин действует на рецепторы к глицину.
Рецепторы, связанные с G-белками
Сигналы, вызванные действием лиганда, приводят к конформационным изменениям рецепторного белка, затем переносятся на белки сопряжения, которые в свою очередь, или стимулирует, или угнетает эффекторную систему в целом.
Белки сопряжения в ходе передачи сигнала связывают молекулу гуанозинтрифосфата (ГТФ) и расщепляют её не гуанозиндифосфат и фосфат. Стимулирующие G-протеины (GS), активируют в ходе передачи сигнала аденилатциклазу клеток-эффекторов, а ингибиторные (GI) – угнетают.
Холерный и коклюшный токсины вызывают АДФ-рибозилирование GS-протеина после его связывания с молекулой ГТФ. В итоге развивается стойкая активация аденилатциклазы и перевозбуждение соответствующих клеток слизистых оболочек.

Многочисленные лекарственные средства (действующие на холинэргические, катехоламинэргические, серотонинэргические синапсы), интоксикация которыми развивается как при перевозбуждении, так и блокаде рецепторов. Сюда относится большая группа веществ, обладающих психодислептической активностью (диэтиламид лизергиновой кислоты, псилоцибин, буфотенин, мескалин, хинуклидинилбензилат - BZ и т.д.)
Антитела
Антитела (имунноглобулины, lg) – особый класс гликопротеинов, присутствующих на поверхности B-лимфоцитов в виде мембранносвязанных рецепторов и в сыворотке крови и тканевой жидкости в виде растворенных молекул и обладающих способностью очень избирательно связываться с конкретными видами молекул – антигенами. Используются иммунитетом для идентификации и нейтрализации чужеродных объектов. Функции:
1.антиген-связывающая;
2.эффекторная (способность вызывать иммунный ответ).
Приобретенный иммунный ответ возникает благодаря уникальному процессу соматической перегруппировки генных сегментов (V, D, J, C) иммуноглобулинов и рецепторов Т-клеток, ответственных за синтез молекул антител или рецепторов Т-клеток, в результате чего создается разнообразие распознающих элементов, перекрывающих все существующие в природе антигены.
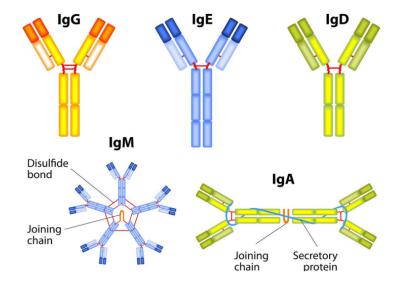
IgE - молекулярная масса 190000, прочно связывается с клетками тканей, с тканевыми базофилами, принимает участие в реакции гиперчувствительности немедленного типа. IgE играет защитную роль при гельминтозах и протозойных болезнях, способствует усилению фагоцитарной активности макрофагов и эозинофилов. Увеличение содержания этого иммуноглобулина при аллергических заболеваниях и миеломной болезни используется в качестве диагностического теста.
Рецепторы, образующие межрецепторные сети
Связывание с лигандом в данном случае не приводит непосредственно к передаче сигнала на эффекторную систему. Процесс восприятия сигнала связан с образованием межрецепторных цепей на поверхности клеток. Наилучшим образом в группе рецепторов данного типа изучены рецепторы к Fc-фрагменту (fragment crystallizible) антител (иммуноглобулинов). Эти рецепторы представляют собой агрегаты двух или более белковых субъединиц, молекулярная масса которых составляет около 30000 – 50000.
Особое патофизиологическое значение имеет образование межрецепторных сетей IgE-Fc- рецепторов, поскольку это явление, наступающее вследствие связывания антигена с молекулами фиксированных на мембранах тучных клеток антител, приводит к экзоцитозу гистаминсодержащих гранул. Экзоцитоз биологически активных веществ, и в частности, гистамина из тучных клеток – основа анафилактических реакций.
