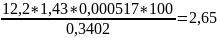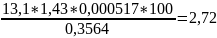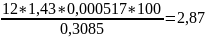Вычисление результатов анализа
Количество миллилитров раствора соли Мора, пошедшее на титрование после окисления гумуса, отвечает тому количеству хромовой кислоты, которое осталось неизрасходованным в процессе окисления.
И. В. Тюрин указывает, что устойчивые результаты получаются тогда, когда на титрование остатка хромовой кислоты после окисления органического вещества идет не менее 20 мл 0,1 н. раствора соли Мора, иначе говоря, концентрация CrO3 не должна быть к концу окисления ниже 0,2 н. Количество соли Мора, отвечающее тому количеству хромовой кислоты, которое пошло на окисление гумуса пробы, определяют вычитанием из результатов холостого титрования результатов титрования после окисления гумуса.
При вычислении содержания органического углерода и гумуса приняты следующие величины: 1 мл 0,1 н. раствора соли Мора соответствует 0,0003 г органического углерода или 0,000517 г гумуса (1 г углерода соответствует 1,724 г гумуса).
Формула вычисления содержания гумуса (в % к воздушно-сухой почве) следующая:
Гумус = (а - b)*К*0,000517*100 / P, где а — количество 0,1 н. раствора соли Мора, пошедшее на титрование 10 мл 0,4 я. раствора K2Cr2O7 при холостом анализе, мл; b — количество 0,1 н. раствора соли Мора, пошедшее на титрование после окисления гумуса, мл; (а - b) — количество 0,1 н. раствора соли Мора, отвечающее количеству хромовой кислоты, израсходованному на окисление гумуса, мл; К — поправочный коэффициент к титру раствора соли Мора; 0,000517 — количество гумуса, соответствующее 1 мл 0,1 н. раствора соли Мора, г; P — навеска воздушно-сухой почвы, г.
Если результаты анализа желательно выразить в углероде, то вместо 0,000517 (коэффициента перевода на гумус) следует поставить величину 0,0003, так как 1 ли 0,1 н. раствора соли Мора соответствует 0,0003 г органического углерода.
Для пересчета содержания гумуса в процентах на почву, высушенную при 105° С, определяют влажность в отдельной навеске почвы и в вычисление вводят соответствующий коэффициент.
Для работы удобна следующая форма записи: 1. Холостой анализ. На титрование 10 мл 0,4 н. раствора K2Cr2O7 идет 45,0 мл раствора соли Мора 0,102 н. (среднее из трех определений). 2. Результаты анализа почв:
Номер анализа |
Глубина пробы, см |
Воздушно-сухая навеска, г |
Количество соли Мора, пошедшее на титрование после окисления гумуса, мл |
Количество соли Мора, отвечающее количеству хромовой кислоты, израсходованному на окисление гумуса, мл |
Гумус, % к воздушно-сухой почве |
1 |
6 |
0,3402 |
37,2 |
37,2-25=12,2 |
|
2 |
6 |
0,3564 |
38,1 |
38,1-25=13,1 |
|
3 |
6 |
0,3085 |
37 |
37-25=12 |
|
Реактивы
Раствор двухромовокислого калия 0,4 н. (окислитель): 40 г измельченного в ступке R2Cr2O7 растворяют в дистиллированной воде, фильтруют через бумажный фильтр в мерную колбу на 1 л, доводят до черты, после чего переносят в колбу из тугоплавкого стекла на 3—5 л или в большую фарфоровую чашку, где смешивают с 1 л H2SO4 (уд. вес 1,84). Во избежание сильного разогревания жидкости при смешивании серную кислоту следует приливать к водному раствору K2Cr2O7 понемногу, с интервалами в 15—20 мин. и при осторожном перемешивании. Смеси дают остыть, вновь тщательно перемешивают и переливают для хранения в склянку с притертой стеклянной пробкой.
Раствор соли Мора 0,1 н. готовят из расчета: 40 г соли Мора в 1 л воды, содержащей 20 мл серной кислоты (уд. вес 1,84). Навеску продажной соли Мора растворяют на холоду в некотором количестве дистиллированной воды, раствор фильтруют через складчатый фильтр. К фильтрату добавляют необходимое по расчету для данной навески количество серной кислоты, доводят раствор дистиллированной водой до заданного объема, после чего тщательно перемешивают. Раствор соли Мора хранят в бутыли, снабженной сифоном со стеклянным краном для подачи раствора в бюретку и склянкой Тищенко с щелочным раствором пирогаллола для предохранения раствора соли Мора от окисления кислородом воздуха.
Раствор дифениламина (индикатор при титровании раствором соли Мора): 0,5 г дифениламина растворяют в 100 мл H2SO4 (уд. веса 1,84); к раствору постепенно, с большой осторожностью, добавляют 20 мл дистиллированной воды.
Раствор фенилантраниловой кислоты (индикатор при титровании раствором соли Мора): 0,2 г ее растворяют в 100 мл 0,2%-ного водного раствора Na2CO3; для лучшего смачивания порошка фенилантраниловой кислоты навеску ее предварительно растирают стеклянной палочкой в фарфоровой чашке с небольшим количеством 0,2%-ного раствора соды до сметанообразного состояния и только после этого добавляют остальное количество раствора соды при тщательном перемешивании.