
4082
.pdf
31
Ксилит представляет собой бесцветное кристаллическое вещество, растворимое в воде и в ряде органических растворителей. Проявляет значительную реакционную способность, связанную с присутствием пяти гидроксильных групп:
CH2OH
H C OH
HO C H
H C OH
CH2OH .
При нагревании ксилита выше 150°С и под давлением в присутствии катализатора происходит расщепление углерод - углеродных связей и присоединение водорода с образованием этиленгликоля, глицерина, метанола. Ксилит и его ангидрид широко применяются в качестве стабилизаторов и пластификаторов в бумажной промышленности, парфюмерии, при получении целлофана. Ксилит является одним из основных компонентов при получении олиф, ПАВ, лаков, клеев и других веществ.
Моносахариды, получаемые при распаде гексозанов гемицеллюлоз, используют для получения этилового спирта, ацетона, органических кислот, антибиотиков путем размножения соответствующих культур различных микроорганизмов.
Широко используются гемицеллюлозы и при производстве целлюлозы: При сульфатной и сульфитной варках целлюлозы гемицеллюлозы подвергаются деструкции; продукты их распада переходят в раствор. Частично преобразованные гемицеллюлозы соответствуют целлюлозе после ее выделения и оказывают влияние на качество целлюлозы и продуктов ее переработки (бумаги, волокна и др.).
Технические целлюлозы и полицеллюлозы содержат значительное количество гемицеллюлоз: сульфитная целлюлоза – до 6,7%, сульфатная – до 8%. Для сульфатных целлюлоз характерно наибольшее содержание остатков ксиланов, для сульфитных и бисульфитных – маннанов.
Гемицеллюлозы оказывают различное влияние на свойства продуктов, получаемых из целлюлозы. При производстве бумаги небольшое количество гемицеллюлоз улучшает ее качество, придают бумаге плотность и прозрачность. Присутствие гемицеллюлоз увеличивает скорость набухания и фибриллирования волокон целлюлозы, что снижает время ее размола и уменьшает энергозатраты. Присутствие небольшого количества гемицеллюлоз в целлюлозе увеличивает прочность бумаги, но в то же время чрезмерное содержание гемицеллюлоз приводит к уменьшению прочности бумаги.
Бумага, полученная из сильно размолотой целлюлозы с высоким содержанием гемицеллюлоз, похожа на пленку и называется растительным пергаментом. Присутствие гемицеллюлоз в целлюлозе, предназначенной для химической переработки, отрицательно влияет на ее качество.
32
Лекция 4
Химия лигнина
Пл а н
1.Общие сведения о лигнине. Распространенность лигнина в природе и его роль в растениях.
2.Строение лигнина. Структурные звенья макромолекулы лигнинов и типы химических связей в макромолекулах. Функциональные группы лигнинов.
3.Физические и физико-химические свойства лигнина.
4.Химические реакции лигнина.
Общие сведения о лигнине
Лигнины представляют собой аморфные высокомолекулярные соединения ароматической природы, построенные из фенилпропановых звеньев. Для макромолекул лигнинов характерны нерегулярные строения и поливариантность связей.
Термин лигнин происходит от латинского названия дерева lignum. Макромолекула лигнина образована не из однородных структурных
единиц, как целлюлоза, а из нескольких различающихся производных фенилпропана. Многообразие связей, которые возникают при образовании лигнина в растениях между его структурными элементами производит к нерегулярности строения лигнина как полимера.
Лигнины различных растений заметно отличаются друг от друга. Их можно подразделить [1] на три основных класса: лигнины хвойной древесины, лигнины лиственной древесины и лигнины травянистых растений.
Лигнины накапливаются в растениях в процессе лигнификации в срединной пластинке и в клеточной стенке. Окончание процесса лигнификации обычно совпадают с прекращением жизнедеятельности клетки. Установлено, что лигнин является необратимым конечным продуктом обмена (метаболизма) в растениях.
Природные лигнины, содержащиеся в растительных тканях, очень подвержены различным воздействиям и могут легко изменяться под действием повышенной температуры и различных реагентов. Даже мягкое химическое воздействие на природный лигнин приводит к его изменению. Поэтому до настоящего времени нет метода, позволяющего полностью выделить лигнин из растения, не изменив его химических и физических свойств.
Природные лигнины обладают рядом специфических свойств. Они легко окисляются. На этом свойстве основан процесс отбелки целлюлозы и получения ряда ценных продуктов, например, ванилина и др. Способность легко взаимодействовать с хлором позволяет использовать хлорирование лигнина при отбелке целлюлозы. Растворимость лигнина в щелочах при нагре-
33
вании используется в натронном и сульфатном способах производства целлюлозы. Способность лигнина растворяться в сернистой кислоте и ее солях применяется при сульфитном способе производства. Природный лигнин в большинстве случаев нерастворим в органических растворителях.
Распространенность лигнина в природе и его роль в растениях
Лигнин входит в состав всех наземных растений. Он отсутствует только в водорослях. Изучение процесса эволюции растений показывает, что лигнификация возникла у растений в связи с переходом к наземному образу жизни.
В клеточных стенках лигнин играет роль цементирующего вещества, которое скрепляет полисахаридные структуры и заполняет пустоты между фибриллами целлюлозы и гемицеллюлоз. Таким образом, лигнин придает стволам и стеблям растений механическую прочность и устойчивость. Кроме, того, лигнин защищает целлюлозные волокна от воздействия различных микроорганизмов.
Древесные клетки, содержащие значительное количество лигнина и образующие проводящую систему древесины, обладают благодаря присутствию лигнина гидрофобностью.
Строение лигнина
Как уже говорилось, макромолекулы лигнинов построены из звеньев фенилпропана.
В качестве элементарных звеньев в структуре лигнина можно выделить
следующие (рис.6) структуры:
α β γ α β γ α β γ
|
|
|
С–С–С |
С–С–С |
С–С–С |
|||||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
1 |
|
|
|
|
|
|
|
|
|
6 |
2 |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
3 |
|
|
|
Н3СО ОСН3 |
|
||
|
4 |
|
|
|
||||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
ОСН3 |
ОН |
ОН |
|||
|
|
|
ОН |
|
|
|
|
|||||
4-окси-3метокси- |
4-окси-3,5-диметокси- |
n- оксифенилпропан |
||||||||||
фенилпропан (I) |
фенилпропан (II) |
(III) |
||||||||||
ОН |
НО |
ОН |
|
|
|
ОН |
ОН |
пирокатехин (IV) |
пирогаллол (V) |
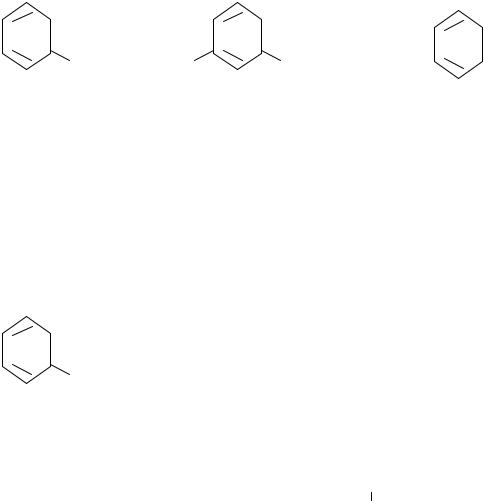
Рис. 6 |
Элементарные звенья структуры лигнина |
34
Для лигнинов хвойной древесины основными элементами являются производные структуры (I), а для лиственной древесины – наряду со структурой (I) и структуры (II). В лигнины однолетних растений наряду со структурами (I) и (II) входят структуры (III).
Кроме того, в состав лигнина хвойной древесины входят производные пирокатехина (V), а лиственной – производные пирокатехина (IV) и пирогаллола (V).
Предшественниками образования этих структур лигнина в растениях являются
СН=СН–СН2ОН |
СН=СН–СН2ОН |
СН=СН–СН2ОН |
||||||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОСН3 |
Н3СО |
|
ОСН3 |
|
|
|
|||
|
||||||||||
ОН |
|
|
ОН |
|
ОН |
|||||
конифериловый |
синаповый |
|
n-кумаровый |
|||||||
спирт |
|
|
спирт |
|
спирт |
|||||
Рис.7 Первичные структуры, предшествующие образованию лигнина |
||||||||||
СН3 |
|
При образовании макромолекул лигнинов пропа- |
||||||||
|
|
|
||||||||
НС–OR |
|
новая цепочка может принимать различные варианты. |
||||||||
HC–OR1 |
Некоторые варианты строения элементарных звеньев |
|||||||||
лигнина хвойной древесины можно представить фор- |
||||||||||
|
|
|
||||||||
|
|
мулой (рис.8):где R,R1,R2 - радикалы (арил или алкил). |
||||||||
|
|
|
||||||||
|
|
|
|
|||||||
|
ОСН3 |
Рис.8 Фрагмент макромолекулы лиственного |
||||||||
ОR2 |
|
|
|
|
лигнина |
|
|
|
||
Следует отметить, что лигнины лиственных пород значительно больше отличаются друг от друга, чем лигнины хвойных пород.
Схема фрагмента макромолекулы лиственного лигнина представлена на рис.8.
Между элементарными звеньями в макромолекулах лигнинов существует два типа связей: простые эфирные и углерод-углеродные. В природном лигнине около половины связей приходится на простые эфиры и другая половина - на С–С связи.
Лигнинам присущи функциональные группы, из которых главными являются: а) метоксилы; б) гидроксилы фенольные и алифатические;
в) карбоксилы; г) карбонилы в положениях α-, β-, γ и хинонные.

35
Биосинтез лигнина в высших растениях
Лигнин появляется в растительной клетке на стадии одревеснения. Формирование зрелого древесного волокна проходит через четыре фазы: деление клеток, расширение клеток, утолщение клеточной стенки и лигнификация.
Сточки зрения биохимии процесс одревеснения делят на два этапа:
1)образование первичных структурных звеньев лигнина, таких как n- кумаровый, конифериловый и синаповый спирты;
2)превращение этих структурных звеньев в лигнин.
Исходным веществом, из которого происходит синтез лигнина являются двуокись углерода.
Одним из основных углеводных предшественников лигнина являются D-глюкоза.
Физические и физико-химические свойства лигнина
Природный лигнин в очень незначительной степени растворим в нейтральных органических растворителях, например, в этаноле.
Препараты лигнина растворимы в полярных органических растворителях, а также в водных растворах щелочей. Растворы препаратов лигнина являются истинными растворами.
Природный лигнин по величине молекулярной массы отличается значительной неоднородностью, т.е. полидисперсностью. Средняя молекулярная
масса Mw лигнина ели колеблется от 7000 до 17000.
Как уже было отмечено, физические свойства природных лигнинов легко изменяются при выделении и обработке и зависят от породы древесины и других факторов. Поэтому препараты лигнина, полученные разными способами из различных пород древесины, могут существенно отличаться друг от друга.
Цвет природного лигнина такой же белый, как и целлюлоза. Цвет препаратов лигнина зависит от метода их выделения и изменяется от почти белого до темно-коричневого (у технического гидролизного лигнина).
Как природный лигнин, так и препараты лигнина аморфные вещества. Природный лигнин и растворимые лигнины являются термопластичными полимерами, а нерастворимые лигнины не плавки. Температура плавления (размягчения) лигнинов колеблется в широких пределах – от 125 до
255оС и зависит от молекулярной массы и содержания влаги в лигнине. Плотность различных препаратов лигнина колеблется в пределах от
1,26 до 1,45 г/см3 , т.е. плотность лигнина приблизительно на 10 % меньше плотности целлюлозы (1,58 г/см3 ).
Природный лигнин и его препараты обладают развитой внутренней поверхностью, составляющей 180-280 м2/г.
36
Различные препараты лигнина при комнатной температуре сорбируют большие количества воды.
Лигнин является слабокислым веществом. Лигнин избирательно сорбирует из разбавленных растворов гидроксиды калия, натрия и аммония.
Наличие в молекуле лигнина функциональных групп, способных к сильному межмолекулярному и внутримолекулярному взаимодействию и к диссоциации, приводит к ассоциации лигнинов в растворах и к аномальным явлениям в растворах лигнинов.
Химические реакции лигнина
Окисление лигнина
Окисление лигнина является одним из способов выяснения его строения
иосновным способом удаления лигнина из целлюлозы при отбелке. В кислой
инейтральной средах молекулярный кислород не действует на лигнин, а в щелочной среде окисление протекает легко. При окислении лигнин разрушается и превращается в смесь алифатических и ароматических кислот. Влияние щелочи определяется происходящим щелочным гидролизом макромолекул лигнина. Кроме кислорода для окисления лигнина применяют перманганат калия, оксиды металлов, перекись водорода, озон, азотная кислота хлор
идр.
При окислении лигнина перекисью водорода происходит деструкция лигнина, что облегчает его удаление при отбелке. При глубоком окислении лигнина образуются гликолевая, малоновая, янтарная, яблочная, винная, муравьиная, уксусная и щавелевая кислоты, а также углекислота.
Окисление лигнина имеет важное техническое значение и используется во многих производствах, например, при отбелке целлюлозы растворами хлорной извести, хлоритов, хлором и двуокисью хлора. При отбелке целлюлозы хлором наряду с хлорированием происходит окисление лигнина за счет того, что хлор, взаимодействуя с водой, образует хлорноватистую кислоту, которая выделяет кислород, окисляющий лигнин:
Cl2 + H2O → HCl + HClO;
HClO → HCl + O.
Важное техническое значение имеет получение из лигнина ванилина и его производных.
Превращение лигнина под влиянием кислот
Природный лигнин под влиянием кислот меняет свои свойства, что имеет большое практическое значение. Превращения лигнина зависят от условий реакции и природы реагентов. Так, при нагревании лигнина с НСl в водном диоксане происходит образование кетонов, являющихся моделями лигнина.
37
В кислой среде происходит конденсация по типу образования фенолальдегидных смол. В этом процессе участвуют все функциональные группы ядра и боковых цепей за исключением метоксилов.
При действии на лигнин разбавленных минеральных кислот при температуре 60-200oС происходят реакции гидролитической деструкции и реакции инактивации лигнина. При гидролитической деструкции возрастает содержание фенольных гидроксилов, уменьшается количество карбонилов и в раствор переходят целые фрагменты макромолекулы лигнина.
При реакциях инактивации лигнина происходит накопление в лигнине новых С-С связей, образующих пространственную сетку. При этом может происходить как “редкая сшивка”, так и образование трехмерной жесткой сетки.
Действие на лигнин азотной кислоты
Все виды лигнинов легко взаимодействуют с азотной кислотой. При этом происходит в основном нитрование лигнина, а также могут протекать окисление, деструкция полимера и образование сложных эфиров. Нитрогруппа входит в ароматическое ядро лигнина в разных положениях, а также на место боковой цепи. Это приводит к деструкции молекул лигнина, причем оторвавшаяся цепь окисляется до кислоты.
Процесс нитрования лигнина представлен на рис.9.
|
|
|
|
|
|
С |
|
|
NO2 |
|
||
|
|
|
|
I O2N |
|
|
O2N |
|
|
|||
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОMe |
|
|
OMe |
|||
C |
|
|
|
|
ОR |
|
|
OR |
|
|||
|
|
+ HNO3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С |
|
|
NO2 |
|
||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||
|
OMe |
|
|
|
+ |
|
||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|||||||
OR |
|
|
II |
|
|
|
|
|
|
|
||
|
|
|
|
|
||||||||
|
|
|
|
|
O2N |
ОMe |
O2N |
OMe |
||||
|
|
|
|
|
||||||||
|
|
|
|
|
|
ОH |
|
|
OH |
|
||
|
|
|
|
|
|
C |
|
|
|
|
|
|
I R = C |
|
|
|
|
|
|
||||||
II R = H
O2N О
О
Рис.9 Нитрование лигнина
38
При обработке лигнина как концентрированной, так и разбавленной азотной кислотой наблюдаются значительная потеря метоксильных групп и увеличение карбоксильных групп. Нитролигнин представляет собой оранжевый легко растирающийся порошок, растворимый в спирте, ацетоне, щелочах и очень плохо растворимый в воде, эфире, бензине.
Реакция нитрования также имеет техническое значение. Нитролигнин является эффективным регулятором глинистых растворов, применяемых при бурении нефтяных и газовых скважин.
Хлорирование лигнина
Хлор легко реагирует с лигнином и способен делигнифицировать растительные материалы при низких температурах. Образующийся оранжевого цвета хлорлигнин легко растворяется в растворах щелочей. Этот метод делигнификации нашел применение при получении целлюлозы из соломы.
Взаимодействие лигнина с хлором сопровождается выделением хлороводорода, что указывает на реакцию замещения водорода.
Реакции, протекающие при хлорировании, можно разделить на две группы:
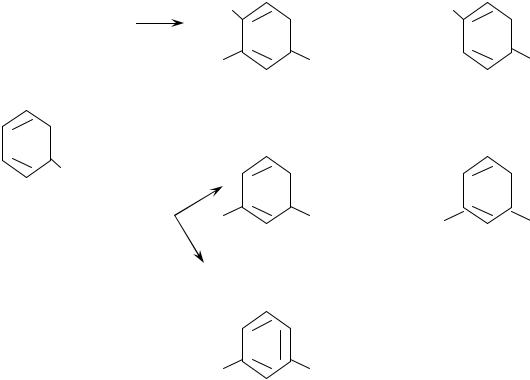
1)реакции собственно хлорирования, когда хлор внедряется в боковую пропановую цепочку и в ароматическое ядро преимущественно в положении 6;
2)реакции окислительно-гидролитической деструкции, катализируемые хлором, которые приводят к расщеплению как эфирных, так и С-С связей в макромолекулах лигнина.
Хлорирование применяется как одна из ступеней в многоступенчатой отбелке целлюлозы. Она заключается в обработке целлюлозы хлорной водой и газообразным хлором при температуре 5-25оС.
Хлорирование лигнина используется для получения холоцеллюлозы, а также для количественного определения содержания целлюлозы в древесине.
Расщепление лигнина металлическим натрием в жидком аммиаке
Эта реакция приводит к расщеплению простых эфирных связей в лигнине.
Алкилирование лигнина
Наиболее часто используется метилирование лигнина. При этом происходит замещение водорода гидроксильных групп лигнина на алкильную группу с образованием простых эфиров. Наиболее сильным метилирующим реагентом является диметилсульфат. Он метилирует все гидроксилы – фенольные, энольные, карбоксильные и спиртовые.
39
Сульфирование лигнина
Сульфирование лигнина является одной из наиболее важных реакций лигнита, так как лежит в основе сульфитной варки целлюлозы. При сульфитной варке лигнин под действием бисульфита и свободной сернистой кислоты превращается в растворимые лигносульфоновые кислоты.
Взаимодействие лигнина со щелочью и сульфидом натрия
Гидролиз лигнина водными растворами щелочей составляет основу щелочных методов получения целлюлозы и применяется при получении ванилина.
Главной реакцией, определяющей растворение лигнина в щелочи, в частности при щелочных варках целлюлозы, является щелочной гидролиз эфирных связей в макромолекулах лигнина, в результате чего высвобождается фенольные гидроксилы.
Термическое разложение лигнина
Термическое разложение гидролизного лигнина используется для получения угля в производстве сероуглерода.
Лигнин дает в 1,5 раза больше угля и в 2 раза больше смолы, чем целлюлоза. Кроме угля, смолы и горючих газов, при гидролизе получается водный дистиллят, содержащий уксусную кислоту, муравьиную кислоту, метанол и ацетон.
Лекция 5
Экстрактивные вещества древесины
Пл а н
1.Общие сведения и классификация экстрактивных веществ.
2.Экстрактивные вещества, растворимые в воде.
3.Смолистые вещества: терпены, смоляные кислоты, нейтральные вещества, жирные кислоты, лигнаны.
Общие сведения и классификация экстрактивных веществ
Экстрактивными веществами называют вещества, не входящие в состав клеточной стенки и извлекаемые (экстрагируемые) органическими растворителями, водой или водяным паром. Вещества, извлекаемые органическими растворителями и отгоняемые с паром, обычно называют смолистыми веществами, или смолой.

40
Экстрактивные вещества древесины и коры включают многочисленные компоненты: смоляные и жирные кислоты, алифатические и ароматические углеводороды, фенолы, эфирные масла, терпены, дубители, камеди, красящие вещества и др. Органические растворители извлекают смолы, жиры, воска, фитостерины. Вода экстрагирует из древесины дубители, камеди и красящие вещества.
Содержание смолы в древесине зависит от многих факторов: породы дерева, его возраста, времени года, места и условий произрастания.
Для экстрагирования используют в основном следующие растворители: этиловый эфир, смесь спирта с бензолом, дихлорэтан.
Собственно смола находится в каналах смоляных ходов под давлением окружающий живых клеток. Смола, вытекающая из смоляных ходов при ранении растущего дерева или подсочке, получила название живицы.
Подсочка является одним из промышленных методов получения живицы и осуществляется при помощи специальных срезов до смоляных ходов. Подсочка является одной из форм прижизненного хозяйственного использования леса. Живица (или терпентин) – это вязкая желтоватого цвета жидкость, состоящая в основном из смоляных кислот и терпенов. На воздухе из живицы испаряется скипидар, смоляные кислоты окристаллизовываются и получается баррас. Живицу подвергают перегонке с водяным паром. Отгоняющийся с паром дистиллят представляет собой скипидар – смесь терпенов. Скипидар представляет собой бесцветную или слабожелтую жидкость с сосновым запахом. Не перегоняющаяся с паром твердая смола называется
канифолью.
Живица, полученная путем подсочки с герметичным приемником, содержит 38 % скипидара. В технической живице, поступающей на канифоль- но-терпентиновые заводы, содержание скипидара колеблется от 13 до 25 %.
Экстрактивные вещества, древесины получают различными способами, классификация которых приведена в табл.6 [1].
Таблица 6
Классификация производств по получению экстрактивных веществ
Название производства |
|
Сырье |
|
Продукция |
|
|
1 |
|
2 |
|
3 |
Канифольно-терпентиновое |
|
Живица, баррас |
|
Канифоль, скипидар (живич- |
|
|
|
|
|
|
ные) |
Канифольно-экстракционное |
Смолистая древесина. |
|
Канифоль, скипидар |
||
|
|
|
|
|
(экстракционные) и др. |
Получение |
канифольно- |
Древесина сосны, ели, ли- |
Сульфатное мыло, талловое |
||
скипидарных |
продуктов |
в |
ственницы (отходы |
лесо- |
масло, жирные кислоты, тал- |
сульфатно-целлюлозном |
|
пиления и деревообработ- |
ловая канифоль, скипидар и |
||
производстве |
|
|
ки), черные щелочи |
|
др. |
