
- •Курсовая работа
- •Содержание
- •1. Литературный обзор
- •1.1. Основные свойства полигидроксиалконатов (пга)
- •1.2. Получение полигидроксиалконатов (пга)
- •1.2.1 Культивирование
- •1.2.2 Экстракция пга
- •2. Материалы и методы
- •2.1. Объект исследования
- •2.2. Оборудование
- •3. Получение полимерных фракций
- •3.1 Однократный размол полимера
- •3.2 Двукратный размол полимера
- •3.3 Шестикратный размол полимера
- •3.4 Десятикратный размол полимера
- •3.5 Двадцатикратный размол полимера
- •4. Анализ результатов
- •5. Выводы
- •6. Список литературы
1. Литературный обзор
1.1. Основные свойства полигидроксиалконатов (пга)
На сегодняшний день в мире сложилась сложная ситуация, при которой легкая промышленность потребляет огромное количество не возобновляемых природных ресурсов, производя ежегодно до 300 млн. тонн пластиков и пластиковых отходов [3].
Биополимеры – это ответ на вызов времени, они сходны по свойствам с традиционными полимерами (полиэтилены, полипропилены), однако и вместе с тем легко биоразлагаются, а продукты их распада не накапливаются во внешней среде в виде вредных отходов.
Одна из основных групп биоразлагаемых полимеров, которая сейчас активно исследуется это полигидроксиалконоаты (ПГА) – полиэфиры от гидроксипроизводных жирных кислот, синтезируемые бактериями в качестве запаса углерода и энергии, при отсутствии питательных элементов при значительном избытке углерода.
На рисунке ниже изображены общие структуры ПГА полимеров.
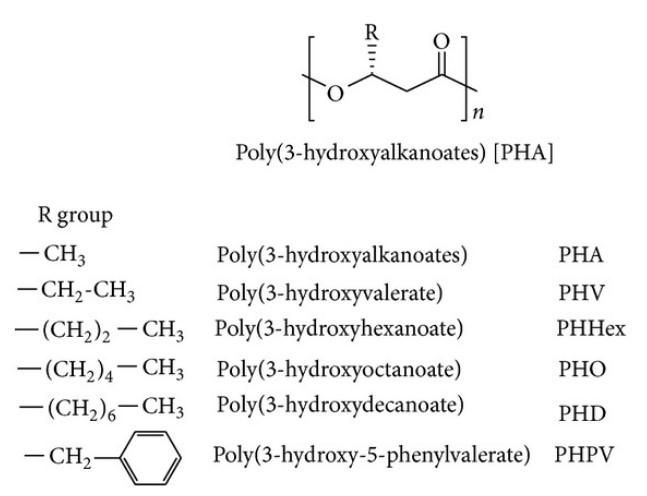
Рисунок 1 – Общая структурная формула полигидроксиалконоатов и их производных
Условно бактериальные ПГА можно разделить на три группы:
1. ПГА с длинной углеродной цепью [6];
2. ПГА со средней длинной углеродной цепи, содержащей обычно 6 – 14 атомов углерода;
3. ПГА с короткой углеродной цепью, содержащей 3 – 5 атомов углерода.
Механические и химические свойства ПГА, зависят не только от длины углеродной цепи, но и от соотношения мономеров. В среднем ПГА содержит несколько тысяч мономеров.
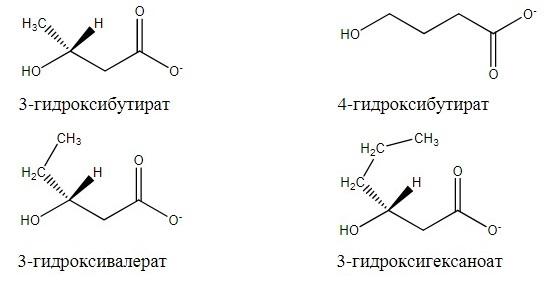
Рисунок 2 – Основные коротко-цепочные мономеры ПГА
ПГА биополимеры находятся в клетках бактерий в виде микрогранул. Количество гранул в клетке может составлять от 2 – 4 до 12 и более. Гранулы заключены в мембрану толщиной 2 – 4 мкм и на 98% состоят из полимера. Основой этих гранул являются полиэфирные белки и липиды. Они образованы фибриллярными структурам, которые представляют собой двойные нити в виде закрученных вправо лент. Последние образуют мицеллообразные кристалы полимера [11]. Особая механическая плотность и гидрофобность полимерных цепей в гранулах связяна с наличием ограничивающих фосфолипидных оболочек под белковыми структурами.
1.2. Получение полигидроксиалконатов (пга)
1.2.1 Культивирование
Для получения биополимера необходимо пройти весь цикл выращивания бактериальной культуры (Cupriavidus Eutrophus) и его дальнейшей экстракции на ферментативной линии.
На первой стадии осуществляется накопление бактериальной биомассы в течении 24 часов до итоговой концентрации в пределах 40 – 50 грамм на литр. Для обеспечения роста культуры используют специальные подпитывающие растворы содержащие соли азота и глюкозу. После достижения оптимальной концентрации начинается следующая стадия.
На второй стадии полностью останавливается подача азота, что приводит к остановке роста концентрации клеток в культуре, начинается процесс накопления полимера в клетках. Оптимальное время необходимое для этой стадии составляет около 30 часов [2].
Основные макроэлементы, необходимые для роста культуры это – углерод, далее – кислород, а также азот [3]. Азот используется микроорганизмами в виде мочевины, аммония или их солей. Другими источниками азота могут являться различные белки, пептоны, аминокислоты и т.д. Соотношение углерода к азоту оказывает существенное влияние на скорость роста микроорганизмов, воздействуя на метаболические пути бактерий [1].
При выращивании микроорганизмов в колбе в околоклеточной жидкости происходит накопление аммиака, что может привести к ингибированию роста культуры. Недостаток азота также является лимитирующим фактором роста бактерий. При наличии углеродного субстрата в достаточном количестве культура начинает накапливать полимер, поэтому следует подбирать оптимальные значения концентрации азотного субстрата и других микро и макроэлементов [4].
