
7
.docxЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Опыт 1. Соединения с комплексным анионом.
Получение комплексного соединения висмута (тетраиодовисмутиата калия)
Ход работы:
В пробирку к 3-4 каплям раствора нитрата висмута прибавляли по каплям 0,5 Н раствор иодида калия до выпадения темно-бурового осадка иодида висмута. Растворили этот осадок, внеся еще несколько капель раствора иодида калия. Раствор стал оранжевого цвета.
Bi(NO3)3 + 3KI = BiI3 + 3KNO3;
BiI3 + KI = K[BiJ4].
K[BiJ4] ↔ K+ + [BiJ4]-- ;
[BiJ4]-- ↔ Bi+3 + 4I-.
Окраска раствора обусловлена присутствием иона J-. Bi+3 - комплексообразователь. J- - адденд. Bi+3 мог бы образовать аквакомплексы [Bi (H2O)4]+3.
Опыт 2. Соединения с комплексным катионом
а) Получение комплексного основания никеля
Ход работы:
Получили осадок гидроксида никеля, внеся в пробирку 3-4 капли раствора сульфата никеля и такой же объем раствора едкого натра. Осадок зеленого цвета. Капиллярной пипеткой удалили жидкую фазу. К осадку добавили 5-6 капель 25% раствора аммиака. Осадок растворился. Ионы Ni в р-ре сульфата никеля зеленого цвета, а ион Ni2+ в [Ni (NH3)6](OH)2 придает раствору голубой цвет.
NiSO4 + 2NaOH → Ni(OH)2↓ + Na2SO4;
Ni(OH)2 + 6NH3 (р-р) → [Ni (NH3)6](OH)2 .
Уравнение диссоциации:
[Ni (NH3)6](OH)2 ↔ [Ni (NH3)6]+2 + 2OH- ;
[Ni (NH3)6]+2 ↔ Ni+2 + 6NH3.
б) Получение комплексного соединения меди с аммиаком
Ход работы:
В пробирку к 5-6 каплям раствора сульфата меди добавили 25% раствор аммиака до полного растворения выпадающего вначале осадка основной соли. Светло-синий цвет полученного раствора обусловлен комплексным ионом меди. К этому раствору прибавили равный объем спирта. Наблюдали образование осадка сульфата тетраамминамеди, который плохо растворим в смеси спирта с водой.
CuSO4 + 2NH3OH = Cu(OH)2 + (NH4)2SO4;
Cu(OH)2 + NH3 (р-р) = [Cu(NH3)4](OH)2;
[Cu(NH3)4](OH)2 ↔ [Cu(NH3)4]2+ + 2OH-- ;
[Cu(NH3)4]2+ ↔ Cu2+ + 4NH3.
[Cu
(NH3)4]
SO4
↔
[Cu
(NH3)4]+2
+ SO
[Cu (NH3)4]+2 ↔ Cu+2 + 4NH3.
Опыт 3. Аквакомплексы
Аквакомплексы кобальта
Ход работы:
В одну пробирку внесли 6-7 капель дистиллированной воды, в другую такой же объем спирта. Добавили в обе пробирки по одному микрошпателю кристаллов шестиводного хлорида кобальта и перемешали растворы стеклянной палочкой. Водный раствор светло-розового цвета, спиртовой раствор малинового цвета. Окраска водного раствора обусловлена присутствием ионов Co2+.
CoCl2 + 6H2O ↔ [Co (H2O)6]Cl2;
[Co (H2O)6]Cl2 ↔ [Co (H2O)6]2+ + 2Cl-- ;
[Co (H2O)6]2+ ↔ Co2+ + 6H2O.
Дегидратация:
[Co (H2O)6]Cl2 → [Co (H2O)4]Cl2 + 2H2O , в присутствии спирта.
Добавили к спиртовому раствору хлорида кобальта 5-6 капель воды. Равновесие сместилось в сторону исходных веществ, в сторону образования [Co (H2O)6]Cl2.
Опыт 4 Комплексные соединения в реакциях обмена.
Взаимодействие ферроцианида калия с сульфатом меди
Ход работы:
В пробирку к 4-5 каплям раствора сульфата меди добавили такой же объем раствора ферроцианида калия K4[Fe(CN)6]. Цвет образовавшегося осадка ферроцианида меди - бурый.
К4[Fe(CN)6] + 2CuSO4→ Cu2[Fe(CN)6]↓ + 2K2SO4;
[Fe(CN)6]4- + 2Cu2+ → Cu2[Fe(CN)6]↓.
Опыт 5. Исследование прочности комплексных ионов. Разрушение комплексов. Диссоциация двойных солей
Ход работы:
В трех пробирках приготовили раствор двойной соли (NH4)2SO4 • FeSO4 • 6H2O (соли Мора), внеся в каждую по 6-8 капель воды и одному микрошпателю соли. В одну пробирку к раствору соли Мора добавили 5-6 капель раствора сульфида аммония, в другую - столько же раствора хлорида бария. В осадок выпали FeS (белые хлопья) и BaSO4(белый).
(NH4)2SO4 • FeSO4 • 6H2O + (NH4)2S = FeS + 2(NH4)2SO4 + 6H2O;
Fe2+ + S2- = FeS.
Реакция указывает на присутствие иона Fe2+.
(NH4)2SO4 • FeSO4 • 6H2O + BaCl2 = BaSO4 + FeCl2 + 6H2O + (NH4)2SO4;
SO42- + Ba2+ = BaSO4.
Реакция указывает на присутствие иона SO42-.
В третью пробирку добавили 7-8 капель 2Н раствора едкого натра и, укрепив в штативе, опустили ее в водяную баню, нагретую почти до кипения. Подержали над пробиркой красную лакмусовую бумажку, смоченную водой. Выделился NH3, лакмус стал синим.
(NH4)2SO4 • FeSO4 • 6H2O + 2NaOH = 2NH4OH + FeSO4 + Na2SO4 + 6H2O;
NH4+ + OH-- = NH4OH.
NH4OH ↔ NH3 ↑ + H2O. (при нагревании).
Реакция указывает на присутствие иона NH4+.
(NH4)2SO4 • FeSO4 • 6H2O ↔ (NH4)2SO4 + FeSO4 + 6H2O.
Соль Мора может быть получена из FeSO4 • 7H2O и (NH4)2SO4.
Проверили действием раствора сульфита натрия, обнаруживается ли присутствие ионов Fe в растворе ферроцианида калия (осадок FeS не выпал, т.к. Fe cвязан сигма-связью с 6 ионами SCN- это устойчивое соединение).
Уравнение диссоциации:
K4[Fe(CN)6]
↔ 4K+
+ [Fe(CN)6]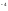 .
.
При диссоциации двойных растворимых солей и комплексов, содержащих устойчивый комплексный ион, существует разница − при диссоциации солей в растворе присутствуют все ионы, составляющие соль, а при диссоциации комплексов в растворе будет присутствовать комплексный ион, поэтому раствор может иметь другие свойства.
Вывод: в результате проделанной работы я изучил несколько видов комплексов, реакции их образования и реакции взаимодействия с некоторыми веществами.
