
6885
.pdfГЛАВА 2
ГОРЕНИЕ ГАЗООБРАЗНЫХ ВЕЩЕСТВ
Горение газовых смесей является гомогенным процессом. Особенностью горения гомогенных систем является наличие критических условий, т.е. определенных, характерных для данной конкретной горючей смеси параметров, вне пределов которых реакция протекает стационарно, без самоускорения, а в их пределах она самоускоряется. К таким параметрам относится: концентрация горючего вещества и окислителя; давление газовой смеси; начальная температура горения; наличие примесей; геометрия сосуда, в котором происходит горение; материал его стенок и некоторые другие параметры.
Переход от медленного процесса к быстрому процессу горения носит резкий характер. Достаточно изменить лишь некоторые параметры.
Время полного израсходования горючего зависит от источника зажигания – его мощности, температуры, площади действия. Если параметры смеси находятся в области воспламенения, то достаточно кратковременного воздействия источника зажигания, чтобы произошло быстрое сгорание смеси.
Характер горения гомогенной газовой смеси
Горение гомогенной газовой смеси зависит от способа подачи воздуха, необходимого для горения. Существуют различные виды сжигания газов. Осуществляют горение предварительно подготовленной горючей газовой смеси, состоящей из окислителя и окисляемого вещества, и горение раздельно поступающих окислителя и горючего газа в зону реакции.
В предварительно перемешанной смеси окислителя и окисляемого веществ – стехиометрической газовой смеси интенсивность горения зависит только от скорости элементарных химических реакций. Такой вид горения называют кинетическим.
31

В стехиометрической газовой смеси реакция идет во всем объеме смеси при выходе из горелки.
Ламинарное и турбулентное горение стехиометрической газовой смеси
Для стехиометрической газовой смеси различают ламинарное и турбулентное горение. При ламинарном движении газа скорость его движения распределяется в горелке по параболе. Это обусловлено тем, что у стенок внутри горелки скорость газа очень мала в результате трения и достигает максимальной скорости на оси горелки. Аналогичное распределение скорости сохраняется и при выходе из горелки (рис. 4).
Поток стехиометрической смеси окислителя и горючего газа
Рис. 4. Ламинарное горение стехиометрической газовой смеси
На выходе из горелки скорость потока равна скорости распространения пламени υпот. = υпл.. Выходной срез горелки нагрет до высокой температуры и обеспечивает непрерывное зажигание стехиометрической смеси окислителя и горючего вещества.
У стенки горелки скорость потока меньше, чем скорость горения, но пламя не может проникнуть внутрь вследствие охлаждения газа ниже разогретого выходного среза горелки, где
υпот. > υпл..
32
В процессе нарастания скорости потока от периферии к центру пламя образует конусообразный факел.
Ламинарное горение стехиометрической смеси характеризуется небольшой высотой пламени, высокой температурой и практически полным сгоранием горючего газа. Эти характеристики являются несомненным достоинством такого горения.
К недостаткам такого вида горелок следует отнести нестабильность пламени. Проскок пламени внутрь или отрыв пламени от устья горелки происходит при малейшем нарушении равенства скоростей движения и горения газового потока υпот. = υпл.
Турбулентное горение однородной газовой наблюдается при высоких скоростях движения газа. Оно используется для интенсификации горения и требует стабилизации пламени. Попутный поток атмосферного воздуха, сопровождающий движение горящего газа, охлаждает зажигающее кольцо горелки. Оно теряет поджигающую способность и факел погасает.
Диффузное горение газа
Диффузное горение газа происходит в случае, когда через горелку подается горючий газ, не смешанный с окислителем. Газ и воздух подаются раздельно, а горение поддерживается в результате взаимной диффузии окислителя и окисляемого вещества. В зависимости от характера движения смешивающихся газов различают ламинарное диффузное горение и турбулентное диффузное горение.
Ламинарное диффузное горение осуществляется в усло-
виях, когда кислород, необходимый для горения, поступает из окружающей атмосферы и смешивается с горючим газом в результате молекулярной диффузии. При круглой горелке формируется конусообразный факел. Горение поддерживается за счет кольцевой зоны зажигания раскаленной верхней кромки газовой горелки. Факел обладает большой устойчивостью. Проскок пламени в горелку исключается из-за раздельной подачи горючего газа и воздуха. Зона устойчивого горения располагается на по-
33

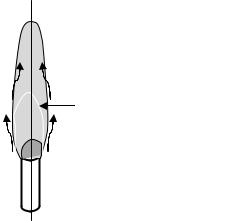
верхности факела, где устанавливается стехиометрическое соотношение между горючим газом и кислородом воздуха. Именно стехиометрическое соотношение обеспечивает устойчивость факела. Реакция горения осуществляется в узкой светящейся зоне фронта горения, которая значительно разбавлена горячими продуктами горения и не превышает по толщине 1 мм. Образующиеся продукты сгорания диффундируют как в окружающее пространство, так и внутрь факела. Поверхность пламени отделяет окислительную область вне факела, в которой имеются кислород и продукты сгорания, но нет горючего газа, от восстановительной области внутри факела, в которой нет кислорода, но есть горючий газ и продукты сгорания (рис. 5).
воздух |
воздух |
Поток горючего газа Рис. 5. Ламинарное диффузное горение газа
Газ, поступающий из горелки в зону горения, нагревается за счет горячих продуктов реакции и подвергается термическому разложению – пиролизу. Так, метан в восстановительной зоне в отсутствии кислорода уже при 680 – 700 оС частично термически распадается с образованием свободного углерода, высокодисперсного углерода (сажи), водорода и трудносжигаемых углеводородов. Доля термической деструкции метана при 950 оС составляет 26%, а при 1150 оС достигает уже 90%.
34
Свободный углерод, раскаленная сажа и другие мелкодисперсные частицы, находящиеся в пламени, излучают яркий свет.
Достоинства ламинарного диффузного горения:
-отсутствие проскока пламени внутрь горелки;
-высокая устойчивость пламени при изменении тепловых нагрузок
-равномерная температура по длине пламени.
Кнедостаткам следует отнести:
-термический распад углеводородов;
-низкая интенсивность горения;
-высокая доля продуктов неполного сгорания горючего
газа.
Турбулентное диффузное горение осуществляется в усло-
виях интенсивного перемешивания горючего газа и кислорода воздуха. Именно этот способ горения широко используется в промышленных теплогенерирующих установках.
Положение зоны воспламенения и горения в турбулентном диффузном горении соответствует месту точек, где образуется смесь стехиометрического состава.
Практика показывает, что выделяющаяся при сгорании газа энергия в форме теплоты посредством диффузии и турбулентной теплопроводности горячих продуктов горения передается горючей смеси, обеспечивая еѐ воспламенение и распространение пламени.
Положение зоны горения определяется условиями турбулентной диффузии, а скорость горения – скоростью диффузии. При наличии турбулентной диффузии фронт горения получается волнистым, размытым на отдельные части и слабо устойчивым.
Ктому же турбулентному диффузному горению присуще неполное сгорание горючего газа и продуктов пиролиза горючего газа.
35
Структура и механизм горения газовых смесей
При вытекании вертикальной газовой струи снизу вверх в
атмосферное пространство образуются зоны горения смеси газов. Смеси с большим содержанием горючего газа условно называются «богатыми», а наибольшая концентрация горючего вещества в смеси с воздухом, при которой еще возможно стойкое, незатухающее распространение горения – верхним концентрационным пределом воспламенения (ВКПВ). Смеси с малым содержанием горючего газа называются «бедными», а наименьшая концентрация горючего вещества в смеси с воздухом, при которой уже возможно стойкое, незатухающее распространение горения – нижним концентрационным пределом воспламенения (НКПВ). Вне этих пределов смеси горючего газа с окислителем (воздухом) не горят.
НКПВ
Т ≈ 1350 – 1550 оС
ВКПВ; Т ≈ 50 оС
Рис. 6. Распределение температур в пламени при горении газообразных веществ
В промежутке между концентрационными пределами горения газовой смеси лежит поверхность стехиометрического состава газовой смеси. В этом тончайшем слое максимальная температура и максимальная скорость горения. Благодаря этому слою устанавливается стационарный режим горения и форма
36

пламени. Ориентировочно максимальная температура пламени в тонком слое стехиометрической смеси для большинства углеводородов равна 1350 – 1550 оС (рис. 6).
Затраты воздуха на сжигание топлива
При горении веществ в воздухе происходит быстрая химическая реакция окисления между горючим веществом и кислородом воздуха с интенсивным тепловыделением. В результате этой реакции образуются в основном оксиды элементов, входящих в состав горючего вещества. При сгорании углеводородов, состоящих из атомов С и Н, образуется СО2 (двуокись углерода) и Н2О (вода). При неполном сгорании наряду с ними образуются СО (окись углерода) и Сn(тв) (углерод) в виде сажи. При написании уравнения горения и составлении материального баланса, как правило, записывают только продукты полного окисления СО2 и Н2О. Если в составе горючего вещества есть сера (S), то при сгорании образуется SО2. Азот (N), входящий в состав горючего вещества, при горении в воздухе не окисляется, а выделяется в виде свободного азота (N2).
С3Н8 + 5О2 |
3СО2 + 4Н2О |
С3Н8 + 5О2 |
3СО2 + 4Н2О |
С3Н6О + 4О2 |
3СО2 + 3Н2О |
СS2 + 3О2 |
СО2 + 2SО2 |
Н2S + 1,5О2 |
Н2О + SО2 |
NН3 + 0,75О2 |
0,5N2 + 1,5Н2О. |
Записанные уравнения химических реакций горения являются брутто-уравнениями, которые показывают только начальное и конечное состояние системы. Они не отражают механизма химического взаимодействия при горении, который достаточно сложен и протекает через ряд промежуточных стадий с участием атомов и радикалов.
37
Уравнение материального баланса процесса горения отличается от уравнения химической реакции тем, что в него для удобства расчетов включают азот, содержащийся в воздухе и не участвующий в химическом превращении. Для расчетов будем принимать, что воздух состоит на 21 % (об.) из кислорода и на 79 % (об.) из азота, т.е. в нем на 1 моль кислорода приходится 79/21 = 3,76 молей азота, поэтому в уравнении материального баланса перед азотом ставят коэффициент 3,76.
Например, уравнение материального баланса для горения пропана будет следующим:
С3Н8 + 5О2 + 5∙3,76N2 3СО2 + 4Н2О + 5∙3,76N2.
Коэффициент, который записывают перед О2 (в данном случае 5) необходимо повторить и перед N2, так как азот и кислород в воздухе неразделимы. Это суммарная реакция, но она достаточна для проведения практических расчетов и является обобщенной записью материального баланса реакции горения.
Уравнение материального баланса позволяет рассчитывать количество воздуха, необходимое для горения любого горючего вещества и количество образующихся продуктов горения.
Минимальный объем воздуха, который необходим для полного сгорания единицы количества горючего вещества, на-
зывается удельным теоретическим объемом воздуха и обознача-
ется voв.В зависимости от единиц измерения количества горючего вещества (1 моль, 1 м³, 1 кг) удельный объем измеряется в м³/моль, м³/м³, м³/кг.
Действительное количество воздуха, который поступает в зону горения, отличается от теоретического. Соответствующий объем называется удельным действительным объемом воздуха и обозначается vв. Разность между количеством воздуха, который идет на горение и теоретически необходимым, называется избытком воздуха. Для характеристики процесса горения исполь-
зуют понятие коэффициент избытка воздуха - αв., который по-
казывает, во сколько раз количество воздуха, который действи-
38
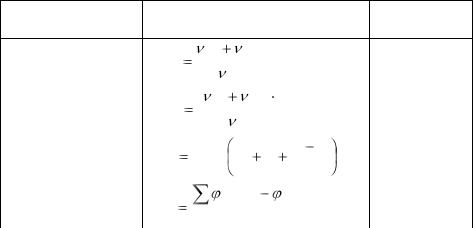
тельно поступает в зону горения, отличается от теоретически необходимого количества для полного сгорания единицы количества горючего вещества.
Таким образом, действительный удельный объем воздуха
равняется:
vв = vов ∙ αв.
Часть воздуха, неизрасходованная на горение, переходит
впродукты горения.
Вслучае кинетического горения при αв = 1 смесь горючего с воздухом является стехиометрической. Величина тепловыделения на единицу продуктов сгорания при этом максимальна, вследствие чего температура в зоне горения также максимальна.
При αв < 1 в смеси имеется недостаток окислителя и излишек горючего вещества. Характерной особенностью процесса горения
вэтом случае является образование продуктов неполного сгора-
ния. При αв > 1 в смеси находится недостаток горючего вещества и излишек окислителя. При этом продукты горения включают в себя избыток воздуха.
Т а б л и ц а 1
Формулы для расчета теоретического объема воздуха
Тип горючего ве- |
Расчѐтные формулы |
Размерность |
щества |
|
|
|
VВ |
0 |
|
|
O2 |
|
N2 |
|
|
|
|
|
|
|
кмоль |
; |
м3 |
|
|||||
Индивидуальное |
|
|
|
|
Г |
|
|
|
|
|
|
кмоль |
м3 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
вещество |
|
|
|
( |
|
|
|
|
|
) |
V |
м3 |
|
|
|
||||||||
|
VВ |
0 |
|
|
O2 |
|
|
N2 |
|
0 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
м |
3 |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
Г M |
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Вещество слож- |
V |
0 |
|
0.269 |
С |
|
Р |
|
S O |
м3 |
|
|
|
||||||||||
ного состава |
В |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
3 |
|
|
|
8 |
|
кг |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Смесь газов |
|
0 |
|
|
|
|
Гi nO2 i |
|
O2 |
м3 кмоль |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
VВ |
|
|
|
|
21 |
|
|
|
|
|
|
|
м3 ; кмоль |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
39 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Для удобства расчѐтов горючие вещества разделяют на три типа (табл.1): индивидуальные химические соединения, вещества сложного состава, смесь газов.
Здесь VВ 0 – теоретическое количество воздуха; νг, νО2, νN2-
количество горючего, кислорода и азота, получаемого из уравнения химической реакции горения, кмоль; М – молекулярная масса горючего; V0 – объем 1 кмоля газа при нормальных условиях (22,4 м3); C, H, S, O – массовое содержание соответствующих элементов в составе горючего, % Гi - концентрация I - го
горючего компонента, % об.; O |
-концентрация кислорода в со- |
|
2 |
ставе горючего газа, % об.; nO2i - количество кислорода, необхо-
димое для окисления одного кмоля i- го горючего компонента, кмоль.
Механизм горения некоторых газов
Целый ряд окислительно-восстановительных реакций протекает таким образом, что вначале в системе образуются свободные атомы и радикалы.
Легкость взаимодействия свободных атомов и радикалов с молекулами-реагентами, сопровождающееся генерированием свободных атомов и радикалов, приводит к цепному взрыву в случае прогрессивно нарастающего количества активных частиц в ходе реакции.
Отступление. Принято неспаренный электрон обозначать точкой. В этом случае атом водорода, содержащий единственный электрон обозначают Н . Атом кислорода содержит в своем составе два неспаренных электрона О . Свободный радикал – это молекула, один из атомов которой содержит неспаренный электрон, например НО .
При контролируемом проведении цепной реакции взрыв исключается, так как происходит регулируемая подача окислителя и окисляемого вещества в зону реакции.
40
