
Кислородсодержащие органические соединения
Спирты,
Простые эфиры,
Альдегиды,
Кетоны,
Карбоновые кислоты, их ангидриды и галогенангидриды
Сложные эфиры,
Фенолы и их простые эфиры.
Спирты
К спиртам относятся соединения, содержащие функциональную группу -OH, связанную с алифатическим радикалом.
Например, CH2=CH-CH2-OH, HC≡C-CH2-OH, CH3-OH.
аллиловый спирт пропаргиловый спирт метанол
В радикал, соединенный с группой –OH, может входить так же остаток ароматического углеводорода, если он отделён, по крайней мере, одной метиленовой группой.
бензиловый спирт
Классификация спиртов
П
 о
типу атомов углерода, контактирующих
с функциональной группой –OH
различают первичные , вторичные и
третичные спирты.
о
типу атомов углерода, контактирующих
с функциональной группой –OH
различают первичные , вторичные и
третичные спирты.

Вторичный спирт
![]()

![]()
Первичный спирт
Третичный спирт
Исключение: CH3-OH (метанол) –он тоже первичный спирт.
По количеству гидроксильных групп различают одноатомные, трёхатомные, многоатомные, полиатомные спирты, например:
(пентанол-3)
одноатомный
двухатомный
(1,2 – этандиол)![]()
![]()
(1, 2, 3 - пропантриол)
глицерин
(пентаэритрит)

трёхатомный
четырёхатомный


многоатомный
(D-сорбит)
полиатомный
(поливиниловый спирт)
Номенклатура и изомерия спиртов
По номенклатуре ИЮПАК в структурной формуле спирта находится самая длинная цепь из атомов углерода, обязательно включающая атом углерода, связанный с гидроксильной группой. Эта цепь нумеруется с той стороны, к которой ближе гидроксил. Сначала называются алкильные радикалы с указанием их места положения в цепи, затем название алкана соответствующего длине выбранной цепи, после чего добавляется окончание спиртов – «ол».
По рациональной номенклатуре атом углерода и связанный с ним гидроксил получают название «карбинол». Сначала называются алкильные радикалы, соединённые с упомянутым выше атомом углерода, а затем слитно слово «карбинол». Ниже в таблице приведены названия спиртов с брутто-формулой С5Н12О по этим видам номенклатур, а также тривиальные (то есть исторически сложившиеся) их названия.
C5H12O |
Название по ИЮПАК |
Рациональное название |
Тривиальное название |
|
Пентанол - 1 |
н- Бутилкарбинол |
Амиловый спирт |
|
Пентанол - 2 |
Метилпропилкарбинол |
- |
|
Пентанол - 3 |
Диэтилкарбинол |
- |
|
2 – метилбутанол - 1 |
Втор - бутилкарбинол |
- |
|
2 - метилбутанол - 2 |
Диметилэтилкарбинол |
Трет – амиловый спирт |
|
3 – метилбутанол - 2 |
Метилизопропилкарбинол |
- |
|
3 – метилбутанол - 1 |
Изобутилкарбинол |
Изоамиловый спирт |
|
2,2 – диметилпропа- нол - 1 |
Трет - бутилкарбинол |
Неопентиловый спирт |
Контрольное задание: написать структурные формулы спиртов C6H14O и дать им названия по номенклатуре ИЮПАК и по рациональной номенклатуре.
Способы получения спиртов
Из алканов. Метан может быть селективно окислен на гетерогенном катализаторе – серебре расчётным количеством кислорода до метанола:

Алканы с большим числом атомов углерода ,такие, например, как пропан и бутан, окисляются до смеси первичных и вторичных спиртов расчётным количеством кислорода в присутствии катализаторов – солей марганца. Реакция малоселективна – получается довольно большое количество примесей: альдегидов и кетонов с тем же числом атомов углерода, альдегидов и спиртов – продуктов деструкции

2. Из алкенов. К любому алкену можно присоединить воду в присутствии кислот

Присоединение идёт по правилу Марковникова.
3. Из алкинов. Ацетилен и терминальные алкины, реагируя с формальдегидом, другими альдегидами и кетонами, дают соответственно первичные, вторичные и третичные спирты



Реакции были впервые опубликованы в 1905 году А.Е. Фаворским и носят его имя.
4. Из алкадиенов. Алкадиены аналогично алкенам присоединяют в присутствии кислот воду.
Присоединение первого моля воды идёт преимущественно в положения 1 – 4. При
присоединении второго моля воды образуются диолы. Ниже представлены примеры обоих
случаев:


5. Из галоидных алкилов. Галоидные алкилы вступают с водными растворами щелочей в реакцию нуклеофильного замещения галогена на гидроксил:


6 .
Из дигалоидных производных.
При действии щелочей на дигалоидные
производные алканов получаются
двухатомные спирты (или диолы):
.
Из дигалоидных производных.
При действии щелочей на дигалоидные
производные алканов получаются
двухатомные спирты (или диолы):
Как показано выше из 1,2-дибромэтана получается 1,2-этандиол (этиленгликоль). Этот диол очень широко применяется для производства антифризов. Например, в незамерзающей жидкости для охлаждения двигателей внутреннего сгорания – «Тосол-А 40» его 40%.
7 .
Из тригалоидных производных.
Из 1,2,3-трихлорпропана, например,
получают широко используемый глицерин
(1,2,3-пропантриол).
.
Из тригалоидных производных.
Из 1,2,3-трихлорпропана, например,
получают широко используемый глицерин
(1,2,3-пропантриол).
8 .
Из аминов. При
нагревании с парами воды в присутствии
катализатора протекает обратимая
реакция, в которой конечными продуктами
являются спирт с тем же строением
углеродного скелета и аммиак.
.
Из аминов. При
нагревании с парами воды в присутствии
катализатора протекает обратимая
реакция, в которой конечными продуктами
являются спирт с тем же строением
углеродного скелета и аммиак.
Первичные амины можно перевести в спирты так же действием нитрита натрия в соляной кислоте при охлаждении до 2 – 5оС:
![]()
9 .
Из альдегидов и кетонов по реакции
Меервейна – Понндорфа – Верлея.
На кетон или альдегид действуют
каким-либо спиртом в присутствии
катализатора – алкоголята алюминия. В
качестве алкоксильных групп берут
остатки того же спирта, который взят в
качестве реагента. Например, в приведённой
ниже реакции вместе с нормальным
бутиловым спиртом взят трибутилат
алюминия. Реакция обратима и равновесие
в ней сдвигают по принципу Ле-Шателье
избытком спирта-реагента.
.
Из альдегидов и кетонов по реакции
Меервейна – Понндорфа – Верлея.
На кетон или альдегид действуют
каким-либо спиртом в присутствии
катализатора – алкоголята алюминия. В
качестве алкоксильных групп берут
остатки того же спирта, который взят в
качестве реагента. Например, в приведённой
ниже реакции вместе с нормальным
бутиловым спиртом взят трибутилат
алюминия. Реакция обратима и равновесие
в ней сдвигают по принципу Ле-Шателье
избытком спирта-реагента.
Первые публикации об этой реакции появились практически одновременно в двух разных немецких и одном французском химических журналах в 1925 – 1926 годах. Реакция имеет огромное значение, так как позволяет восстановить карбонильную группу в спиртовую, не восстанавливая двойные связи, нитро- и нитрозогруппы, которые водородом и другими восстановителями переводятся соответственно в простые связи и аминогруппы, например:

Как видно двойная связь, присутствовавшая в кетоне, сохранилась и в полученном спирте. Ниже показано, что при гидрировании кетогруппы одновременно гидрируется и двойная связь.

Аналогичная картина наблюдается и при наличии в кетоне нитрогруппы: в реакции Меервейна –Понндорфа-Верлея она сохраняется, а при гидрировании водородом на катализаторе восстанавливается до аминогруппы:


10. Из альдегидов и кетонов путём гидрирования на катализаторах – металлах платиновой группы: Ni, Pd, Pt :


11. Получение спиртов из альдегидов и кетонов путём синтезов Гриньяра.
Реакции, открытые Франсуа Огюстом Виктором Гриньяром в 1900 – 1920 годах имеют колоссальное значение для синтезов многих классов органических веществ. Так, например, с их помощью можно из любого галоидного алкила и формальдегида в три стадии получить первичный спирт:
 (1)
(1)


Для получения вторичного спирта надо вместо формальдегида взять любой другой альдегид:
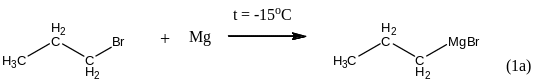

При гидролизе такой соли получается спирт с числом атомов углерода равным сумме их в магнийорганическом соединении и в альдегиде:

Для получения третичного спирта вместо альдегида в синтезе используют кетон:

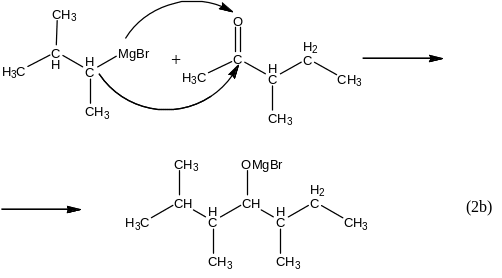

12. Из карбоновых кислот спирты можно получить только в две стадии: на первой из карбоновой кислоты действием пентахлорида фосфора или действием оксиддихлорида серы (IV) получают её хлорангидрид:


На второй стадии, полученный хлорангидрид гидрируют на палладии до спирта:

13. Из алкоголятов спирты очень легко получаются путём гидролиза при комнатной температуре:


Борные эфиры гидролизуются труднее – только при нагревании:

Выпадает в осадок если её больше, чем 4г/100г H2O
14. Из сложных эфиров спирты наряду с карбоновыми кислотами могут быть получены путём автокаталитического, кислотного или щелочного гидролиза. При автокаталитическом процессе в результате очень медленного гидролиза водой появляется слабая карбоновая кислота, которая в дальнейшем ходе реакции играет роль катализатора, заметно ускоряя расход сложного эфира и появление спирта во времени. Например, для реакции втор-бутилового эфира 2-метилпропановой кислоты кинетические кривые, то есть зависимости изменения молярных концентраций во времени представяют собой сигмоиды или S-образные кривые (смотрите график ниже реакции).


15. Если добавить к сложному эфиру сильную кислоту, которая является катализатором, то в
реакции не будет индукционного периода, когда гидролиз почти не идёт (от 0 до 1 времени).
Кинетические кривые в этом случае будут представлять собой экспоненты: нисходящую
для сложного эфира и восходящую для спирта. Процесс называется кислотным гидролизом:

16. Если добавить к сложному эфиру щёлочь (моль на моль или избыток) , то реакция так же описывается экспоненциальными кинетическими кривыми, но в отличие от кислотного гидролиза, где концентрации веществ стремятся к равновесным значениям, здесь конечная концентрация спирта практически равна исходной концентрации эфира. Ниже приведена реакция щелочного гидролиза того же сложного эфира и график с кинетическими кривыми. Как видно щёлочь здесь не катализатор, а реагент, и реакция необратима:


17. Из сложных эфиров спирты можно получить также по Буво и Блану. Этот способ был впервые опубликован авторами в двух разных французских химических журналах в 1903 и 1906 годах и заключается в восстановлении сложных эфиров натрием в спирте, например:

Как видно в реакции получаются два спирта: один из кислотной части сложного эфира и он всегда первичный, второй из спиртовой части и он может быть любым – первичным, вторичным или третичным.
18. Более современный способ получения спиртов из сложных эфиров заключается в восстановлении их комплексными гидридами до алкоголятов (реакция ( 1 ) ), которые затем легко переводятся в спирты путём гидролиза (реакции ( 2а ) и ( 2b ) ), например:


![]()








