
- •Введение
- •4.3. Титриметрический метод анализа
- •4.3.1. Классификация методов титриметрического анализа
- •4.3.2. Стандартизация раствора титранта
- •4.3.3. Кривые титрования
- •4.3.3. Индикаторы титриметриметрических методов анализа
- •4.3.4. Принцип эквивалентности
- •4.3.5. Расчет результата прямого титрования при разных способах выражения концентрации раствора
- •4.3.6. Расчет результата в методе обратного титрования
- •4.4 Кислотно-основное титрование.
- •4.4.1.Общая характеристика метода
- •4.4.2 Индикаторы в методе кислотно-основного титрования
- •4.4.3. Кривые титрования
- •4.4.4 Кривая титрования сильной кислоты сильным основанием ( и наоборот)
- •Расчет кривой титрования 10,0 мл 0,1 м hCl раствором 0,1 м NaOh
- •Титрование сильного основания сильной кислотой
- •Расчет кривой титрования 10,0 мл 0,1 м сh3cooh раствором 0,1 м NaOh
- •4.4.5. Техника выполнения работ в титриметрических методах анализа
- •3. Стандартизация раствора хлороводородной кислоты по тетраборату натрия.
- •4. Определение содержания щёлочи в растворе
- •Контрольные вопросы :
- •Задачи для самостоятельного решения
- •5. Окислительно-восстановительное титрование .
- •5.1.Классификация методов окислительно-восстановительного титрования
- •5.2. Индикаторы окислительно-восстановительного титрования
- •5.3.Перманганатометрия
- •1. Приготовление раствора титранта кМnO4
- •2. Приготовление раствора первичного стандарта
- •3. Стандартизация раствора титранта кМnO4
- •4. Вычисления
- •5) Определение железа (II)
- •6. Физико - химические методы анализа.
- •Определение концентрации ионов меди в растворе
- •4. Определение меди в исследуемом растворе
- •1. Основные понятия аналитической химии
- •2. Методы качественного анализа
- •3. Классификация катионов в качественном кислотно-основном
- •4. Методы количественного анализа
- •4.3. Титриметрический метод анализа
- •4.4 Кислотно-основное титрование.
- •5. Окислительно-восстановительное титрование .
- •6. Физико - химические методы анализа.
- •4.3. Титриметрический метод анализа
- •4.3.1. Классификация методов титриметрического анализа
- •4.3.2. Стандартизация раствора титранта
- •4.3.3. Кривые титрования
- •4.3.3. Индикаторы титриметриметрических методов анализа
- •4.3.4. Принцип эквивалентности
- •4.3.5. Расчет результата прямого титрования при разных способах выражения концентрации раствора
- •4.3.6. Расчет результата в методе обратного титрования
- •4.4 Кислотно-основное титрование.
- •4.4.1.Общая характеристика метода
- •4.4.2 Индикаторы в методе кислотно-основного титрования
- •4.4.3. Кривые титрования
- •4.4.4 Кривая титрования сильной кислоты сильным основанием ( и наоборот)
- •Расчет кривой титрования 10,0 мл 0,1 м hCl раствором 0,1 м NaOh
- •Титрование сильного основания сильной кислотой
- •Расчет кривой титрования 10,0 мл 0,1 м сh3cooh раствором 0,1 м NaOh
- •4.4.5. Техника выполнения работ в титриметрических методах анализа
- •3. Стандартизация раствора хлороводородной кислоты по тетраборату натрия.
- •4. Определение содержания щёлочи в растворе
- •Контрольные вопросы :
- •Задачи для самостоятельного решения
- •5. Окислительно-восстановительное титрование .
- •5.1.Классификация методов окислительно-восстановительного титрования
- •5.2. Индикаторы окислительно-восстановительного титрования
- •5.3.Перманганатометрия
- •1. Приготовление раствора титранта кМnO4
- •2. Приготовление раствора первичного стандарта
- •3. Стандартизация раствора титранта кМnO4
- •4. Вычисления
- •5) Определение железа (II)
- •6. Физико - химические методы анализа.
- •Определение концентрации ионов меди в растворе
- •4. Определение меди в исследуемом растворе
- •1. Основные понятия аналитической химии
- •2. Методы качественного анализа
- •3. Классификация катионов в качественном кислотно-основном
- •4. Методы количественного анализа
- •4.3. Титриметрический метод анализа
- •4.4 Кислотно-основное титрование.
- •5. Окислительно-восстановительное титрование .
- •6. Физико - химические методы анализа.
Расчет кривой титрования 10,0 мл 0,1 м сh3cooh раствором 0,1 м NaOh
|
V(NaOH),мл |
|
|
|
[OH-],моль/л |
pH |
1. |
0,00 |
0,10 |
- |
- |
- |
2,88 |
2. |
2,50 |
0,06 |
0,020 |
3,000 |
- |
4,28 |
3. |
5,00 |
0,03 |
0,030 |
1,000 |
- |
4,76 |
4. |
9,00 |
5 · 10 -3 |
0,047 |
0,100 |
- |
5,76 |
5. |
9,90 |
5 · 10 -4 |
0,050 |
0,010 |
- |
6,76 |
6. |
9,99 |
5 · 10 -5 |
0,050 |
0,001 |
- |
7,76 |
7. |
10,00 |
- |
0,050 |
- |
- |
8,76 |
8. |
10,01 |
- |
0,050 |
- |
5 ·10 - 5 |
9,7 |
9. |
10,10 |
- |
0,050 |
- |
5 ·10 - 4 |
10,7 |
10. |
11,00 |
- |
0,047 |
- |
5 ·10 - 3 |
11,7 |
11. |
15,00 |
- |
0,040 |
- |
0,02 |
12,3 |
В общем случае рН в начале скачка на кривой титрования слабой одноосновной кислоты можно вычислить по формуле
pH = pK + 3
Эта формула получается с учетом того факта, что логарифм отношения количества неоттитрованной кислоты (0,1 %) к количеству полученной соли (99,9 %) в данном случае
![]()
В точке эквивалентности (добавлено 10,0 мл 0,1 М NaOH) рН рассчитывается для гидролизующейся соли CH3COONa по формуле
![]()
За точкой эквивалентности расчет рН ведется аналогичным образом, как и в случае титрования сильной кислоты щелочью. Внешний вид кривой титрования приведен на рис.2.
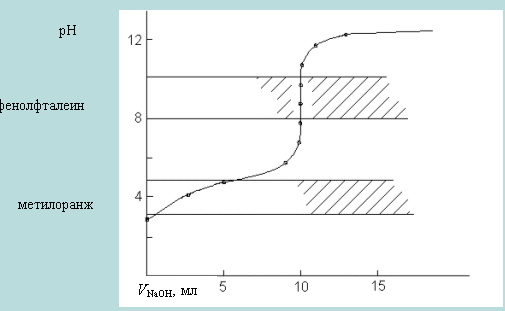
Рис.2 Кривая титрования 10 мл 0,1 М CH3COOH раствором 0,1 М NaOH
Анализ кривой титрования
Характерной особенностью кривых титрования слабых одноосновных кислот является несовпадение точки эквивалентности с точкой нейтральности и расположение точки эквивалентности в щелочной области. Величина скачка на кривой титрования значительно меньше, чем в случае титрования сильной кислоты щелочью. Так, в данном случае рН = рН конца скачка - рН начала скачка = 9,7 - 7,76 = 1,94 вместо 5,4 единиц при титровании 0,1 М HCl раствором 0,1 М NaOH. В данном случае в качестве индикатора можно использовать только фенолфталеин, метиловый оранжевый применять нельзя.
Величина скачка уменьшается с уменьшением концентрации кислоты, с возрастанием температуры, с уменьшением константы диссоциации слабой кислоты. При Kкисл < 10 - 6 скачок исчезает вообще.
