
Тонкая структура спектральных термов.
Исследование спектров щелочных металлов при помощи приборов с большой разрешающей силой показало, что каждая линия этих спектров является двойной (дублет). Так, например, характерная для натрия желтая линия ЗР -> 3S (см. рис. 2) состоит из двух линий с длинами волн 5890 и 5896 Å. То же относится и к другим линиям главной серии, а также к линиям других серий.
Структура спектра, отражающая расщепление линий на компоненты, называется тонкой структурой. Сложные линии, состоящие из нескольких компонент, получили название мультиплетов. Тонкая структура обнаруживается, кроме щелочных металлов, также и у других элементов, причем число компонент в мультиплете может быть равно двум (дублеты), трем (триплеты), четырем (квартеты), пяти (квинтеты) и т. д. В частном случае спектральные линии даже с учетом тонкой структуры могут быть одиночными (синглеты).
Расщепление спектральных линий, очевидно, обусловлено расщеплением энергетических уровней. Для объяснения расщепления уровней Гаудсмит и Уленбек выдвинули в 1925 г. гипотезу о том, что электрон обладает собственным моментом импульса Ms, не связанным с движением электрона в пространстве. Этот собственный момент был назван спином.
Первоначально предполагалось, что спин обусловлен вращением электрона вокруг своей оси. Согласно этим представлениям электрон уподоблялся волчку или веретену. Кстати, отсюда происходит и сам термин «спин»: по-английски spin означает «верчение». Однако очень скоро пришлось отказаться от подобных модельных представлений, в частности по следующей причине. Вращающийся заряженный шарик должен обладать магнитным моментом, причем отношение магнитного момента к механическому должно иметь значение
![]() `
(4)
`
(4)
Действительно, было установлено, что электрон, наряду с собственным механическим моментом, обладает также и собственным магнитным моментом ms. Однако ряд опытных фактов, в частности сложный эффект Зеемана, свидетельствует о том, что отношение собственных магнитного и механического моментов в два раза больше, чем для орбитальных моментов:
![]() .
(5)
.
(5)
Таким образом, представление об электроне как о «вращающемся шарике» оказалось несостоятельным. Спин следует считать внутренним свойством, присущим электрону, подобно тому, как ему присущи заряд и масса.
Предположение о спине электрона было подтверждено большим количеством опытных фактов и должно считаться совершенно доказанным. Оказалось также, что наличие спина и все его свойства автоматически вытекают из установленного Дираком уравнения квантовой механики, удовлетворяющего требованиям теории относительности. Таким образом, выяснилось, что спин электрона является свойством одновременно квантовым и релятивистским. Спином обладают также протоны, нейтроны, фотоны и другие элементарные частицы (кроме мезонов).
Величина собственного момента импульса электрона определяется по общим законам квантовой механики так называемым спиновым квантовым числом s, равным 1/2:
![]() (6)
(6)
Проекция спина на заданное направление может принимать квантованные значения, отличающиеся друг от друга на ħ:
![]() (S=
±1/2). (7)
(S=
±1/2). (7)
Чтобы найти значение собственного магнитного момента электрона, умножим S на отношение (5):
![]() ,
(8)
,
(8)
где б – магнетон Бора.
Проекция собственного магнитного момента на заданное направление может иметь значение :
![]() (9)
(9)
Орбитальный момент количества движения l и спиновой момент s складывается в полный момент количества движения j= l+s по правилам векторного сложения.
Энергия электрона в основном определяется его электростатическим взаимодействием с зарядом ядра. На этот эффект накладывается энергия взаимодействия спина электрона с зарядом ядра. Его называют спин-орбитальное взаимодействие. В его существовании можно убедиться наглядно, воспользовавшись системой координат связанной с электроном. В такой системе ядро движется относительно электрона и создает магнитное поле, которое взаимодействует со спиновым магнитным моментом электрона. Энергия взаимодействия будет разной для различных направлений спинового момента (по полю и против поля H). Формально спин-орбитальное взаимодействие рассматривается как взаимодействие между спиновым и орбитальным магнитными моментами. Из-за спин-орбитального взаимодействия каждый энергетический уровень атома расщепляется на несколько подуровней (мультиплеты), образуя тонкую структуру.
В спектроскопии состояния электронной системы принято описывать следующим набором квантовых чисел: n, l, j, 2s+1.Число 2s+1 – называется мультиплетностью энергетического уровня. Мультиплетность уровня показывает число возможных проекций спинового магнитного момента на заданное направление. Состояние с квантовыми числами n=3, l=0, j=1/2, 2s+1=2 записывается в виде:
32s1/2
С тонкой структурой спектральных термов связано появление тонкой структуры в спектрах свечения и поглощения щелочных металлов. Оно определяется разрешенными переходами между различными подуровнями расщепившихся энергетических уровней (правилами отбора). Для одноэлектронных атомов правила отбора имеют вид:
l= 1
j= 1
Рассмотрим возникновение тонкой структуры в главной серии спектра свечения атомов натрия (рис.2).
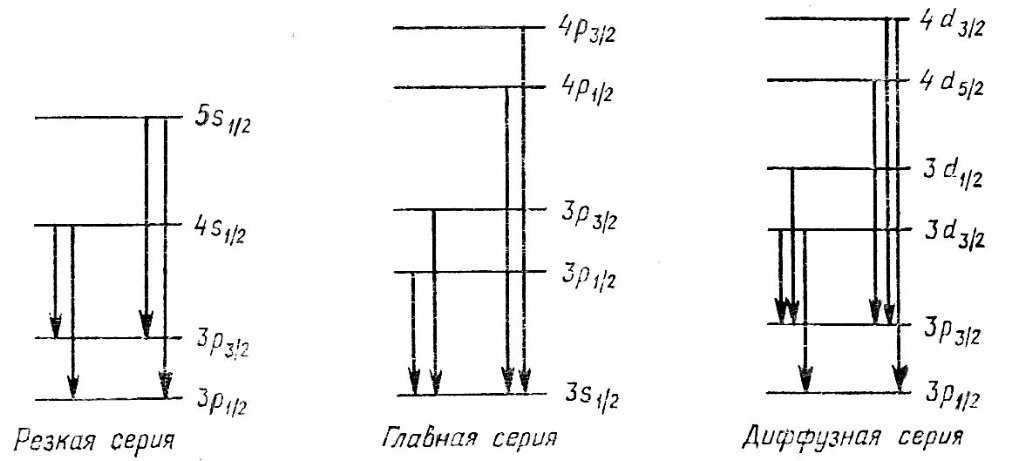
рис.2
Главная серия возникает в результате переходов на наиболее глубокий уровень 3s1/2 с вышележащих р-уровней. Уровень 3s1/2 простой, а все р-уровни - двойные, причем расстояние между компонентами этих уровней убывает с возрастанием главного квантового числа п. Поэтому и сами спектральные линии главной серии получаются двойными — дублетами. Расстояние между компонентами дублета уменьшается с возрастанием его номера (т. е. с увеличением частоты). Главная серия возникает и в спектре поглощения, так как в нормальном состоянии атомы натрия находятся на наиболее низком уровне, т. е. на 3s1/2. Наиболее интенсивной является желтая резонансная линия натрия, возникающая при переходах 3р1/2 3s1/2 и 3р3/23s1/2. Этим переходам соответствуют длины волн 1 = 589,6 нм и 2 = 589,0 нм с разностью между ними = 0,6 нм.
