
- •Методические советы студентам
- •Техника лабораторных работ и безопасность труда
- •Биологическим материалом
- •Реактивами
- •3. Электрическими приборами
- •Центрифугами в лабораторном практикуме
- •5. Газовыми и другими нагревательными приборами
- •6.Водопроводом
- •7. Химической посудой и вспомогательными приспособлениями
- •Занятие № 1 работа № 1. Колориметрия, общий принцип. Устройство фотоэлектроколориметра
- •Принципиальная схема устройства фотоэлектроколориметра
- •Занятие № 2 работа № 1. Цветные реакции на белки и аминокислоты
- •Биуретовая реакция на белки.
- •2. Нингидриновая реакция.
- •Ксантопротеиновая реакция Мульдера (на ароматические аминокислоты).
- •4. Реакция Фоля на цистеин.
- •Работа № 2. Определение общего белка плазмы биуретовым методом
- •Занятие № 3 работа № 1. Осаждение белков концентрированными минеральными кислотами
- •Работа № 2. Разделение альбуминов и глобулинов яичного белка методом высаливания
- •Занятие № 4 работа № 1. Кислотный гидролиз белков
- •Работа № 2. Определение протеолитической активности трипсина
- •Занятие № 5 работа № 1. Влияние температуры на активность амилазы
- •Работа № 2. Влияние активаторов и ингибиторов на активность амилазы слюны
- •Работа № 3. Определение активности амилазы (диастазы) в сыворотке крови и моче по методу каравея
- •Занятие № 6 работа № 1. Кинетика действия липазы. Влияние желчи на активность липазы
- •Занятие № 10 работа № 1. Количественное определение мочевой кислоты в моче
- •Работа № 2. Определение активности цитохромоксидазы
- •Принцип метода:
- •Занятие № 13 работа № 1. Количественное определение макроэргических соединений мышц
- •Занятие № 14
- •Занятие № 16 работа № 1. Качественная реакция на адреналин
- •Занятие № 17 работа № 1. Качественное определение
- •Занятие № 18 работа № 1. Количественное определение витамина с
- •Занятие № 19 работа № 1. Количественное определение глюкозы в крови. Энзиматический (глюкозооксидазный) метод
- •Занятие № 20
- •Занятие № 21 работа № 1. Количественное определение пировиноградной кислоты в моче
- •Занятие № 25 работа № 1. Определение общего холестерина в сыворотке крови (энзиматический метод)
- •Занятие № 26 работа № 1. Определение липопротеинов низкой плотности (лпнп) в сыворотке крови
- •Занятие № 30 работа № 1. Определение мочевины в сыворотке крови
- •Занятие № 34 работа: биохимический анализ мочи
- •Качественная реакция на белок.
- •2. Полуколичественное определение белка.
- •3. Полуколичественное определение глюкозы
- •3. Определение ацетона (кетоновых тел) в моче (экспресс-метод).
- •4. Качественная реакция на кровяные пигменты.
- •Ход работы: взять пробирку: опыт
- •Занятие № 35 работа № 1. Определение гемоглобина гемоглобинцианидным методом.
- •Биохимия нервной системы
- •Занятие № 36 работа № 1: определение глюкозы в спинномозговой жидкости
- •Занятие № 37 работа № 1: определение общего белка в спинномозговой жидкости биуретовым методом
- •Занятие № 38 работа № 1: определение хлоридов в спинномозговой жидкости
- •Референтные величины основных биохимических показателей у взрослых кровь
- •Спинномозговая жидкость
- •Референтные величины основных биохимических показателей крови у детей
Занятие № 10 работа № 1. Количественное определение мочевой кислоты в моче
ОБОСНОВАНИЕ ВЫПОЛНЕНИЯ РАБОТЫ: мочевая кислота образуется из пуриновых оснований (аденин, гуанин). Выделение мочевой кислоты с мочой зависит от содержания пуринов в пище и от состояния обмена нуклеиновых кислот в организме. Мочевая кислота в виде кислого урата натрия входит в состав подагрических отложений в сухожилиях, хрящах, слизистых оболочках суставных сумок. Метаболит существует в виде 2-х таутомерных форм:
 OH O
OH O

 C C
C C
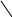 N C N
HN C NH
N C N
HN C NH


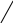 C-OH C = O
C-OH C = O


H
 O
- C C N C C NH
O
- C C N C C NH
 H
H
O
N N
H
Енольная форма Кетонная форма
ПРИНЦИП МЕТОДА: мочевая кислота в щелочной среде восстанавливает фосфорновольфрамовый реактив, который приобретает интенсивный синий цвет. Количество восстановленного фосфорновольфрамового реактива можно определить (титруя) раствором K3Fe(CN)6. При этом синий раствор обесцвечивается. Количество использованного K3Fe(CN)6 эквивалентно содержанию мочевой кислоты.
ХОД РАБОТЫ: взять две пробирки:
Отмерить
|
Стандарт |
Опыт |
Моча Стандартный раствор мочевой кислоты ( 0,5 мг/мл) Раствор NaOH – 20 % раствор Фосфорновольфрамовый реактив |
-
2,0 мл 1,0мл 1,0мл |
2,0 мл
- 1,0 мл 1,0 мл |
Титрование каждой пробы раствором К3Fe(CN)6 до исчезновения синего цвета.
РЕЗУЛЬТАТ: записать объем K3Fe(CN)6, пошедший на титрование.
ВЫЧИСЛЕНИЕ РЕЗУЛЬТАТА. Пример:
На титрование стандарта использовано
2мл K3Fe(CN)6
На титрование опыта – 3 мл K3Fe(CN)6
Составляем пропорцию:
1 мг мочевой кислоты - 2 мл
х мг мочевой кислоты - 3 мл
3 х 1
2 мл мочи содержит = Х = ----------- = 1,5
2
мг/пробе
Суточное выделение мочевой кислоты рассчитывают с учетом суточного диуреза (мужчины –1,5, женщины – 1,2 л.).
ВЫВОД:
КЛИНИКО-ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ:
У взрослых здоровых людей с мочой за сутки выделяется 1,6 – 6,44 ммоль (0,3 – 1,2 г) мочевой кислоты.
Повышенная экскреция мочевой кислоты (гиперурикурия) наблюдается при: заболеваниях, сопровождающихся ускоренной гибелью клеток (терапия раковых и лейкозных больных цитостатиками, гемобластозы, гемолитические процессы, псориаз, синдром длительного сдавления), токсикозах беременности, алкоголизации, потреблении богатых пуринами продуктов (печень, почки, икра рыб)
Пониженное выведение мочевой кислоты (гипоурикурия) отмечается при: почечной недостаточности, подагре, нефритах, отравлениях свинцом и бериллием, синдроме Дауна.
Дата_______________
ЗАНЯТИЕ № 11
САМОСТОЯТЕЛЬНАЯ АУДИТОРНАЯ РАБОТА
ПО ТЕМЕ «БИОСИНТЕЗ БЕЛКОВ»
Дата: _______________
ЗАНЯТИЕ № 12
РАБОТА № 1. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ СУКЦИНАТДЕГИДРОГЕНАЗЫ
ОБОСНОВАНИЕ ВЫПОЛНЕНИЯ РАБОТЫ: СДГ один из ключевых ферментов цикла трикарбоновых кислот, прочно связаный с внутренней мембранной митохондрий. Роль кофермента выполняет ФАД, соединенный с белком ковалентной связью. Фермент in vivo окисляет янтарную кислоту (сукцинат):
ФАД ФАДН2
СООН СООН


 СН2
СН
СН2
СН
СН2 сукцинатдегидрогеназа СН
(СДГ)
СООН СООН
Сукцинат Фумарат
Работа дает представление о дегидрогеназных реакциях в ЦТК.
ПРИНЦИП МЕТОДА:
Субстрат – янтарная кислота. Конечный акцептор водорода – 2,6-дихлорфенолиндофенол (синий цвет), который при восстановлении превращается в бесцветную лейкоформу. Источником фермента является отмытая мышечная ткань. В опыте (in vitro) ход реакций следующий:

Малонат является конкурентным ингибитором фермента СДГ.
ХОД РАБОТЫ:
А. Получение ферментного препарата.
2 г свежих мышц измельчают ножницами, гомогенизируют с небольшим количеством воды. Мышечную кашицу переносят на двойной слой марли (воронка) и промывают 25 мл воды. Отжатую мышечную массу переносят в пробирку, добавляют 4 мл воды, размешивают стеклянной палочкой и суспензию равномерно разливают в 4 пробирки.
Б. Определение активности фермента.
Взять четыре пробирки и приготовить инкубационные смеси в соответствии со схемой:
отмерить |
1 |
2 |
3 |
4 |
Ферментный препарат (гомогенат ткани)
Н2О
Малонат
Сукцинат
2,6-дихлорфенолиндофенол |
1,0 мл кипячение 2 минуты
0,5 мл
-
1,0 мл
2 капли |
1,0 мл -
0,5 мл
-
1,0 мл
2 капли |
1,0 мл -
1,5 мл
-
-
2 капли |
1,0 мл -
-
0,5 мл
1,0 мл
2 капли |
Перемешать. Инкубация 15 минут, при 37о С. в термостате |
||||
РЕЗУЛЬТАТ:
ВЫВОД:

 № пробирки
№ пробирки