
- •Мультиферментные комплексы и изоферменты. Клиническое значение определения активности изоферментов. Энзимодиагностика. Ферментативные лекарственные препараты.
- •Окисление жирных кислот. Внутриклеточная локализация и биоэнергетика процесса. Особенности обмена жирных кислот с нечетным количеством углеродных атомов и ненасыщенных жирных кислот.
- •О каком заболевании следует думать, если моча новорожденного ребенка дает положительную реакцию на наличие фенилпирувата? Какой молекулярный блок лежит в основе данной патологии?
- •Классификация ферментов. Общая характеристика класса лиаз. Коферменты лиазных реакций.
- •Регуляция липидного обмена. Гормоны, влияющие на обмен липидов. Патология липидного обмена: гиперлипидемии, атеросклероз, липоидозы, жировое перерождение печени, ожирение.
- •Классификация гормонов по локализации рецепторов. Вторичные посредники действия гормонов.
- •Гемоглобин, его структура, синтез, виды. Гемоглобинозы.
- •Белки плазмы крови, место их синтеза, биологическая роль. Изменения белкового спектра сыворотки крови при различных заболеваниях. Белки "острой фазы".
- •Глюкоза крови, пути ее поступления и использования. Гексокиназная реакция – ключевая реакция углеводного обмена. Пути превращения глюкозо-6-фосфата.
- •Дыхательная цепь. Ферментные комплексы дыхательной цепи, их локализация. Редокс-потенциалы ферментных систем. Ингибиторы переноса электронов.
- •Адреналин и норадреналин, их синтез и влияние на обмен веществ.
- •Особенности обмена в эритроцитах. Эритроцитарные энзимопатии. Синтез гема. Порфирии.
- •Процессы переваривания белков в кишечнике. Протеолитические ферменты панкреатического и кишечного соков. Гниение аминокислот в кишечнике и обезвреживание продуктов.
- •3.Оцените состояние больного по следующим данным анализа крови и мочи: глюкоза крови – 10,0 ммоль/л, рН крови – 7,30, в моче обнаружены глюкоза, кетоновые тела.
- •Эндокринная система организма. Классификация гормонов по химической структуре, их роль в регуляции обменных процессов. Причины эндокринных заболеваний. Механизм действия гормонов.
- •Цнс гипоталамус гипофиз периферические железы ткани мишени
- •Тканевой распад пуриновых и пиримидиновых нуклеотидов. Конечные продукты обмена пуринов и пиримидинов. Гиперурикемия. Подагра.
- •1.Биологические мембраны, их структурные компоненты. Функции биологических мембран.
- •2. Патология углеводного обмена. Сахарный диабет. Нарушение углеводного и липидного обмена при этом заболевании.
- •3. В крови больного повышена активность липазы, амилазы, трипсина. О какой патологии следует думать? Какие реакции катализируются данными ферментами?
- •Классификация ферментов. Общая характеристика класса трансфераз. Основные подклассы. Коферменты трансферазных реакций.
- •Напишите последовательность реакций превращения ацетил-КоА в мевалоновую кислоту в процессе синтеза холестерина. Укажите ферменты и коферменты.
- •Биохимический анализ нормальной и патологической мочи. Глюкозурия, протеинурия, кетонурия, билирубинурия.
- •Витамины, их классификация. Витамин в12 и фолиевая кислота, участие в обмене веществ и признаки витаминной недостаточности.
- •3.Какие изменения белкового спектра будут наблюдаться при остром воспалении? Что такое белки «острой фазы»? Диагностическое значение определения их концентрации в крови.
- •1. Роль воды в организме. Водный баланс, его регуляция и патология. Макроэлементы: натрий, калий, хлор, магний.
- •2. Биосинтез днк (репликация). Биосинтез рнк (транскрипция). Посттранскрипционный процессинг рнк. Основные положения аминокислотного кода. Обратная транскрипция.
- •1.Регуляция процессов биосинтеза белка на генетическом уровне (теория Жакоба и Моно). Гормональная регуляция белкового обмена. Гормоны анаболического и катаболического действия.
- •3.Будет ли протекать глюконеогенез, если в клетке цитратный цикл и дыхательная цепь полностью ингибированы. Ответ поясните.
- •Структура гликогена, синтез и распад гликогена в печени и мышцах. Гликогенозы.
- •Изогидрия. Механизмы поддержания изогидрии. Ацидоз и алкалоз.
- •Паратгормон и тиреокальцитонин. Влияние гормонов на обмен кальция и фосфора в организме человека
- •Сопряжение обмена углеводов и липидов. Сопряжение обмена углеводов и аминокислот. Пути превращения и образования пировиноградной кислоты.
- •1)Обмен и биологическое значение серосодержащих аминокислот (метионин и цистеин). Участие метионина в реакциях трансметилирования. Молекулярная патология обмена этих аминокислот.
- •2. Микроэлементы: селен, цинк, марганец, стронций, фтор, йод, молибден. Микроэлементозы.
- •3. Оценить состояние больного, если: рН крови - 7,31, рН мочи - 4,8. Общее содержание со2 в крови повышено. РСо2 - 80 мм рт ст. Титрометрическая кислотность мочи повышена.
- •Основные пути обмена аминокислот: декарбоксилирование, дезаминирование. Биологическая роль биогенных аминов.
- •2. Витамины р и с, их структура, признаки витаминной недостаточности, влияние на обмен веществ.
- •3. У больного после переливания крови развилась желтуха. Какой вид желтухи можно заподозрить? Как изменились показатели пигментного обмена в крови и моче?
- •Классификация ферментов. Общая характеристика класса оксидоредуктаз. Коферменты оксидоредуктазных реакций.
- •2. Гормональная регуляция углеводного обмена. Гормоны, повышающие и понижающие уровень глюкозы в крови. Механизм их действия.
- •3. В крови снижено содержание мочевины. Нарушение какого метаболического пути можно предположить, каковы возможные причины этих нарушений?
- •1. Понятие об обмене веществ. Процессы анаболизма и катаболизма, их характеристика и взаимосвязь. Виды метаболических путей. Центральные метаболиты.
- •I . Подготовительная фаза.
- •II фаза. Превращение мономеров в простые соединения - центральные метаболиты (пвк, ацетилКоА)
- •III фаза. Цикл Кребса
- •Витамины рр и в2, структура, признаки витаминной недостаточности и участие в обмене веществ.
- •1. Обмен и биологическое значение глутаминовой и аспарагиновой аминокислот в организме человека.
- •2. Микроэлементы: железо, медь и кобальт. Их роль в организме. Понятие о микроэлементозах.
- •3. Пациенту в лечебных целях назначили диету с низким содержанием углеводов. Концентрация глюкозы в крови нормальная. За счет каких процессов преимущественно поддерживается уровень глюкозы в крови?
- •1. Основные пути межуточного обмена аминокислот. Трансаминирование. Клиническое значение определения активности трансаминаз.
- •2. Антиоксидантная система организма. Неферментативные антиоксиданты. Антиоксидантные ферменты.
- •1. Гормоны передней доли гипофиза, их химическая структура и влияние на обмен веществ. Последствия изменений продукции соматотропного гормона в организме.
- •Соматотропный гормон
- •Тиреотропный гормон
- •Адренокортикотропный гормон ( актг )
- •Лютеинизирующий гормон ( лг )
- •Пролактин
- •2. Глюконеогенез. Основные субстраты, ключевые ферменты процесса. Цикл Кори
- •3. Больной 50 лет поступил в клинику с жалобами на резкие боли в области сердца, слабость. Активность каких ферментов следует определить в крови больного для исключения инфаркта миокарда?
- •1) Холестерин, его биологическая роль, биосинтез. Гиперхолестеринемии. Атеросклероз.
- •2. 2. Кровь, ее роль в организме. Химический состав плазмы. Калликреин-кининовая система. Про это смотри в книге!
- •3. Для лечения подагры применяется аллопуринол, структурный аналог гипоксантина. Объясните биохимический механизм действия данного лекарственного средства.
- •2. Синтез жирных кислот. Внутриклеточная локализация. Биосинтез триацилглицеролов.
- •1. Нуклеопротеины и нуклеиновые кислоты. Структурная организация молекул днк и рнк. Распад нуклеопротеинов в пищеварительном тракте. Нуклеотидный пул клеток, пути его пополнения и расходования.
- •2. Витамины а, е, к, влияние на обмен веществ, признаки витаминной недостаточности.
- •3. Оценить состояние больного по следующим данным анализа крови: активность креатинфосфокиназы повышена, общая активность лдг повышена, преимущественно за счет лдг1. Коэффициент де Ритиса - 1,90.
- •1. Биологическая роль печени. Роль печени в обмене углеводов, липидов, аминокислот и белков. Антитоксическая роль печени.
- •2. Биосинтез пуриновых и пиримидиновых нуклеотидов. Оротовая ацидурия.
- •1. Распад гемоглобина. Образование билирубина и продуктов его обмена. Характеристика прямого и непрямого билирубина. Диагностическое значиние их определения. Классификация желтух.
- •2. Глюкоза крови. Гипергликемия, гипогликемия, глюкозурия. Диагностическое значение определния глюкозы в крови и моче.
- •2. Витамин d. Химическая природа витамина, гормонально-активные формы. Участие витамина в обмене веществ. Рахит.
- •1)Фосфолипиды, их химическая структура, биологическая роль, биосинтез, переваривание и распад. Липотропные вещества.
- •2.Регуляция и патология белкового обмена.
- •1.Гормоны островкового аппарата поджелудочной железы. Химическая структура и влияние на обмен веществ.
- •2.Окислительное фосфорилирование. Значение и механизм процесса. Разобщение дыхания и фосфорилирования. Свободное окисление. Субстратное фосфорилирование.
- •3.Почему при переходе на рацион питания с высоким содержанием белка, у человека возрастает потребность в витамине в6.
- •1.Пути обезвреживания аммиака в организме. Транспорт аммиака. Мочевина как конечный продукт обмена аминокислот. Синтез мочевины. Гипераммониемия.
- •2.Классификация и химическая структура углеводов, их роль в обеспечении жизнедеятельности организма. Переваривание и всасывание углеводов в пищеварительном тракте. Мальабсорбция.
- •3.О поражении какой ткани можно думать, если в крови больного повышена активность алт, лдг и аргиназы? За счет каких изоферментов лдг можно предполагать повышение активности фермента?
- •1)Основные функции белков в организме. Структурная организация белковой молекулы. Особенности формирования первичной, вторичной, третичной и четвертичной структур белка.
- •2.Образование и распад ацетоновых тел. Кетогенез в норме и при патологии.
- •2.Обмен и биологическое значение фенилаланина и тирозина. Молекулярная патология обмена этих аминокислот.
- •3)Сколько молекул глюкозы надо разрушить до лактата, чтобы получить то же количество атф, которое образуется при полном распаде молекулы глюкозы (до со2 и н2о). Обоснуйте ответ.
- •2)Биохимия мышечной ткани. Важнейшие белки мышц. Креатин, креатинфосфат, креатинин, их синтез и биологическая роль.
- •3. У двух пациентов тест толерантности к глюкозе дал следующие результаты: глюкоза (ммоль/л)
- •2)Аэробный (дихотомический) путь распада глюкозы. Роль пируватдегидрогеназного комплекса в процессе окислительного декарбоксилирования пирувата. Биоэнергетика процесса.
- •II этап - окислительное декарбоксилирование пвк
- •3)В моче больного обнаружено увеличение уробилина. Чем это может быть обусловлено? Какие биохимические исследования нужно провести, чтобы уточнить причину появления билирубина в моче?
- •1)Биосинтез белка. Активация аминокислот, трансляция. Ингибиторы синтеза белка. Влияние облучения на синтез белка.
- •2)Гормоны стероидной природы: глюкокортикоиды, половые гормоны, минералокортикоиды. Химическая структура гормонов, механизм действия, влияние на обмен веществ.
- •1)Виды специфичности ферментов. Основные пути активации и ингибирования ферментативной активности.
- •2)Тироксин, его синтез, влияние на обмен веществ. Гипотиреоз и гипертиреоз.
- •3. Конденсация йодтирозинов
- •3. Как осуществляется связывание аммиака в различных тканях человеческого организма и его выделение? Напишите уравнения соответствующих реакций.
- •Сопряжение обмена липидов и аминокислот. Сопряжение обмена углеводов, липидов и аминокислот на уровне образования ацетил-КоА и на уровне цикла Кребса.
- •Гормоны гипоталамуса и нейрогипофиза, их химическая природа и влияние на обмен веществ.
- •1. Основные фазы унификации питательных веществ в организме. Цикл трикарбоновых кислот и его роль в обмене веществ.
- •Унификация питательных веществ идёт в три фазы
- •II. Биохимия нервной ткани, ее химический состав, особенности обмена.
- •2. Свободнорадикальное окисление. Понятие о перекисном окислении липи дов.
- •1. Аминокислоты - структурные единицы белка. Классификация аминокислот по структуре радикала. Заменимые и незаменимые аминокислоты. Значение для организма незаменимых аминокислот.
- •Транспортные формы липидов. Роль липопротеинов в обмене холестерина.
- •Заменимые, незаменимые и условнозаменимые аминокислоты. Кетопластичные и глюкопластичные аминокислоты. Аминокислотный пул. Пути его пополнения и использования. Биосинтез заменимых аминокислот.
- •2. Обмен кальция и фосфора в организме человека, регуляция обмена.
- •1. Классификация ферментов. Общая характеристика изомераз и лигаз. Коферменты изомеразных и лигазных реакций.
- •2. Остаточный азот крови. Диагностическое значение определения компонентов остаточного азота. Гиперазотемия, причины, виды.
- •1. Биосинтез белка. Активация аминокислот, трансляция. Ингибиторы синтеза белка. Влияние облучения на синтез белка.
- •1.Инициация.
- •2. Элонгация
- •3. Терминация
- •2. Гормоны стероидной природы: глюкокортикоиды, половые гормоны, мине ралокортикоиды. Химическая структура гормонов, механизм действия, влияние на об мен веществ.
- •1. Глюкокортикоиды.
- •1. Виды специфичности ферментов. Основные пути активации и ингибирования ферментативной активности.
- •Виды специфичности:
- •2. Тироксин, его синтез, влияние на обмен веществ. Гипотиреоз и гипертиреоз.
3. В крови больного повышена активность липазы, амилазы, трипсина. О какой патологии следует думать? Какие реакции катализируются данными ферментами?
Билет8
амилаза -острый панкреотит
трипсин- расщепление белков
липаза -гидролиз липидов
Билет 9.
Классификация ферментов. Общая характеристика класса трансфераз. Основные подклассы. Коферменты трансферазных реакций.
В основе классификации лежит тип катализируемой реакции.
•Оксидоредуктазыкатализируют окислительно-восстановительные реакции.
•Трансферазы-реакции с переносом групп.
•Гидролазы -гидролитический разрыв связи СС, СN, СSс присоединением воды по месту разрыва.
•Лиазы–реакции негидролитическогорасщепления с образованием двойных связей, некоторые обратные реакции синтеза.
•Изомеразы–перенос групп внутри молекулы с образованием изомеров.
•Лигазыкатализируют соединение двух молекул, сопряжённое с разрывом пирофосфатнойсвязи АТФ.
Трансферазы
Коферменты трансфераз:
•ФП,
•ТГФК,
•АТФ,
•ФАФС,
•АДФ
Трансферазы
•фосфотрансферазы,
•аминотрансферазы,
•гликозилтрансферазы,
•ацилтрансферазы,
•переносчики одноуглеродных частиц,
•переносчики кетонных и альдегидных групп.
Трансферазы катализируют реакции переноса различных групп от одного субстрата (донор) к другому (акцептор), участвуют в реакциях взаимопревращения различных веществ, обезвреживания природных и чужеродных соединений. Коферментами являются пиридоксальфосфат,коэнзим А, тетрагидрофолиевая кислота, метилкобаламин. Класс подразделяется на 9 подклассов в зависимости от строения переносимых групп.Примером подклассов являются ферменты, переносящие одноуглеродные фрагменты, альдегидные или кетоостатки, ацильные остатки, азотсодержащие группы, фосфорсодержащие группы. селенсодержащие группы.На подподклассы деление производится в зависимости от вида переносимой группы – метил (2.1.1.), карбоксиметил или формил (2.1.2.), амино-группы (2.6.1.).Часто встречается рабочее название трансфераз – киназы. Это трансферазы, катализирующие перенос фосфата от АТФ на субстрат (моносахариды, белки и др), т.е. фосфотрансферазы.
Напишите последовательность реакций превращения ацетил-КоА в мевалоновую кислоту в процессе синтеза холестерина. Укажите ферменты и коферменты.
Синтез холестерина
включает 35 реакций,
идёт в 3 стадии:
образование из ацетил-КоА мевалоновой кислоты,
образование из мевалоновой кислоты сквалена,
циклизация сквалена в холестерин.

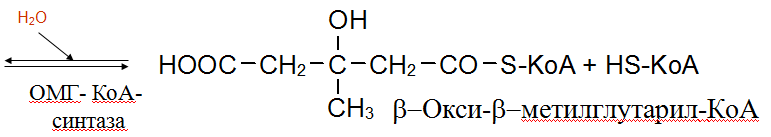


Биохимический анализ нормальной и патологической мочи. Глюкозурия, протеинурия, кетонурия, билирубинурия.
Патологические компоненты мочи
Пигменты
Кроме указанных выше пигментов, в моче при патологиях может обнаруживаться еще пигмент – продукт распада гема билирубин.
Клинико‑диагностическое значение
Билирубинурия может развиться при инфекционных заболеваниях, диффузном токсическом зобе. При заболеваниях печени он появляется в моче в виде билирубина глюкуронида (прямой билирубин) – паренхиматозные желтухи при вирусных гепатитах или нарушение оттока желчи при механических желтухах. Для гемолитических желтух билирубинурия не характерна, т.к. непрямой билирубин не проходит через почечный фильтр.
Белки
В норме белок в моче практически отсутствует.
Клинико‑диагностическое значение
Появление белка в моче называется протеинурией. По степени потери белка различают от 0,003 до 1 г/сут, от 1 до 3 г/сут, от 3 г/сут и более. Самая большая потеря белка происходит при поражении гломерулярного аппарата. Почечная протеинурия возникает при поражении почек:
поражение почечного фильтра – повышение проницаемости гломерул (нарушение эндотелия, базальной мембраны, дефект подоцитов),
снижение кровотока в почках (замедление, уменьшение объема крови).
Внепочечные протеинурии:
данный вид протеинурия возникает при воспалении в мочеточниках, мочевом пузыре, уретре, предстательной железе.
также в моче определяют белок Бенс-Джонса, что характерно для миеломной болезни, макроглобулинемии Вальденстрема.
Функциональная почечная протеинурия (временная) – при стрессах, отрицательных эмоциях, при длительной физической нагрузке (маршевая), при длительном нахождении в положении стоя (чаще у детей), холодовая.
Глюкоза
Моча здорового человека содержит минимальное количество глюкозы, которое обычными лабораторными пробами не обнаруживается.
Клинико‑диагностическое значение
Появление глюкозы в моче называется глюкозурия. Для более достоверной оценки исследуют мочу, собранную за сутки. Существуют две основные причины, обуславливающие появление глюкозы в моче:
гипергликемия, при которой концентрация глюкозы в ультрафильтрате превышает способность почек к ее реабсорбции (сахарный и стероидный диабет, тиреотоксикоз),
нарушение канальцевой реабсорбции, при которой даже низкие количества глюкозы не реабсорбируются (нефроз, нефрит, нефротический синдром, ренальный диабет).
Физиологическая глюкозурия наблюдается при употреблении большого количества сладостей (только при наличии нарушений в почках или инсулярного аппарата), при стрессе, после приема лекарств (кофеин, кортикостероидные гормоны).
Кетоновые тела
Клинико‑диагностическое значение
Наличие кетоновых тел в моче называют кетонурией. Чаще всего наблюдают при тяжелом сахарном диабете, диабетической коме, голодании, тяжелых токсикозах. Определение кетонов в моче может использоваться для оценки эффективности диеты при снижении веса.
Билет 10.
Классификация и химическая структура липидов. Роль липидов в обеспечении жизнедеятельности организма. Переваривание и всасывание липидов, роль желчи в этом процессе, желчные кислоты. Ресинтез липидов в эпителии кишечника.
1) ЛИПИДЫ. Липиды - сложные эфиры ВЖК и спиртов (глицерин, инозит, сфингозин). Липиды не растворимы в воде Простые липиды представлены двухкомпонентными веществами - сложными эфирами вжк с глицерином. В эту группу относят: а) триацилглицерины - сложные эфиры ВЖК и глицерина. б) воска - сложные эфиры ВЖК и высших спиртов. в) стериды - сложные эфиры ВЖК и полициклических спиртов (холестерин). Сложные липиды - многокомпонентные вещества, состоящие из спиртов, ВЖК, остатка фосфорной кислоты, азотистых оснований, одного или нескольких остатков углеводов. Их подразделяют на фосфолипиды и гликолипиды.
1. Фосфолипиды представляют собой сложные эфиры многоатомных спиртов (глицерин, сфингозин, инозит) с ВЖК, содержащие в качестве добавочных групп остатки фосфорной группы и азотистых оснований. Выделяют: а) глицерофосфолипиды: лецитин, инозитфосфолипид. б) сфингофосфолипиды. Входят в состав всех тканей и клеток организма. Они легко образуют комплексы липидов с белками, облегчая транспорт липидов, участвуют в формировании плазматических и внутриклеточных мембран, обеспечивают проницаемость мембран.
2. Гликолипиды. В их состав входит галактоза или её производные, сфингозин и ВЖК. Они восстанавливают электровозбудимость мозговой ткани, вовлечены в процесс приема сигналов, поступающих в клетки, участвуют в рецепции пептидных гормонов, входят в состав мозговой и нервной ткани.
БИОРОЛЬ: 1.Энергетическая (при окислении 1 грамма жира выделяется 9,3 ккал). 2.Пластическая (в комплексе с белком входят в состав биологических мембран клеток и клеточных органелл, обеспечивая их проницаемость).
Участвуют в передаче нервного импульса.3.Жир, окружая внутренние органы своеобразной капсулой, предохраняет их от ударов и сотрясений.4.Входя в состав подкожной клетчатки, липиды выполняют функцию терморегуляции.
5.Являются источником жирорастворимых витаминов.
Переваривание и всасывание липидов.Суточная потребность 80-100 г., из них 25 г. должно поступать растительных липидов. Переваривание липидов происходит в тех отделах пищеварительного тракта, где имеются следующие условия: 1. Наличие липаз-ферментов расщеляющих липиды. 2. Условия для проявления их оптимальной активности (рН=7,8-8). 3. Условия для эмульгирования липидов. Липаза может воздействовать только на эмульгированные жиры. Эмульсии-дисперсные системы двух несмешивающихся жидкостей, где одна жидкость находится в раздробленном состоянии (в виде капелек) в другой (жир-Н2О).
Такими эмульгаторами для липидов в нашем организме являются соли желчных кислот.
В ротовой полости переваривания липидов не происходит. В желудке липаза низкоактивна, т.к. рН среды в желудке 1,5-2,0. Исключение составляют новорожденные и грудные дети. У них в желудке рН среды =5-6, в этих условиях липаза расщепляет эмульгированный жир грудного молока.
Основное место переваривания липидов у взрослого организма – тонкий отдел кишечника (12-перстная кишка), где имеются все необходимые условия.
В этот отдел кишечника поступает сок поджелудочной железы, содержащий липазы, сюда же поступает из желчного пузыря желчь, составные компоненты которой (желчные кислоты) необходимы для переваривания липидов.
Функции желчных кислот: 1. эмульгируют липиды 2. активируют липазы 3. способствуют всасыванию продуктов гидролиза липидов в стенку кишечника.
Желчные кислоты образуются в печени из холестерина и являются производными холановой кислоты.
В желчи человека содержатся, главным образом, парные желчные кислоты (т.е. желчная кислота взаимодействует с глицином или таурином).
Н апример:
холевая кислота + глицин -
гликохолевая; соответственно
апример:
холевая кислота + глицин -
гликохолевая; соответственно
таурохолиевая кислота) и т.д.
Гидролиз триацилглицерина в кишечнике идёт ступенчато.
40% жира гидролизуется полностью до глицерина и ВЖК. Таким образом, образующаяся в результате гидролиза липидов смесь содержит: жирные кислоты, моноацилглицерины, диацилглицерины, глицерин и другие компоненты липидов.
Всасывание продуктов гидролиза липидов.
Глицерин и жирные кислоты с короткой углеродной цепью уходят из кишечника через портальную систему кровообращения и поступают в печень. А жирные кислоты с количеством углеродных атомов больше 10, моноацил-глицерины, диацилглицерины всасываются с помощью желчных кислот (путем образования с ними мицелл), которые транспортируют их через слизистую оболочку кишечника в эпителий кишечника. Внутри стенки кишечника мицелла распадается, а желчные кислоты уходят в кровь и через систему воротной вены попадают в печень, а оттуда вновь в желчные протоки. Таким образом происходит постоянная циркуляция желчных кислот между печенью и кишечником. Установлено, что у человека общий пул желчных кислот составляет 2,8-3,5 г., при этом они совершают 6-8 оборотов в сутки. 0,3 г. желчных кислот теряется с калом. Нарушения желчеобразования или поступления желчи в кишечник приводит к тому, что жиры выделяются в непереваренном или частично переваренном виде с калом – стеаторея. Из продуктов гидролиза триацилглицеринов пищи в стенке кишечника происходит ресинтез жиров, специфичных для данного организма. Здесь же в стенке кишечника реситезированный жир формирует с белками липопротеидные комплексы - хиломикроны (ХМ), которые являются транспортной формой экзогенного жира.
ХМ - это комплекс белка (2%) + липид (Тгл/90%) + ХС + фосфолипид.
