
- •Глава 1 общие вопросы хирургии традиции и перспективы развития хирургии
- •Глава 2 методология постановки диагноза в хирургической клинике
- •Глава 3 важнейшие синдромы,
- •Глава 4 методы анестезии
- •И обеспечения безопасности
- •Больного во время
- •Хирургического вмешательства
- •Глава 5 принципы лечения больных в послеоперационном периоде
- •Глава 6 абдоминальная хирургия
- •Глава 7 острый холецистит
- •Глава 8 острый панкреатит
- •Глава 9 осложнения язвенной болезни
- •Глава 10 наружные брюшные грыжи
- •Глава 11 острая кишечная
- •Глава 12 острые нарушения
- •Глава 13 травма живота
- •Глава 14 гнойный перитонит
- •Глава 15 стрый живот.
Глава 9 осложнения язвенной болезни
Язвенная болезнь желудка и двенадцатиперстной кишки широко распространена во всём мире. Приводимые в специальной литературе конца XX века статистические данные свидетельствуют о многих миллионах больных в экономически развитых странах, подчёркивая тенденцию к росту заболеваемости этим недугом. По мнению ведущих гастроэнтерологов мира, язвенная болезнь — национальная проблема многих стран.
Последнее десятилетие характеризовалось новыми достижениями в лечении язвенной болезни, отразившимися на врачебном подходе к этому заболеванию. Речь идёт об успехах фармакотерапии (появлении принципиально новых классов антисекреторных препаратов), а также об уточнении представления о патогенезе язвенной болезни (роли Helicobacter pylori). Всё это вызвало у части врачей, в первую очередь терапевтов, своего рода эйфорию. Казалось, что проблема язвенной болезни разрешается исключительно терапевтическим путём и хирургии не остаётся места в лечении этого заболевания. Между тем летальность, обусловленная осложнениями язвенной болезни, не претерпела столь заметных изменений. Поэтому ещё долгие годы хирурги наряду с терапевтами будут призваны оказывать помощь этому многочисленному контингенту больных.
Хирургия язвенной болезни в первую очередь — хирургия её осложнений. Поэтому в данной главе учебника речь пойдёт только об осложнённых формах заболевания. К ним относят перфорацию язвы, профузное желудочно-кишечное кровотечение, пилородуоденаль-ный стеноз, пенетрацию и малигнизацию. Последнее осложнение в силу особенностей хирургической тактики будет рассмотрено в главе, посвященной раку желудка. Пенетрация (проникновение язвы в соседние анатомические структуры, чаще всего в головку поджелудочной железы и печёночно-двенадцатиперстную связку) становится частой причиной гастродуоденального кровотечения. Поэтому своеобразные диагностические приёмы и хирургическая техника, используемые при этом осложнении, будут описаны в рамках кровоточащих язв.
Перфоративные гастродуоденальные язвы
Перфорация — тяжёлое, угрожающее жизни осложнение, занимающее ведущие позиции в структуре летальности при язвенной болезни. Снизившаяся к 50-м годам прошлого века летальность при этом состоянии уже в течение многих лет составляет от 5 до 17,9%. Определяющие летальность факторы — тяжёлое общее состояние пациента, обусловленное развитием перитонита, нередко выраженной сопутствующей патологией, а также время, прошедшее с момента возникновения осложнения. Так, у больных, оперированных через сутки после перфорации, летальность возрастает в 7-8 раз по сравнению с пациентами, которым операцию провели в течение первых 6 ч.
Современная статистика последнего десятилетия подчёркивает рост доли этого грозного осложнения, при этом перфорации язв стали возникать гораздо чаще, чем стеноз, приближаясь к частоте язвенных кровотечений. Количество операций по поводу перфоратив-ной язвы стабильно держится на уровне 7,5—13,0 на 100 000 человек.
Как правило, осложнение возникает преимущественно у мужчин, в основном молодого возраста, с кратким язвенным анамнезом (до 3 лет) и периодическими обострениями, чаще в весенний и осенний периоды. У 25% больных жалоб в прошлом не было.
Перфоративные язвы чаще бывают локализованы в двенадцатиперстной кишке (75%). Примерно в 10% случаев перфорация язвы сопровождается кровотечением или стенозом.
Классификация
Этиология:
перфорация хронической язвы;
перфорация острой язвы (в том числе медикаментозной, стрессовой, уремической и др.).
Локализация перфорации:
• язва желудка: малой кривизны, передней стенки, задней стенки;
язва двенадцатиперстной кишки: передней стенки, задней стенки. Клиническая форма перфорации:
в свободную брюшную полость (в том числе прикрытая);
атипичная", в сальниковую сумку, малый или большой сальник, забрюшинную клетчатку, изолированную спайками полость;
Фаза течения перитонита (клинический период):
сочетание с желудочно-кишечным кровотечением;
сочетание со стенозом выходного отдела желудка
химический перитонит (период первичного шока);
бактериальный перитонит (период мнимого благополучия);
разлитой гнойный перитонит (период абдоминального сепсиса).
Основные черты патологии
Перфорация язвы приводит к поступлению гастродуоденального содержимого в свободную брюшную полость, воздействуя на брюшинный покров как химический, физический, а затем и бактериальный раздражитель. Перитонит, возникающий при перфорации, — один из факторов, влияющих на тактику хирургического лечения. Следует отметить некоторые особенности перитонита при перфорации. Начальная реакция организма на прободение язвы ярко клинически окрашена в связи с воздействием кислого желудочного сока на брюшину (по сути, её химическим ожогом). В дальнейшем развивается серозно-фибринозный перитонит, а затем и гнойный. Как правило, до 6—12 ч от момента перфорации в брюшной полости выявляют прозрачный или мутный экссудат с нитями и хлопьями фибрина, париетальная и висцеральная брюшина ярко гиперемирована. Степень бактериальной контаминации при этом не превышает 103-105 микробных тел в 1 мл экссудата. Микробный пейзаж в большинстве случаев представлен грамположительными кокками, лактобацил-лами, грибами рода Candida. Следует отметить, что в 30% случаев в эти сроки бактериальное обсеменение отсутствует. Указанные изменения позволяют выбрать радикальный способ оперативного вмешательства у этой группы больных.
В более поздние сроки с момента перфорации в брюшной полости появляются гноевидный экссудат, фиксированные наложения фибрина, паралитическая кишечная непроходимость с увеличением бактериальной контаминации. В период разлитого гнойного перитонита следует избрать минимально травматичный способ вмешательства, включающий санацию брюшной полости.
Диагностика Симптоматика
Перфорация язвы развивается остро, хотя у 20% больных удаётся выявить продромальный период — усиление болей за 3-4 дня, появление тошноты, рвоты. Перфорация сопровождается классической триадой признаков: кинжальная боль (95%), доскообразное напряжение мышц живота (92%), предшествующий язвенный анамнез (80%).
Данные физикального обследования
В течение заболевания различают три фазы (шока, мнимого улучшения и гнойного перитонита), имеющие свои характерные клинические проявления.
В первой фазе перфорации (до 6 ч) при физикальном обследовании выявляют шок. Обращает на себя внимание внешний вид больного: он лежит неподвижно на спине или правом боку с приведёнными к животу ногами, охватив руками живот, избегает перемены положения тела. Лицо больного осунувшееся и бледное, с испуганным выражением. Дыхание частое и поверхностное. Характерна начальная брадикардия: пульс нередко падает до 50—60 в минуту (так называемый вагусный пульс) вследствие ожога брюшины и нервных окончаний кислотой. АД может быть снижено. Язык в первые часы после перфорации остаётся влажным и чистым. Обращают на себя внимание резчайшая перкуторная и пальпаторная болезненность живота, напряжение мышц передней брюшной стенки сначала в верхних отделах, а затем и по всему животу. Положителен симптом Щёткина—Блюмберга. Исчезает или значительно уменьшается печёночная тупость — характерный симптом появления свободного газа в брюшной полости. Вместе с тем, этот признак в первые часы после перфорации, вследствие небольшого количества газа в брюшной полости, может отсутствовать. Иногда отмечают болезненность в правом боковом канале и правой подвздошной ямке {симптом Кервена). Зачастую выявляют положительный френикус-симптом — иррадиацию болей в надключичную область, правую лопатку. Как правило, перистальтика кишечника не выслушивается. Уже в первые часы заболевания удаётся обнаружить резкую болезненность тазовой брюшины при пальцевом ректальном или вагинальном исследовании.
Описанная картина, характерная для фазы шока, через 6—12 ч после перфорации «стирается». Наступает период мнимого благополучия. Лицо больного приобретает нормальную окраску. Пульс и АД нормализуются. Дыхание перестаёт быть поверхностным. Язык становится сухим и обложенным. Напряжение мышц брюшной стенки уменьшается, при пальпации сохраняются болезненность и положительные симптомы раздражения брюшины. Перистальтика не выслушивается, печёночная тупость отсутствует. При ректальном исследовании можно обнаружить нависание передней стенки прямой кишки и её болезненность.
Затем, через 12—24 ч после перфорации состояние больных начинает прогрессивно ухудшаться — наступает фаза гнойного перитонита. Появляется рвота. Больной ведёт себя беспокойно. Температура тела повышается. Учащается дыхание, падает пульсовое давление, возникает вздутие живота, перистальтика отсутствует. Налицо развернутая клиническая картина абдоминального сепсиса.
Диагностические методы
Обзорная рентгенография органов брюшной полости при перфорации полого органа выявляет свободный газ под куполом диафрагмы в 80% случаев. Точность рентгенологического метода находится в прямой зависимости от количества газа, поступившего в свободную брюшную полость. В сомнительных случаях следует прибегать к пнев-могастрографии, повышающей достоверность метода до 95%. Установив в желудок зонд, в его просвет с помощью шприца Жане вводят 150-200 мл воздуха и тотчас выполняют обзорную рентгенографию брюшной полости. Тяжёлым больным целесообразно проводить рентгенографию в положении на боку, при этом свободный газ локализуется у места прикрепления диафрагмы к боковой стенке живота.
Эзофагогастродуоденоскопия позволяет уточнить диагноз в сложных случаях, дать точную картину локализации язвы и её размеров, обнаружить сочетанные осложнения (наличие второй язвы с кровотечением или угрозой его развития, признаки стеноза).
Лапароскопия помогает уточнить диагноз и выбрать адекватный план лечения при неясной клинической картине (в тех ситуациях, когда другие вышеперечисленные методы не позволяют распознать прикрытую или атипичную перфорацию), а в части случаев позволяет убедиться в возможности проведения того или иного вида операции.
Лабораторное исследование крови констатирует быстро нарастающий лейкоцитоз со сдвигом лейкоцитарной формулы влево. В анализах мочи при перитоните отмечают появление форменных элементов крови,белка и цилиндров.
Дифференциальная диагностика
Дифференциальный диагноз перфоративной язвы нередко приходится проводить с острым аппендицитом, особенно если больного осматривают через 6—7 ч после перфорации, когда желудочное содержимое и экссудат скапливаются в правой подвздошной ямке, вызывая симптомы, характерные для аппендицита. В части случаев диагностические затруднения могут возникнуть при других острых хирургических заболеваниях органов верхнего этажа брюшной полости. Прежде всего, это острый холецистит, острый панкреатит, почечная колика и острая кишечная непроходимость.
Нельзя также забывать о возникающих иногда чрезвычайных трудностях диагностики терапевтических заболеваний, таких как инфаркт миокарда, базальный плеврит, пневмония.
В заключение следует подчеркнуть, что вопросы точной диагностики причины «острого живота» становятся непреодолимыми при уже развившемся разлитом гнойном перитоните, тогда их решают при экстренной срединной лапаротомии.
Лечение
Консервативный способ ведения больных с перфоративными язвами (так называемый метод Тейлора) предполагает постоянную аспирацию желудочного содержимого, голод, назначение больших доз антибиотиков, а также придание телу больного положения Фовлера (с приподнятым головным концом). Сегодня очевидно, что этот метод несовершенен и поэтому применим только как вынужденная мера — при предельно тяжёлом состоянии больного либо отсутствии возможности проведения операции. Поэтому диагноз перфоратив-ной язвы желудка или двенадцатиперстной кишки — абсолютное показание к экстренной операции.
Хирургическая тактика
Характер и объём хирургического вмешательства определяют строго индивидуально в зависимости от вида язвы, её локализации, характера и распространённости перитонита, наличия сопутствующих перфорации других осложнений язвенной болезни, а также с учётом степени операционно-анестезиологического риска. Различают радикальные операции, направленные не только на спасение жизни больного, но и на профилактику дальнейших рецидивов образования язв (резецирующие методы, ваготомия с иссечением язвы и пи-лоропластикой), а также паллиативные — различные способы ушивания перфорации, устраняющие только угрожающее жизни осложнение болезни.
Ушивание дуоденальной или желудочной перфоративной язвы остаётся спасительным методом лечения, особенно для больных с распространённым «поздним» перитонитом или высокой степенью опе-рационно-анестезиологического риска. На рис. 9-1 и 9-2 представлены наиболее распространённые способы ушивания перфоративной дуоденальной язвы. Летальность зависит, прежде всего, от условий, в которых выполняют вмешательство, распространённости и формы перитонита; она составляет от 10 до 60%.
Лапароскопическое ушивание (или ушивание из абдоминального доступа) показано также лицам молодой возрастной группы, когда перфорируется так называемая «немая язва», в анамнезе отмечают невыраженное или благоприятное течение заболевания, а выполненная дооперационная диагностическая программа свидетельствует об отсутствии других сочетанных осложнений язвенной болезни.
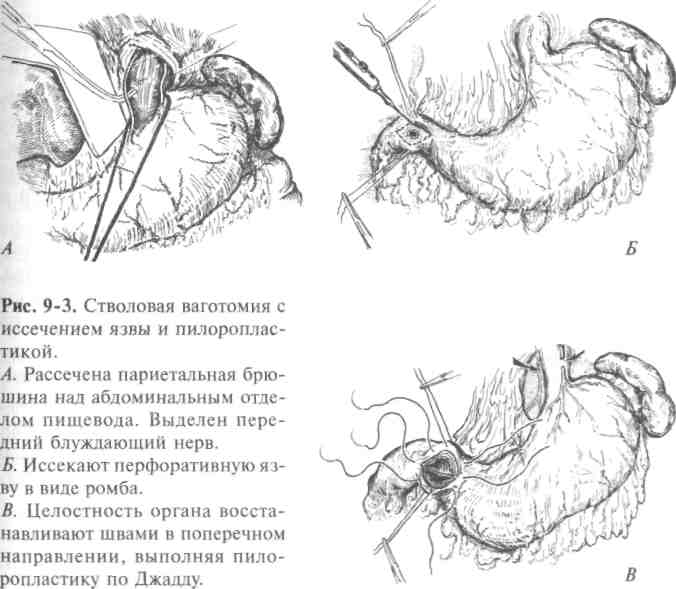
Стволовая ваготомия с иссечением язвы и пилоропластикой — золотой стандарт хирургического лечения перфоративной дуоденальной язвы, позволяющий ликвидировать другие осложнения заболевания, сопутствующие перфорации, и создать условия профилактики дальнейших рецидивов. На рис. 9-3 представлена стволовая ваготомия с иссечением язвы и пилоропластикой по Джадду. Кроме того, довольно часто выполняют пилоропластику по Финнею. Послеоперационная летальность после этих операций составляет 1,8—2,5%.

Ваготомию с антрумэктомией используют при перфорации, если выявлены другие осложнения (поздняя стадия пилородуоденального стеноза), а также при сочетанной форме язвенной болезни.
Резекцию желудка (гемигастрэктомию) проводят при прободной желудочной язве больным с невысоким операционно-анестезиоло-гическом риском, когда перфорирована длительно существующая каллёзная язва или существуют сочетанные с перфорацией другие осложнения (кровотечение, различной выраженности стеноз). Летальность при этом достигает 4—9%.
Послеоперационный период
Ведение послеоперационного периода у больных, оперированных по поводу прободных гастродуоденальных язв, необходимо соотносить с характером проведённого вмешательства.
Так, при ушивании прободных язв, когда операция фактически не влияет на патогенез заболевания, дальнейшее благополучие больного зависит от противорецидивного лечения, начинаемого сразу после операции. Оно должно быть комплексным, состоящим из антисекреторных препаратов (блокаторы Н2-гистаминовых рецепторов, блокаторы протонной помпы) и антихеликобактерной терапии (препараты висмута в комбинации с антибиотиками — амоксициллином, флемоксином). После выписки из стационара больной переходит под наблюдение гастроэнтеролога для последующей поддерживающей и противорецидивной терапии.
Хирургические операции, имеющие патофизиологическое обоснование (ваготомия с пилоропластикой, ваготомия с антрумэктомией, резекция желудка), по современным представлениям также должны сопровождаться поддерживающей и противорецидивной терапией. Её начинают также сразу в послеоперационном периоде.
После окончательной оценки непосредственного эффекта противоязвенного лечения в условиях диспансерного наблюдения больных, когда амбулаторно определяют состояние секреторной и эвакуатор-ной функций оперированного желудка и эрадикацию Helicobacter pylori, больные окончательно переходят под наблюдение врача-гастроэнтеролога.
Прогноз
Показатели летальности были указаны в начале этого раздела. Среди погибших после операций по поводу перфоративной язвы превалируют пациенты с исходным предельно тяжёлым состоянием, обусловленным либо сопутствующей патологией, либо терминальной фазой перитонита. Неблагоприятный исход чаще всего становится следствием поздней обращаемости больного за медицинской помощью и несвоевременной диагностики.
У части больных возможно развитие хирургических осложнений. Наиболее типичные из них — несостоятельность ушитой язвы или сформированного анастомоза с развитием перитонита, абсцессы различной локализации на фоне недостаточной санации брюшной полости при первичной операции, паралитическая кишечная непроходимость, послеоперационная спаечная кишечная непроходимость, острый послеоперационный панкреатит.
Одна из особенностей состояния больных после операций с ва-готомией — нарушение моторно-эвакуаторной функции желудка и двенадцатиперстной кишки. Ниже, в разделе, посвященном язвенному стенозу выходного отдела желудка, об этом будет сказано более детально.
Одна из задач современной хирургической гастроэнтерологии — не только обеспечение хороших непосредственных результатов, но и создание условий для быстрейшей реабилитации пациентов в раннем послеоперационном периоде и предотвращение рецидивов язвенной болезни. В качестве неблагоприятных факторов в отдалённом периоде рассматривают органические (рецидив язвы, дефект сформированных ранее анастомозов) и функциональные (нарушение желудочной эвакуации функциональной природы, ранний и поздний демпинг-синдром, синдром приводящей петли, диарея и т.д.) расстройства.
Очевидно, что органосохраняющие операции с ваготомией имеют свои преимущества — в отдалённом послеоперационном периоде у большинства пациентов (90%) отмечают хорошие результаты, а качество жизни соответствует таковому у здорового человека. И всё же следует иметь в виду, что количество рецидивов язвенной болезни достигает 10%. Строгое определение группы больных, которым показано ушивание прободной язвы (в том числе и лапароскопическое) с последующей медикаментозной терапией, позволяет достичь хорошего качества жизни у большинства больных язвенной болезнью при достаточно низкой частоте рецидива язвы.
Язвенная болезнь, осложнённая кровотечением
Гастродуоденальные кровотечения язвенной природы составляют около половины всех кровотечений из верхнего отдела ЖКТ. Количество больных с язвенными гастродуоденальными кровотечениями в последнее десятилетие увеличивается, и заболеваемость составляет 90—103 на 100 000 взрослого населения в год. По данным отечественной статистики, за последние годы количество подобных больных возросло в 1,4-1,6 раза, что, очевидно, связано с экономическими факторами, когда больные порой не в состоянии обеспечить дорогостоящее курсовое противоязвенной лечение. Важность знания врачами (не только хирургами!) способов диагностики и лечения острых язвенных желудочно-кишечных кровотечений в первую очередь определяется высоким уровнем летальности, достигающей 50% в группе больных с тяжёлыми желудочно-кишечными кровотечениями. Среди пациентов с кровотечением велика доля людей пожилого и старческого возрастов (до 60%) с выраженной возрастной и сопутствующей патологией, поэтому велика доля послеоперационных осложнений. У мужчин желудочно-кишечные кровотечения при язвенной болезни отмечают в 3 раза чаще, чем у женщин.
Классификация
Локализация источника кровотечения:
язва желудка;
язва двенадцатиперстной кишки;
рецидивная язва после различных оперативных вмешательств на желудке.
Степень тяжести кровопотери:
лёгкая;
средняя;
тяжёлая.
Характер язвенного кровотечения (определяют эндоскопически):
продолжающееся;
остановившееся:
высокая угроза рецидива;
низкая угроза рецидива.
При оценке степени тяжести кровотечения учитывают как объём перенесённой кровопотери, так и состояние больного. Данные клинического обследования больного и лабораторные показатели позволяют определить объём кровопотери, спланировать рациональную инфузионно-трансфузионную терапию, адекватно оценить состояние больного. В табл. 9-1 приведены наиболее важные показатели, используемые в клинической практике.
Таблица 9-1. Степень тяжести кровопотери
Показатели |
Степень кровопотери |
||
лёгкая |
средняя |
тяжёлая |
|
Количество эритроцитов |
>3,5-10|2/л |
3,5-2,5-1012/л |
<2,5-1012/л |
Содержание гемоглобина, г/л . |
>100 |
83-100 |
<83 |
Пульс в минуту |
до 80 |
80-100 |
более 100 |
Систолическое АД, мм рт.ст. |
>110 |
110-90 |
<90 |
Гематокрит, % |
>30 |
25-30 |
<25 |
Дефицит объёма циркулирующих эритроцитов, в % должного |
до 20 |
20-30 |
30 и более |
Патофизиологические нарушения в организме
Реакция больного на кровопотерю, с одной стороны, определяется интенсивностью и массивностью самого кровотечения (объёмом потерянной крови и временем кровотечения), а с другой — исходным состоянием и реакцией на кровопотерю основных систем организма больного. Фактором, существенно повлиявшим на понимание патофизиологических основ этого процесса и формирование грамотной терапии, послужило учение о диссеминированном внутрисосу-дистом свёртывании (ДВС), как универсальном механизме реализации синдрома массивной кровопотери и пусковом механизме синдрома полиорганной недостаточности. Следует подчеркнуть, что гиперкоагуляционная фаза ДВС-синдрома и микроциркуляторные нарушения, ведущие к ухудшению обеспеченности тканей кислородом и питательными веществами, развиваются у каждого пациента с клинически значимым желудочно-кишечным кровотечением. Понятно, что существовавшие у пациента функциональные либо органические расстройства со стороны сердечно-сосудистой, дыхательной и выделительной систем (так называемые возрастные сопутствующие заболевания) лишь усугубляют тяжесть состояния больного, требуют соответствующей коррекции и учитываются при принятии решения об оперативном лечении либо при подготовке к нему.
Считают, что быстрая кровопотеря около 500 мл крови может привести к коллапсу, причём проявления гемодинамических нарушений будут более выраженными у пожилых больных с исходной сердечнососудистой недостаточностью. Приблизительно такой же объём излившейся в просвет пищеварительного тракта крови требуется для появления характерных признаков желудочно-кишечных кровотечений — рвоты кровью (hematemesis) и дегтеобразного стула (melena).
Наиболее яркие проявления наблюдают при острых массивных кровотечениях, когда на протяжении короткого времени, измеряемого минутами или часами, больной теряет более 1500 мл крови, или около 25% ОЦК. В подобных обстоятельствах клиническая картина соответствует геморрагическому (гиповолемическому) шоку, из прямой кишки отмечают выделение красной малоизмененной крови (hematochezia). Необходимо отметить, что у больного, если он лежит, сначала может не быть сколько-нибудь выраженных изменений АД (так называемая компенсированная гиповолемия), в то время как феномен ортостатической гипотензии более точно отражает объём кровопотери. Периферический спазм артерий, проявляющийся бледностью кожных покровов, а также венозный спазм поддерживают относительно стабильный уровень центрального кровообращения.
Диагностика
Врач, заподозривший кровотечение, должен ответить на следующие вопросы.
Есть ли желудочно-кишечное кровотечение?
Что стало его источником?
Продолжается ли кровотечение?
Каковы темпы кровотечения?
Какова тяжесть кровопотери?
Симптоматика
Клинические проявления острых, особенно массивных гастроду-оденальных кровотечений достаточно ярки и складываются из общих симптомов, характерных для кровопотери (резкая слабость, головокружение, потеря сознания), и проявлений, характерных для кровотечения в просвет ЖКТ (гематомезис, мелена или гематохезия). У значительной доли больных кровотечение возникает на фоне обострения язвенной болезни или в анамнезе удаётся отметить типичные признаки этого заболевания с характерным «язвенным» болевым синдромом и сезонностью обострений. У части больных можно встретить указания на неэффективность проведённого ранее хирургического лечения, когда вновь появившийся болевой синдром следует связать, прежде всего, с образованием пептической язвы. Кровавая рвота и дегтеобразный стул — примерно одинаково частые признаки кровотечения язвенной этиологии, хотя при локализации язвы в двенадцатиперстной кишке чаще выявляют изолированную мелену
Данные физикального обследования
Данные физикального обследования позволяют судить о степени тяжести кровотечения и предположительно о его источнике. Спутанное сознание, резкая бледность кожных покровов, частый пульс слабого наполнения и напряжения, снижение АД и пульсового давления, наличие в желудке большого количества крови и сгустков, а при ректальном исследовании — чёрного жидкого либо с примесью крови содержимого — признаки острого массивного кровотечения. Фактически в таких случаях речь идёт о геморрагическом шоке (дефицит глобулярного объёма крови, как правило, более 30%). При лёгкой и средней степенях тяжести желудочно-кишечных кровотечений (уменьшение объёма циркулирующих эритроцитов крови менее чем на 30%) клинические проявления менее выражены. Общее состояние больных, как правило, остаётся удовлетворительным либо средней тяжести, гемодинамические показатели в пределах нормы или изменяются умеренно, нет большого объёма крови в желудке. Рвота и мелена редко бывают многократными.
Инструментальные методы
На сегодняшний день ведущим методом диагностики источника, типа, характера кровотечения и прогноза его рецидива, безусловно, остаётся неотложная фиброэзофагогастродуоденоскопия (ФЭГДС). Она играет чрезвычайно важную роль в определении лечебной тактики.
Основные показания к выполнению неотложного эндоскопического исследования верхних отделов пищеварительного тракта — наличие у больного признаков острого желудочно-кишечного кровотечения либо подозрение на него и необходимость проведения гемостаза через эндоскоп. Эффективность исследования тем выше, чем раньше его проводят — в идеале в течение первого часа (максимум 2 ч) с момента поступления в стационар. ФЭГДС позволяет обнаружить сочетанные осложнения заболевания — пилородуоденальный стеноз и пенетрацию язвы.
Показанием к повторной (динамической) ФЭГДС считают необходимость активного мониторинга источника кровотечения в связи с сохраняющимся риском его рецидива (активная контрольная ФЭГДС), рецидив кровотечения, развившийся в стационаре у больного предельного операционно-анестезиологического риска с язвенным кровотечением.
Подготовка к исследованию верхних отделов пищеварительного тракта заключается в возможно более полном опорожнении их просвета, отмывании от крови и сгустков слизистой оболочки пищевода, желудка и двенадцатиперстной кишки. Считают, что в большинстве случаев решить эту задачу можно путём промывания желудка «ледяной» водой через толстый желудочный зонд. Большой внутренний диаметр зонда позволяет эвакуировать крупные сгустки, а локальная гипотермия — достичь уменьшения интенсивности кровотечения или его полной остановки.
Анестезиологическое обеспечение экстренных эндоскопических вмешательств варьирует в широких пределах. Значительную часть исследований можно выполнить под местной анестезией зева с использованием премедикации. При беспокойном поведении больного, затрудняющем адекватный осмотр или выполнение гемостаза, применяют седативные средства внутривенно, а также внутривенный или (при нестабильном состоянии пациента) эндотрахеальный наркоз.
Рентгенологическое исследование верхних отделов пищеварительного тракта как метод экстренной диагностики желудочно-кишечных кровотечений отошло на второй план. В основном его применяют после остановки кровотечения в качестве метода получения дополнительной информации об анатомическом состоянии и мотор-но-эвакуаторной функции ЖКТ. Вместе с тем при отсутствии условий для выполнения эндоскопического исследования и большом практическом навыке врача рентгенологический метод позволяет обнаружить язву в 80—85% случаев.
Ангиографический метод диагностики кровотечений всё ещё имеет достаточно ограниченное использование. Его применяют в специализированных учреждениях, обладающих необходимым оборудованием. Хорошо разработанная техника катетеризации сосудов по Сельдингеру сделала возможным проведение селективной или даже суперселективной визуализации чревного ствола, верхней брыжеечной артерии и их ветвей, а также венозных стволов. Ограниченность метода применительно к условиям неотложной хирургии объясняется не только его технической сложностью, но и сравнительно небольшой информативностью: хорошее контрастирование экстравазатов из источника кровотечения возможно только при артериальном кровотечении достаточно большой интенсивности.
Показания к селективной ангиографии могут возникнуть в случаях повторных рецидивирующих кровотечений, когда источник геморрагии не установлен ни эндоскопическим, ни рентгенологическим методом исследования. Разумеется, диагностическую ангиографию выполняют как первый этап лечебного эндоваскулярного вмешательства, направленного на селективную инфузию сосудосуживающих препаратов, эмболизацию кровоточащей артерии или вены либо наложение трансъюгулярного интрапечёночного портосистемного соустья при портальной гипертензии и массивном кровотечении из ва-рикозно расширенных вен пищевода.
Накопленный опыт применения ангиографической диагностики эзофагогастродуоденальных кровотечений свидетельствует о том, что она может быть хорошим подспорьем в определении таких редких заболеваний, приводящих к кровотечению, как разрывы аневризм сосудов, сосудисто-кишечные фистулы, гемобилии, синдром портальной гипертензии.
Лабораторные методы
Экстренный анализ крови предоставляет ценную диагностическую информацию. Падение концентрации гемоглобина, уменьшение количества эритроцитов, снижение гематокрита, лейкоцитоз, несомненно, ориентируют в отношении тяжести кровопотери. Между тем, в первые часы от начала острого кровотечения все эти показатели могут меняться несущественно и, следовательно, имеют относительное значение. Истинная выраженность анемии становится ясной лишь по прошествии суток и более, когда уже разовьётся компенсаторная гемодилюция за счёт внесосудистой жидкости, необходимой организму для восстановления внутрисосудистого объёма крови.
Исследование ОЦК и его компонентов позволяет более точно определять объём кровопотери. Среди существующих методов наибольшее распространение получили красочный метод с краской Т-1824 (эванс синий) и изотопный метод с использованием меченых эритроцитов. Для условий неотложной хирургии приемлемы простые методы с использованием номограмм, например определение глобулярного объёма по данным гематокрита и концентрации гемоглобина. Наибольшее значение при остром кровотечении имеет снижение глобулярного объёма, так как восстановление его дефицита происходит медленно, в то время как снижение других показателей (объём циркулирующей плазмы и ОЦК) относительно быстро нивелируется.
У многих больных кровотечение возникает на фоне обострения язвенной болезни или в анамнезе удаётся отметить типичные признаки этого заболевания с характерным «язвенным» болевым синдромом и сезонностью обострений. В части случаев можно встретить указания на неэффективность проведённого ранее хирургического лечения, когда вновь появившийся болевой синдром следует связать, прежде всего, с образованием пептической язвы.
Кровотечение из разрывов слизистой оболочки области пище-водно-желудочного перехода (синдром Мэллори—Вейса) следует заподозрить, если у больных молодого возраста, злоупотребляющих алкоголем, многократные приступы рвоты заканчиваются появлением алой крови в рвотных массах. У пожилых больных необходимо выявить или исключить факторы, предрасполагающие к разрывам пищеводно-желудочного перехода (тяжёлые заболевания сердечно-сосудистой системы и лёгких, грыжи пищеводного отверстия диафрагмы).
Наличие неопределённых «желудочных» жалоб, похудание и нарушение общего состояния больного (так называемый синдром малых признаков) заставляют заподозрить опухоль желудка как причину кровотечения. Рвотные массы в этих случаях чаще имеют характер «кофейной гущи».
Для кровотечения из варикозно расширенных вен пищевода характерна многократная рвота тёмной кровью. Дегтеобразный стул появляется обычно через 1-2 сут. Из перенесённых заболеваний важно отметить болезни печени и желчевыводящих путей (в первую очередь цирроз печени), а также тяжёлые повторные приступы острого панкреатита. Из клинической практики известно, что эти больные нередко страдают алкоголизмом.
Данные анамнеза необходимо скрупулёзно уточнить, чтобы не пропустить очень важных факторов, способных обусловить острое желудочно-кишечное кровотечение. Необходимо выяснить наличие тяжёлых терапевтических заболеваний с выраженными гемодинами-ческими нарушениями (инфаркт миокарда, нарушение мозгового кровообращения и др.), системных заболеваний (болезни крови, уремия и др.), возможное лечение медикаментами, обладающими уль-церогенным эффектом.
Дифференциальный диагноз в части случаев проводят с кровотечением из верхних дыхательных путей, носоглотки и лёгких, когда заглатываемая больным кровь может симулировать кровотечение из пищеварительного тракта. Тщательно собранный анамнез и осмотр больного позволяют заподозрить лёгочное кровотечение: характерен ярко-красный цвет пенистой крови, выделяемой обычно при кашле или отдельными плевками. Следует также помнить, что чёрная окраска кала возможна после приёма некоторых медикаментов (препаратов железа, викалина, карболена и др.).
Лечение
Общие вопросы лечебной тактики
Современные подходы к лечению острых язвенных желудочно-кишечных кровотечений базируются на лечебной тактике, сочетающей активный характер диагностических и лечебных мероприятий с дифференцированным определением показаний к неотложной операции.
Коллективный многолетний опыт показывает, что большинство язвенных кровотечений (до 75%) останавливается под воздействием консервативного лечения. И только 25% больных с язвенной болезнью, осложнённой профузным желудочно-кишечным кровотечением, подлежат неотложному оперативному вмешательству. Возможности современной эндоскопии (не только диагностические, но и лечебные) в сочетании с энергичной противоязвенной терапией ещё более упрочили значение консервативного лечения этой группы больных. Поэтому основа лечебной тактики при острых желудочно-кишечных кровотечениях — консервативная терапия.
Решение важного вопроса лечебной тактики о показаниях к неотложной операции почти всегда представляет большие сложности. Правильно будет сказать, что операцию необходимо выполнить в оптимальные сроки для больного, когда тщательно взвешены все «за» и «против». Для этого нужно получить диагностические данные, оценить эффективность проводимого лечения и взвесить имеющиеся факторы риска.
Эндоскопическая остановка кровотечения
Лечебная эндоскопия при острых желудочно-кишечных кровотечениях обладает достаточно высокой эффективностью и позволяет осуществить временный гемостаз у подавляющего большинства больных. роме того, она предоставляет возможность адекватно подготовить их к срочному оперативному вмешательству, если оно показано. Последующая медикаментозная терапия даёт возможность предотвратить рецидив кровотечения и перенести операцию на этап плановой хирургии. Лечебная эндоскопия может стать единственным оправданным методом лечения у группы больных с предельно высоким операционным риском, когда выполнение неотложной операции невозможно. Этим больным обеспечивают динамическую ФЭГДС и повторный гемостаз.
Проведение эндоскопического гемостаза необходимо уже при первичном осмотре в условиях продолжающегося в момент эндоскопического исследования кровотечения. При язвенных геморрагиях продолжающееся струйное аррозивное кровотечение встречают у 8—10% больных. После его эндоскопической остановки возможный риск потенциального рецидива кровотечения существует в 80-85% случаев. Продолжающееся капиллярное кровотечение в виде диффузного просачивания отмечают у 10-15% больных с риском рецидива кровотечения до 5%.
Остановившееся на момент эндоскопического осмотра кровотечение со следами недавно перенесённой геморрагии также считают показанием к лечебной эндоскопии (профилактика рецидива). Стигмами состоявшегося кровотечения служат обнаруживаемые в краях и/или дне язвы мелкие тромбированные сосуды в виде тёмно-коричневых или тёмно-красных пятен, плотно фиксированный к язвенному кратеру тромб-сгусток или видимый крупный тромбированный сосуд. При такой эндоскопической картине рецидив кровотечения вероятен у 25% больных.
Показание для проведения эндоскопического гемостаза во время динамической ФЭГДС (у больных с предельно высоким операци-онно-анестезиологическим риском) — отрицательная динамика со стороны источника кровотечения, когда сохраняются интактными ранее обработанные сосудистые структуры, появляются новые тромбированные сосуды либо развивается рецидив кровотечения.
Для воздействия на источник кровотечения через эндоскоп применяют различные методы, отличающиеся по физическим свойствам и механизму действия, но зачастую сходные по эффективности. В арсенале эндоскопического гемостаза следующие методы: моно- и биактивная диатермокоагуляция, термокаутеризация, аргоно-плаз-менная коагуляция; инъекционные методы введения эпинефрина, 96% раствора этанола, а также специальных склерозантов, методы эндоклипирования.
Инфузионно-трансфузионная терапия необходима для восстановления основных параметров гомеостаза, нарушенных в результате острого развившегося дефицита ОЦК. Хорошо известно, что организм человека способен выдержать острую потерю 60—70% объёма эритроцитов, но утрата 30% объёма плазмы не совместима с жизнью. Первоочередные задачи — введение в сосудистое русло адекватного количества коллоидных и кристаллоидных растворов для устранения дефицита ОЦК, нормализация микроциркуляции и реологии крови, коррекция водно-электролитного обмена. Особенности инфузион-ной терапии при кровотечении рассмотрены в главе 3 (раздел «Шок»).
Критериями восстановления ОЦК служат симптомы, указывающие на уменьшение степени гиповолемии: повышение АД, уменьшение ЧСС, увеличение пульсового давления, потепление и восстановление розовой окраски кожных покровов. Важными показателями адекватности проводимой терапии считают почасовой диурез и ЦВД.
Лекарственная терапия язвенных кровотечений
Особое значение в лечении кровотечений язвенной этиологии имеют антисекреторные препараты. Обоснованием к их применению служат следующие положения:
соляная кислота и пепсин препятствуют образованию тромба и вызывают лизис уже сформированного сгустка;
критический порог рН, при котором пепсин теряет свою активность, составляет 6;
агрегация тромбоцитов происходит при рН>6;
для предотвращения рецидива кровотечения относительно безопасный уровень концентрации водородных ионов рН= 4.
Внедрение в клиническую практику парентеральных форм антагонистов Н2-гистаминовых рецепторов, а несколько позже и ингибиторов протонной помпы, обладающих мощным антисекреторным эффектом, даёт возможность создать в полости желудка оптимальные условия для предотвращения рецидива кровотечения и заживления язвы, позволяет отодвинуть операцию на этап плановой хирургии либо вообще отказаться от неё. Особые надежды возлагают на применение парентеральных форм ингибиторов протонной помпы. Эффективность проводимой терапии антисекреторными средствами целесообразно контролировать 24-часовой рН-метрией.
Антихеликобактерные средства ускоряют регенеративные процессы. Антациды и препараты, обладающие цитопротективным действием (синтетические аналоги простагландинов), назначают в качестве патогенетически обоснованных средств для скорейшего заживления язвенных и эрозивных поражений, ставших источником кровотечения.
Питание больных с желудочно-кишечным кровотечением — составная часть консервативной терапии. Вопросы энтерального и парентерального питания у различных групп больных решают неоднозначно, это зависит от избранной лечебной тактики.
Пациентам, прооперированным в неотложном порядке, перораль-ное питание следует назначить только после восстановления перистальтики (как правило, с 3—4-х суток после операции). До этого следует проводить полное парентеральное питание.
Группе больных с высокой угрозой рецидива кровотечения после эндоскопического гемостаза на фоне консервативного лечения (динамические эндоскопические осмотры в сочетании с медикаментозной терапией) до исчезновения риска кровотечения также следует назначить парентеральное питание.
Пациентам с невысокой угрозой рецидива кровотечения после очищения кишечника от излившейся крови (как правило, в течение суток) следует назначить диету Мейленграхта (частое дробное питание; пищу, полноценную по составу, механически щадящую, богатую молочными продуктами и витаминами).
Хирургическая тактика
Кровотечение из гастродуоденальных язв — показание к неотложной операции:
экстренной, если с помощью нехирургических методов его не удаётся остановить;
срочной, когда слишком велика угроза его рецидива.
Таким образом, в экстренном порядке оперируют следующих пациентов:
больных с профузным продолжающимся кровотечением, геморрагическим шоком и клинико-анамнестическими данными, свидетельствующими о кровотечении язвенной природы;
больных с массивным кровотечением, если консервативные мероприятия, включая эндоскопические методы, оказались неэффективными;
больных с рецидивом кровотечения в стационаре.
Срочная операция показана больным с язвенным кровотечением, остановка которого консервативными способами представляется недостаточно надёжной, или есть указания на высокий риск рецидива кровотечения. Больным этой группы хирургическое вмешательство, как правило, проводят в течение 12-24 ч с момента поступления (время, необходимое для подготовки больного к операции). Следует лишь подчеркнуть, что доля таких больных по мере внедрения надёжных средств неоперативного гемостаза постепенно сокращается, о чём уже было сказано выше. Особые надежды возлагают на комбинированный способ ведения таких больных, включающий адекватный эндоскопический гемостаз и современную противоязвенную терапию, включающую дозированное внутривенное введение блокатора протонной помпы под контролем 24-часовой рН-метрии.
Прогноз рецидива кровотечения, остановленного эндоскопически, основывают на учёте клинико-лабораторных данных, отражающих в основном интенсивность кровотечения, и результатах эндоскопического исследования. Клинико-лабораторные критерии высокой угрозы рецидива кровотечения:
клинические признаки геморрагического шока;
обильная рвота кровью и/или массивная мелена;
дефицит глобулярного объёма, соответствующий тяжёлой степени кровопотери.
Эндоскопические критерии высокой угрозы возврата кровотечения:
крупные тромбированные сосуды в язвенном кратере;
язвенный дефект большого диаметра и глубины;
локализация язвы в проекции крупных сосудов.
Наличие двух любых неблагоприятных факторов расценивают как свидетельство существующей угрозы повторного кровотечения.
Если кровотечение остановлено консервативными методами и риск его возобновления невелик, неотложное оперативное вмешательство не показано, таких больных ведут консервативно.
В практической хирургии выделяют ещё одну группу больных, для которых неотложная операция любого объёма неприемлема. Это больные преклонного возраста с предельной степенью операцион-но-анестезиологического риска, как правило, обусловленного декомпенсацией сопутствующих заболеваний на фоне перенесённой кровопотери. Таких больных, даже при указаниях на высокий риск рецидива кровотечения, вынужденно ведут консервативно, как указано выше, с динамическим эндоскопическим контролем. Контрольные эндоскопические исследования носят в таких случаях лечебный характер, их проводят ежедневно до исчезновения риска рецидива кровотечения. Хирургическую операцию таким больным проводят как сугубо вынужденную меру («операция отчаяния»).
Выбор метода хирургического вмешательства, прежде всего, зависит от тяжести состояния больного, степени операционно-анестезио-логического риска, а также локализации и характера кровоточащей язвы. До сравнительно недавнего времени вопрос о выборе метода операции при этом осложнении язвенной болезни решали фактически однозначно — резекция желудка. Сейчас у хирурга в арсенале существуют следующие средства хирургического лечения язвенных желудочных кровотечений.
Органосохраняющив операции с ваготомией (как правило, стволовой) применительно к запросам неотложной хирургии имеют особое значение, так как отличаются технической простотой. Остановка кровотечения из дуоденальной язвы заключается в пилородуодено-томии, иссечении и/или прошивании источника кровотечения отдельными швами (рис. 9-4), а при пенетрации — с выведением язвенного кратера из просвета кишки (экстрадуоденизацией) и последующей стволовой ваготомией с пилоропластикой. Летальность после этой операции составляет 3-5%.
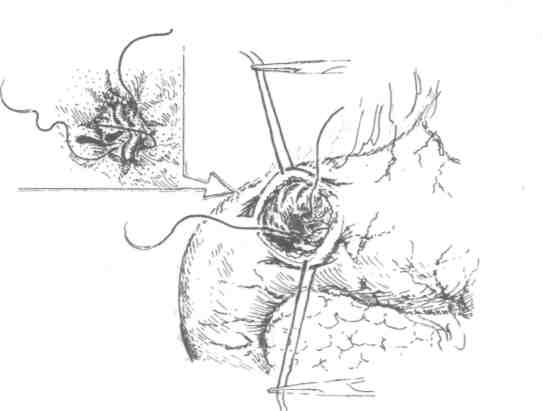
Рис. 9-4. Прошивание кровоточащей язвы. Выполнена продольная гастро-дуоденотомия. Края разреза разведены в поперечном направлении. На задней стенке двенадцатиперстной кишки видна язва с сосудом, которую прошивают 8-образным швом.
Антрумэктомия с ваготомией при дуоденальной локализации кровоточащей язвы показана больным со сравнительно невысокой степенью операционного риска (молодой возраст, небольшая или средняя степень кровопотери). Негативная сторона этой операции — техническая сложность, вместе с тем она обеспечивает более надёжную остановку кровотечения и большую радикальность лечения язвенной болезни. Последнее обстоятельство немаловажно, когда массивному кровотечению предшествует длительный анамнез с упорным течением заболевания. Кроме того, такой вариант операции показан пациентам с сочетанными осложнениями — кровотечением и поздней стадией стеноза, а также при сочетанной форме язвенной болезни. При проведении вмешательства хирург должен быть готов к закрытию «трудной» дуоденальной культи, когда речь идёт о язве, пенет-рирующей в поджелудочную железу. Летальность после этой операции составляет 5-10%.
Пилоропластику с иссечением или прошиванием язвы без ваготомии выполняют вынужденно в связи с продолжающимся кровотечением, которое невозможно остановить эндоскопическим способом, как правило, у пациентов пожилого и старческого возрастов с крайне высоким операционно-анестезиологическим риском. Послеоперационная летальность у таких больных превышает 50%.
Резекция желудка (рис. 9-5) показана при кровоточащей желудочной язве, если степень операционного риска сравнительно невысока. Послеоперационная летальность после резекции составляет 2-7%.
Иссечение язвы (клиновидная резекция) или прошивание желудочной язвы через гастротомический доступ можно предпринять у больных с предельно высокой степенью операционного риска. Этим технически несложным оперативным вмешательством можно остановить кровотечение из язвы желудка. Такие операции носят характер «вынужденных», когда другие средства гемостаза исчерпаны. Послеоперационная летальность превышает 50%.
Послеоперационный период
Особенности ведения ближайшего послеоперационного периода зависят от тяжести состояния больных (степень кровопотери, пожилой возраст и сопутствующие заболевания), а также от характера проведённого оперативного вмешательства. Послеоперационный период У больных, перенёсших прошивание кровоточащей язвы и органосбе-регающие операции с ваготомией, имеет особенности. В ближайшем
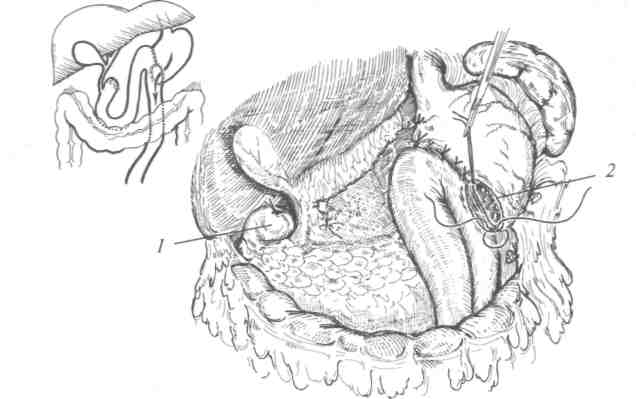
Рис. 9-5. Резекция желудка по Гофмейстеру—Финстереру (схема операции): 1 — культя двенадцатиперстной кишки; 2 — гастроэнтероанастомоз.
послеоперационном периоде больному проводят курс противоязвенной терапии, включающий ингибиторы протонной помпы либо последнее поколение Н2-блокаторов, а также комплекс антихеликобак-терной терапии. Особенность послеоперационного периода у этих больных — необходимость профилактики моторно-эвакуаторных расстройств оперированного желудка.
Прогноз
Арсенал современных консервативных и оперативных методов позволяет с удовлетворительными результатами решить сложный вопрос об угрозе жизни больного с профузным язвенным кровотечением. Многое зависит от своевременности и адекватности оказания неотложной помощи.
После оценки ближайших результатов операций (резецирующих, органосохраняющих с ваготомией) больные, находящиеся на диспансерном наблюдении, должны быть через 2-3 мес переданы врачу-гастроэнтерологу. Прогноз рецидива язвы зависит не только от проведённого оперативного вмешательства (оно должно быть патофизиологически обоснованным), но и от хорошо организованной консервативной терапии (поддерживающая и противорецидивная антисекреторная терапия, антихеликобактерное лечение с достижением эрадикации). Особое место занимают больные, перенёсшие язвенные кровотечения из желудочной язвы. Им необходимо пристальное внимание из-за возможности ракового перерождения (малигнизации) хронической язвы желудка.
Язвенный пилородуоденальный стеноз
Около трети больных, оперированных по поводу осложнений язвенной болезни, составляют пациенты с пилородуоденальный стенозом. Мужчины страдают этой патологией чаще, чем женщины (5:1). Обычно это больные среднего возраста. Отмечаемое снижение частоты случаев, требующих хирургического лечения, можно связать с активным внедрением в клиническую практику новых медикаментозных средств.
Классификация
Существуют клинические, анатомические и функциональные критерии выделения различных стадий пилородуоденального стеноза. При этом их можно определить лишь при сопоставлении клинических, рентгенологических, эндоскопических данных и результатов специального исследования моторной функции желудка. В клинической практике чаще всего выделяют три стадии этого патологического процесса (табл. 9-2).
Сочетание рубцово-язвенного стеноза с другими осложнениями язвенной болезни (перфорацией, кровотечением) не следует считать большой редкостью. В части случаев пилородуоденальный стеноз развивается после возникшего ранее осложнения (ушивание перфо-ративной язвы или эпизод кровотечения, излеченный без операции).
Основные черты патологии
Деформация и сужение пилородуоденальной области развиваются вследствие рубцевания многократно рецидивирующих язв, что влечёт за собой ту или иную степень её непроходимости и замедление эвакуации желудочного содержимого. Чтобы компенсировать опорожнение желудка, происходят гипертрофия его мышечной оболочки и усиление двигательной активности. С прогрессированием стеноза желудок теряет свои компенсаторные возможности, растягивается,
Таблица 9-2 |
. Классификация язвенного пилородуоденального стеноза |
|
|
Исследо- |
Стадии стеноза |
||
вания |
компенсированный |
субкомпенсированный |
декомпенсированный |
Клинические |
Начальные признаки стеноза. Проба с зондированием (+). Лечение уменьшает до нормы объём аспирируемого содержимого |
Яркая клиника стеноза. Нарушение водно-солевого обмена, снижение массы тела. Проба с зондированием (++), застойное содержимое. Лечение уменьшает объём аспирируемого содержимого |
Рвоты может не быть. Общее состояние тяжёлое, кахексия, обезвоживание, гипопротеинемия, гипокалиемия, азотемия, алкалоз. Проба с зондированием (+++), постоянное наличие пищевых масс в желудке |
Рентгенологические |
Желудок нормальных размеров или несколько расширен, перистальтика усилена. Сужение пилородуоденального канала. Задержка эвакуации на 6—12 ч |
Желудок расширен, натощак определяется жидкость. Перистальтика ослаблена. Сужение пилородуоденального канала. Задержка эвакуации на 12—24 ч |
Желудок резко растянут, натощак определяется большое количество содержимого. Перистальтика резко ослаблена. Задержка эвакуации более чем на 24 ч |
Эндоскопические |
Выраженная рубцовая деформация пилородуоденального канала с сужением его просвета до 0,5—1 см |
Желудок растянут. Пилородуоде-нальный канал сужен до 0,3—1 см за счёт резкой рубцовой деформации |
Желудок больших размеров. Атрофия слизистой оболочки. Различной степени рубцовые сужения пилородуоденального канала |
Моторная функция желудка (иономано- метрия) |
Тонус желудка нормальный или повышенный. Сокращения ан-трального отдела усилены, часто носят спастический характер. Замедление ритма голодных сокращений желудка. После пищевой нагрузки — редкие сокращения желудка в период задержки начальной эвакуации |
Тонус желудка нормальный или незначительно сниженный. Сохраняется градиент давления между смежными отделами. Натощак и после пищевой нагрузки — редкие сокращения в теле и антральном отделе желудка. Значительное снижение силы редких сокращений после растяжения желудка пищей. Выраженная задержка начальной эвакуации |
Тонус желудка резко снижен, одинаковый в теле и антральном отделе. Базальный тонус равен пластическому. Натощак и после пищевой нагрузки — редкие сокращения сниженной амплитуды, особенно в антральном отделе. Длительная задержка начальной эвакуации |
увеличивается в размерах, ослабляется его перистальтика, что ещё в большей степени усугубляет нарушения желудочной эвакуации. Постепенно появляются признаки декомпенсации патологического процесса, характеризующиеся рвотой застойным желудочным содержимым, значительным замедлением эвакуации пищи из желудка, нарушением питания и жизнедеятельности больного. Отмечают также прогрессирующий метаболический алкалоз (хлорид-чувствительный), нарушение водно-электролитного и белкового баланса (подробности описаны в главе 3, раздел «Нарушения метаболизма»),
К этому следует добавить, что стеноз с выраженной дилатацией и нарушениями моторно-эвакуаторной функции желудка приводит к резкому истончению его стенки, потере компенсаторных возможностей восстановления моторной активности и микробному «загрязнению» слизистой оболочки вследствие гнилостного брожения застоявшейся пищи.
Диагностика Клиническая симптоматика
Наряду с «язвенными» болями в стадии компенсации стеноза настойчиво возникает чувство переполнения в эпигастральной области после приёма пищи. Эпизодически появляется рвота, на некоторое время приносящая больному облегчение. При зондировании желудка эвакуируют около 200-500 мл желудочного содержимого с кислым неприятным запахом и примесью недавно принятых пищевых масс. Общее состояние больного существенно не страдает.
При субкомпенсации больной ощущает постоянное чувство тяжести и переполнения в эпигастральной области, сочетающееся с болью и отрыжкой воздухом. При физикальном исследовании можно отметить «шум плеска» в проекции желудка. Ежедневно, по несколько раз в день бывает обильная рвота сразу или через 1-2 ч после еды только что принятой и съеденной накануне пищей, без признаков гнилостного брожения. Натощак в желудке при зондировании определяют большое количество содержимого. В этой стадии стеноза больной отмечает похудание.
Некомпенсированный стеноз характеризуется прогрессирующим желудочным стазом, растяжением желудка. Состояние больного значительно ухудшается, происходит резкое обезвоживание, снижение количества отделяемой мочи. Характерна землистая окраска потерявших тургор кожных покровов. Недомогание, апатия и вялость
нивелируют другие симптомы болезни. Гипокалиемия проявляется выраженной мышечной слабостью, нарушениями сердечного ритма и проводимости. Гипохлоремия чревата возникновением судорожного синдрома (так называемая хлоропривная тетания). Помимо общих судорог (иногда принимаемых за эпилептический припадок), возникает тризм (спазм жевательной мускулатуры). Определяются симптомы Труссо («рука акушера») и Хвостека (подергивание мышц лица при поколачивании в области лицевого нерва). Чувство распирания в эпигастральной области заставляет больного самостоятельно вызывать рвоту. Рвотные массы в огромном количестве содержат зловонное разлагающееся содержимое с остатками многодневной пищи. При осмотре обращает внимание сухость языка и кожных покровов. При аускультации слышен «шум плеска» в проекции желудка. Зон-довые пробы позволяют эвакуировать большое количество застойного желудочного содержимого с признаками брожения и гниения. Опорожнение желудка в стадиях субкомпенсации и декомпенсации значительно облегчает самочувствие больных.
Инструментальные диагностические методы
Особую роль при этом осложнении язвенной болезни играет рентгенологическое исследование. В стадии компенсации выявляют некоторое увеличение размеров желудка, рубцово-язвенную деформацию пилородуоденальной зоны. Отмечают замедление желудочной эвакуации до 12 ч. При субкомпенсированном стенозе обнаруживают признаки начинающейся декомпенсации моторики желудка — увеличение его в размерах, ослабление перистальтической активности. В этой стадии появляется симптом так называемого «трёхслойного желудка» (трёхслойное содержимое — контрастное вещество, слизь, воздух). Задержка эвакуации составляет более 12 ч. Стадия декомпенсации характеризуется значительным увеличением размеров желудка, снижением перистальтики, резким сужением пилородуоде-нального канала и выраженными нарушениями желудочной эвакуации. Бариевая взвесь остаётся в желудке более 24 ч.
ФЭГДС. В первой стадии отмечают выраженную рубцовую деформацию пилородуоденального канала с сужением его просвета до 0,5—1 см. Можно обнаружить гипертрофию слизистой оболочки желудка и усиленную перистальтику. Во второй стадии метод даёт точные представления о значительном сужении пилородуоденального канала, задержке эвакуации желудочного содержимого, увеличении размеров желудка. В третьей стадии выявляет резкое сужение пило-одуоденального канала, истончение слизистой оболочки желудка, тсутствие перистальтики желудочной стенки и чрезмерное расши-ение просвета желудка. Исследование моторной функции методом иономанометрии даёт представление о тонусе, частоте, амплитуде сокращений желудка натощак и после приёма пищевого раздражителя, позволяет определить время задержки начальной эвакуации. Для компенсированного стеноза характерен редкий ритм активных желудочных сокращений. При субкомпенсированном моторная функция ослабляется. В стадии декомпенсации выявляют резкое снижение тонуса и двигательной активности желудка.
УЗИ. Выполнение УЗИ брюшной полости натощак в поздних стадиях стеноза позволяет визуализировать наполненный жидкостью желудок. Метод неточен в плане определения стадии стеноза, но может быть полезным для экспресс-диагностики.
Лабораторная диагностика
При помощи лабораторной диагностики (при поздних стадиях стеноза) определяют признаки метаболического (хлор-чувствительного) алкалоза, эксикоза, гипогликемии, гипопротеинемии.
Дифференциальная диагностика
Дифференциальный диагноз необходимо проводить с опухолевым поражением антрального отдела желудка, опухолью головки поджелудочной железы с прорастанием в двенадцатиперстную кишку.
Лечение Консервативная терапия
Консервативная терапия при пилородуоденальном стенозе становится предоперационной подготовкой больных к плановому хирургическому вмешательству. Она направлена, прежде всего, на заживление активной язвы с применением современных антисекреторных средств и антихеликобактерных препаратов. Кроме того, необходимо обеспечить коррекцию нарушений водно-электролитного обмена, белкового состава плазмы крови и восстановление массы тела. Этих целей достигают парентеральным введением солевых и белковых
препаратов. В поздних стадиях стеноза одним из наиболее эффективных способов подготовки больного к операции служит энтераль-ное зондовое питание (зонд проводят с помощью эндоскопа за уровень сужения в тощую кишку). В настоящее время существует много питательных смесей для энтерального питания. В клинической практике наибольшее распространение получили сбалансированные пищевые смеси: Нутризон, Изокал, Эншур.
Большое внимание следует уделить восстановлению или улучшению двигательной активности желудка, создав условия для профилактики развития послеоперационных осложнений, включающих моторно-эвакуаторные расстройства. С этой целью проводят постоянную или фракционную аспирацию желудочного содержимого, промывание желудка холодной водой, назначают современные про-кинетические средства (см. ниже).
Хирургическая тактика
Процесс рубцевания пилородуоденальной зоны носит необратимый и прогрессирующий характер. Поэтому лечение данного осложнения может быть только оперативным, независимо от тяжести клинических проявлений, степени расширения желудка, нарушений его моторной и эвакуаторной функций. Пилородуоденальный стеноз — показание к хирургическому лечению. При выборе метода оперативного вмешательства следует учитывать стадию развития стеноза и степень нарушений моторной функции желудка и двенадцатиперстной кишки, а также особенности желудочной секреции и степень операционного риска.
Стволовая ваготомия в сочетании с дренирующими желудок операциями — наиболее частое вмешательство при этой патологии. Его выполняют более чем у половины больных. Наиболее аргументированы показания к этой операции при компенсированном пило-родуоденальном стенозе. Её можно выполнить и в части случаев субкомпенсированного стеноза, когда больным была проведена адекватная предоперационная подготовка (восстановление водно-электролитных нарушений, заживление активной язвы, нормализация тонуса желудка и темпов желудочного опорожнения). Летальность при такой операции, выполняемой в плановом порядке, близка к нулю.
Лапароскопическая стволовая ваготомия с пилоропластикой из минидоступа — новое техническое направление малоинвазивной хирургии. Её выполняют при компенсированном пилородуоденальном стенозе. Летальность после таких операций также стремится к нулевой отметке.
Стволовая ваготомия с антрумэктомией показана при пилородуо-денальных стенозах с признаками субкомпенсации и декомпенсации, а также при сочетанной форме язвенной болезни. Комбинация резекции желудка со стволовой ваготомией позволяет уменьшить объём удаляемой части органа, сохраняя при этом лечебный эффект операции. Летальность при этих операциях составляет 0—2%.
Резекция желудка (гемигастрэктомия) показана больным с деком-пенсированным стенозом и сниженной кислотообразующей функцией желудка. Летальность при этом составляет 1-4%.
Гастроэнтеростомия как окончательный способ лечения показана пожилым больным, находящимся в тяжёлом состоянии, с поздними стадиями стеноза, фактически при «отзвучавшей» язве. Этих больных по ряду причин не удаётся подготовить к плановому вмешательству, что обусловлено чаще всего крайне высоким опера-ционно-анестезиологическим риском. Обычно при язвенном пило-родуоденальном стенозе формируют задний позадиободочный гаст-роэнтероанастомоз по Гакеру. В настоящее время такие операции приходится выполнять довольно редко.
Послеоперационный период
Ведение послеоперационного периода у этой группы больных имеет свои особенности. Следует принимать во внимание, что в условиях язвенной болезни, осложнённой стенозом, существенно страдает моторно-эвакуаторная функция желудка. Длительность заболевания, частые обострения, активная язва на момент госпитализации, нарушения координации работы смежных отделов желудка и двенадцатиперстной кишки и другие факторы позволяют считать, что риск развития моторно-эвакуаторных нарушений после операций с ваготомией может быть крайне высоким. Именно поэтому в предоперационном периоде назначают препараты, нормализующие моторику (ме-токлопрамид, домперидон). В некоторых случаях необходимо и проведение зондового энтерального питания. В ходе операции для профилактики нарушений моторно-эвакуаторной функции устанавливают двухканальный зонд. При этом один его канал открывается в желудке и служит для декомпрессии последнего в послеоперационном периоде, второй — в тощей кишке за связкой Трейтца, он предназначен для энтерального кормления больных.
Диагностировать развитие нарушений желудочной эвакуации в послеоперационном периоде следует по клиническим и инструментальным признакам. Жалобы могут быть выражены неярко, но в условиях перенесённой ваготомии следует обращать внимание на минимальные проявления. Такими признаками следует считать тяжесть в желудке, возникающую вечером или после приёма пищи, отрыжку, изжогу, икоту. Для диагностики нарушения желудочной эвакуации наиболее простой способ — зондирование желудка с эвакуацией содержимого. УЗИ поможет установить размеры желудка и примерное содержание жидкости натощак. Окончательным методом определения степени и вида нарушения желудочной эвакуации служит рентгенологическое исследование с контрастным веществом.
Параллельно зондовому питанию в послеоперационном периоде следует проводить медикаментозное и физиотерапевтическое лечение, направленное на профилактику и ликвидацию развившегося замедления желудочной эвакуации.
Нельзя забывать о проведении комплексного противоязвенного лечения, состоящего из антисекреторного препарата (Н2-блокатор, блокатор протонной помпы), препарата висмута в комбинации с антибиотиками.
Прогноз
Основная причина летальных исходов у больных со стенозом — выраженные нарушения гомеостаза, возникшие на фоне поздних стадий стеноза, а также декомпенсация сопутствующей патологии у пожилых больных.
