
- •1 Основные понятия
- •2 Парообразование в – диаграмме
- •3 Тройная точка. Правило фаз
- •4 Влажный пар и его параметры
- •???????????????????????5 Ts– диаграмма водяного пара
- •???????????6 Is – диаграмма водяного пара
- •7 Расчет основных процессов водяного пара
- •8. Основные определения
- •9 Относительная влажность воздуха.Температура точки росы
- •11 Уравнение первого закона термодинамики для потока
2 Парообразование в – диаграмме
Изобарный
процесс парообразования в
–
диаграмме изображается горизонтальной
линией a-b-c-d
у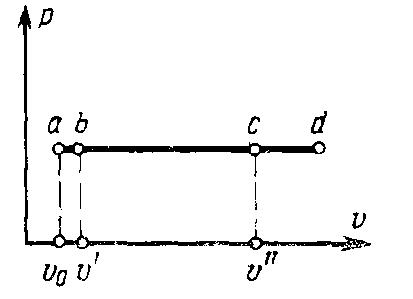 которой участок a-b
соответствует подогреву жидкости от
0°С до температуры кипения, участок b-c
– превращению кипящей воды в сухой
насыщенный пар и участок с-d
– перегреву пара до заданной температуры.
Таким образом, на графике величины
которой участок a-b
соответствует подогреву жидкости от
0°С до температуры кипения, участок b-c
– превращению кипящей воды в сухой
насыщенный пар и участок с-d
– перегреву пара до заданной температуры.
Таким образом, на графике величины
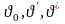 соответствуют
удельным объемам жидкости при 0°С,
кипящей жидкости и сухого насыщенного
пара.
соответствуют
удельным объемам жидкости при 0°С,
кипящей жидкости и сухого насыщенного
пара.
При
подогреве жидкости удельный объем ее
несколько увеличивается а процесс
парообразования характеризуется резким
увеличением удельного объема. Так,
например, для воды при нормальном
давлении
 =
0,001м3/кг,
=
0,001м3/кг,
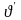 =0,001044
м3/кг,
=0,001044
м3/кг,
 =
1,677 м3/кг,
т. е. при подогреве воды от 0°С до
температуры кипения (100°С), удельный
объем увеличивается всего лишь на 4,4%,
а в процессе парообразования более чем
в 1600 раз.
=
1,677 м3/кг,
т. е. при подогреве воды от 0°С до
температуры кипения (100°С), удельный
объем увеличивается всего лишь на 4,4%,
а в процессе парообразования более чем
в 1600 раз.
Построив
в
 диаграмме аналогичные графики для
нескольких различных давлений и соединив
одноименные точки плавными линиями
(рис. 7.4), м
диаграмме аналогичные графики для
нескольких различных давлений и соединив
одноименные точки плавными линиями
(рис. 7.4), м ожно
заметить, что в связи с очень малой
сжимаемостью жидкости линия а – а1 –
а2…, выражающая зависимость
ожно
заметить, что в связи с очень малой
сжимаемостью жидкости линия а – а1 –
а2…, выражающая зависимость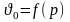 ,
практически вертикальна; в связи с тем,
что при увеличении давления возрастает
температура кипения, от которой зависит
,
линия b–b1–b2..., выражающая зависимость
,
практически вертикальна; в связи с тем,
что при увеличении давления возрастает
температура кипения, от которой зависит
,
линия b–b1–b2..., выражающая зависимость
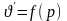 ,
идет круто вверх с наклоном в правую
сторону; наконец, линия c – c1 – c2...,
выражающая зависимость
,
идет круто вверх с наклоном в правую
сторону; наконец, линия c – c1 – c2...,
выражающая зависимость
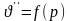 ,
имеет гиперболический характер. Например,
для водяного пара она до давления 20 бар
довольно точно описывается уравнением
Молье
,
имеет гиперболический характер. Например,
для водяного пара она до давления 20 бар
довольно точно описывается уравнением
Молье
![]() ,
(7.1)
,
(7.1)
где
р выражено в барах, а
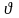 – в кубических метрах на килограмм.
– в кубических метрах на килограмм.
Линия b – b1– b2…, отделяющая область жидкости от области влажного пара и характеризуемая равенством х = 0, называется нижней пограничной кривой; линия c – c1 – c2..., отделяющая область влажного пара от области пара перегретого и характеризуемая равенством х=1, называется верхней пограничной кривой.
С
ростом давления разность
![]() уменьшается и пограничные кривые
сближаются, плавно сходясь в критической
точке k, где они обе принимают горизонтальное
направление.
уменьшается и пограничные кривые
сближаются, плавно сходясь в критической
точке k, где они обе принимают горизонтальное
направление.
Как видно из графика, точка k соответствует некоторому предельному состоянию вещества, при котором исчезает видимое различие между жидкостью и паром. Критические параметры, характеризующие это состояние для каждого вещества, имеют определенные значения. Так, например, для воды ркр=221,15 бар, ркр=374,12°С, ркр= 0,003147 м3/кг.
3 Тройная точка. Правило фаз
влажный пар представляет собой равновесную систему, в которой одно и то же вещество находится в двух различных агрегатных состояниях.
О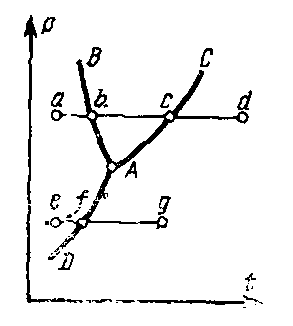 тдельные
части равновесной системы, называются
фазами, а происходящий в ней переход из
одного агрегатного состояния в другое
называется фазовым превращением.
тдельные
части равновесной системы, называются
фазами, а происходящий в ней переход из
одного агрегатного состояния в другое
называется фазовым превращением.
Р
Рисунок 7.5
ассмотрим вопрос фазовых превращении вещества в более широком плане, включая в него и твердую фазу. Для этого удобно использовать pt-диаграмму, т. е. систему координат, в которой по оси абсцисс откладывается температура вещества, а по оси ординат давление, под которым оно находится (рис. 7-5).Если точка а в такой диаграмме изображает исходное состояние вещества, взятого в твердой фазе, то процесс изобарного подвода тепла с переходом вещества сначала в. жидкое, а затем в газообразное состояние изобразится горизонтальной линией a-b-c-d, причем участок ее a-b соответствует нагреву твердой фазы до расплавления, участок b-c нагреву жидкой фазы до температуры кипения и участок c-d перегреву газовой фазы (т. е. паров данного вещества).
Отсюда видно, что точка b соответствует двухфазной системе твердое тело– жидкость, а точка с –двухфазной системе жидкость–пар (т. е. всем состояниям влажного пара).
С увеличением давления точка b смещается влево, так как температура плавления уменьшается, а точка с смещается вправо, так как температура кипения увеличивается. Следовательно, с ростом давления точки b и с расходятся.
Наоборот, с уменьшением давления точки b и с сближаются и, наконец, сливаются в одной точке А.
При более низких давлениях переход вещества из твердого состояния в газообразное происходит непосредственно, без промежуточного превращения в жидкость (например, по линии e-f-g, на которой точка f соответствует двухфазной системе твердое тело – перегретый пар). Такой процесс называется сублимацией или возгонкой. Обратный переход вещества из газообразного состояния в твердое обычно называют десублимацией.
Таким образом, получается фазовая диаграмма, в которой площадь, расположенная левее линии В-А-D, соответствует твердой фазе, площадь, расположенная выше линии В-А-С,– жидкой фазе и площадь, расположенная правее линии С-А-D,– газовой фазе (перегретому пару).
Точка А, соответствующая такому состоянию вещества, при котором оно может находиться во всех трех фазах, называется тройной тоxкой. Каждому веществу в тройной точке свойственны строго определенные значения всех параметров.
Так,
для воды ра
= 0,006112 бар,
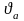 =1,00021
л/кг
=1,00021
л/кг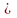 0,001
м3/кг,
tа=0,0075
0,01°С.
тройная точка принята за начало отсчета
внутренней энергии и энтропии воды и
водяного пара, т. е. Uа=0
и sа=
0.
0,001
м3/кг,
tа=0,0075
0,01°С.
тройная точка принята за начало отсчета
внутренней энергии и энтропии воды и
водяного пара, т. е. Uа=0
и sа=
0.
