
- •Понятие химическое вещество и химическая реакция. Основные типы химических реакций.
- •Классификация химических реакций.
- •Понятие химическое в-во и хим. Реакция.
- •Классификация химических реакций.
- •I. В зависимости от механизма реакции могут быть отнесены к простым и сложным.
- •2) Последовательными реакциями называются реакции, при которых продукт начальной реакции является исходным веществом для следующей реакции.
- •II. По признаку изменения числа исходных и конечных веществ реакции можно выделить такие типы:
- •1. Реакции, идущие без изменения степеней окисления элементов:
- •2. Окислительно-восстановительные реакции:
- •IV. По признаку выделения или поглощения энергии реакции делят на экзотермические и эндотермические.
- •V. По признаку обратимости реакции подразделяются на две группы: необратимые и обратимые.
- •1) Необратимые реакции могут идти только в одном направлении и протекают до полного завершения.
- •2) Обратимыми называются реакции, протекающие в двух противоположных направлениях: прямом и обратном.
2) Последовательными реакциями называются реакции, при которых продукт начальной реакции является исходным веществом для следующей реакции.
Последовательные реакции протекают согласно схемам:
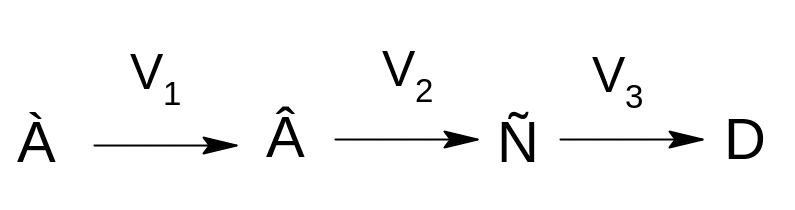

Таковы, например, реакции омыления эфиров двухосновных кислот щелочью. В последовательных реакциях скорость процесса в целом определяется скоростью самой медленной стадии.
3) Сопряженные реакции, это реакции одна из которых идет самопроизвольно, тогда, как другая имеет место только в присутствии первой. В таком случае говорят, что одна реакция индуцирует протекание другой, т. е. имеет место химическая индукция. Идущая самопроизвольно первая реакция называется первичной, индуцируемая реакция - вторичной.
Сопряженные реакции протекают по схеме:

К сопряженным реакциям относят цепные реакции, протекающие по свободно-радикальному механизму.
Свободный радикал – это атом, имеющий неспаренный электрон и обладающий высокой химической активностью
Особым примером сопряженных реакций является реакция между хлором и водородом. При температуре 150—250°С в темноте реакция практически не идет. Однако она протекает с высокой скоростью в тех же условиях в присутствии паров натрия:

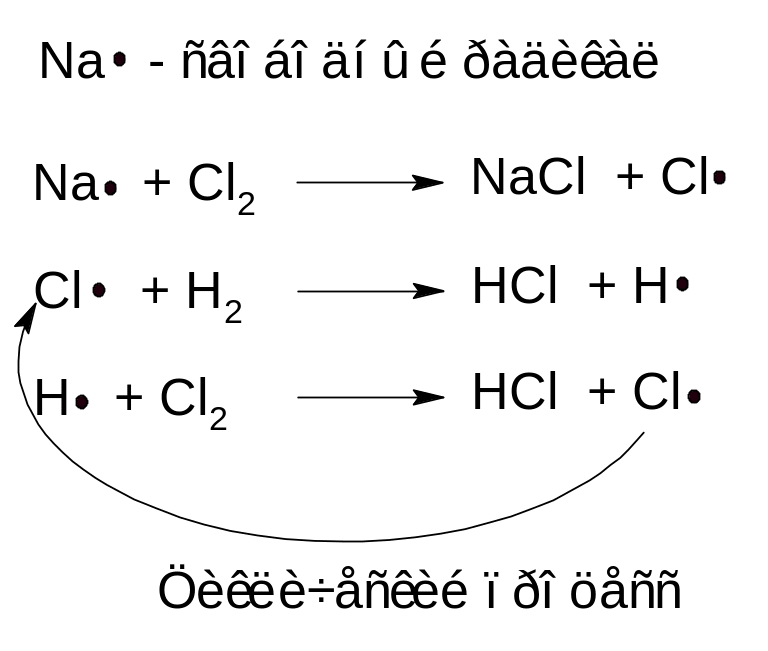

Это - пример так называемой цепной реакции, протекающей по радикально-цепному механизму. При цепном процессе имеет место цепочка реакций, в каждой из которых образуется молекула продукта и одновременно — свободный атом или, в общем случае, радикал, т. е. фрагмент молекулы, имеющий неспаренный электрон. Свободные радикалы химически активны, и время их жизни в химической системе невелико — они быстро реагируют либо с молекулами, либо с другими свободными радикалами. Когда свободный радикал реагирует с другой молекулой исходного вещества, образуется еще одна молекула продукта и новый радикал и т. д. Длина такой цепи может быть очень большой (десятки тысяч элементарных актов взаимодействия). Одновременный обрыв двух цепей происходит тогда, когда два свободных радикала (или свободных атома) сталкиваются друг с другом и реагируют с образованием молекулы (реакция рекомбинации). Для рассмотренной выше цепной реакции между водородом и хлором имеют место следующие элементарные акты обрыва кинетической цепи:
Для того чтобы свободные атомы соединились в молекулу, необходимо присутствие третьей частицы или твердой поверхности, в противном случае образовавшаяся молекула обладала бы запасом энергии, равным тому, который необходим для ее распада; не отдав эту энергию третьей частице или твердой поверхности, она снова распалась бы. Поэтому для цепных реакций характерно влияние на скорость реакции размеров, материала и формы сосуда, в котором протекает реакция. Для этих реакций характерна также чувствительность к следам примесей, прекращающих реакцию за счет обрыва цепей или же, наоборот, вызывающих ее за счет инициирования цепей.
II. По признаку изменения числа исходных и конечных веществ реакции можно выделить такие типы:
1) реакции соединения, при которых из двух или нескольких веществ получают одно вещество:
в общем виде А + В+. . . → С;
2Mg + О2 → 2MgO;
SO2 + Н2О → Н2SО3
2) реакции разложения, при которых из одного вещества образуется несколько веществ:
в общем виде С → А + В. . . ;
t
2HgO → 2Hg + O2;
t
Сu (ОН)2 → СuО + Н2О
3) реакции замещения, при которых простое вещество замещает составную часть сложного вещества и в результате образуются новое простое и новое сложное вещества:
в общем виде АВ + С → АС + В;
Н2SО4 + Zn → ZnSO4 + Н2↑
Fe + CuSO4 → FeSO4 + Cu
4) реакции обмена, при которых молекулы сложных веществ обмениваются своими составными частями:
или в общем виде AB + CD → AD + CB,
HCl + NaOH → NaCl + H2O
BaCl2 +Н2SО4 → BaSO4 ↓ + 2НCl
III. По признаку изменения степеней окисления элементов, которые входят в состав реагирующих веществ, выделяют реакции, идущие без изменения степеней окисления элементов, и на окислительно-восстановительные (идущие с изменением степеней, окисления элементов).
