- •Предмет физики и ее связь с другими науками. Единицы физических величин.
- •Механика, как физическая теория.
- •Кинематика поступательного движения.
- •Кинематика вращательного движения.
- •Динамика поступательного движения.
- •Механический принцип относительности Галилея. Преобразования Галилея. Классический закон сложения скоростей.
- •Основные положения сто. Преобразования Лоренца.
- •Следствия из преобразований Лоренца.
- •Работа сил. Механическая работа. Кинетическая работа.
- •Поле как форма материи. Потенциал и напряженность поля.
- •Потенциальная энергия. Связь потенциальной энергии с силой.
- •Закон сохранения полной энергии. Закон сохранения механической энергии.
- •Закон всемирного тяготения.
- •Вращение абсолютно твердого тела. Уравнение динамики вращательного движения.
- •Момент инерции тела. Момент инерции материальной точки, обруча, диска, шара, стержня. Теорема Штейнера.
- •Импульс тела. Закон сохранения и изменения импульса.
- •Удары тел.
- •Момент импульса. Закон сохранения и изменения момента импульса.
- •Закон Гука. Упругие свойства тел.
- •Колебания. Свободные колебания. Гармонические колебания.
- •Сложение колебаний одного направления.
- •Сложение взаимно перпендикулярных колебаний. Фигуры Лиссажу.
- •Математический маятник.
- •Физический маятник.
- •Пружинный маятник.
- •Затухающие колебания.
- •Вынужденные колебания. Резонанс.
- •Волновые процессы. Уравнение плоской бегущей волны.
- •Продольные и поперечные волны. Скорость распространения волн в среде. Дисперсия волн.
- •Стоячие волны.
- •Звук и его характеристики.
- •Предмет молекулярной физики. Основные положения. Методы исследования.
- •Взаимодействие между молекулами.
- •Идеальный газ. Экспериментальные газовые законы.
- •Уравнения Клапейрона-Менделеева. Основное уравнение мкт.
Взаимодействие между молекулами.
Сильное, или ядерное, взаимодействие обусловливает связь протонов и нейтронов в ядрах атомов и обеспечивает исключительную прочность этих образований, лежащую в основе стабильности вещества в земных условиях.
Электромагнитное взаимодействие характеризуется как взаимодействие, в основе которого лежит связь с электромагнитным полем. Оно характерно для всех элементарных частиц, за исключением нейтрино, антинейтрино и фотона. Электромагнитное взаимодействие, в частности, ответственно за существование атомов и молекул, обусловливая взаимодействие в них положительно заряженных ядер и отрицательно заряженных электронов.
Слабое взаимодействие — наиболее медленное из всех взаимодействий, протекающих в микромире. Оно ответственно за взаимодействие частиц, происходящих с участием нейтрино или антинейтрино (например, (
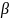 -распад,
-распад,
 -распад),
а также за без нейтринные процессы
распада, характеризующиеся довольно
большим временем жизни распадающейся
частицы (
-распад),
а также за без нейтринные процессы
распада, характеризующиеся довольно
большим временем жизни распадающейся
частицы (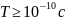 ).
).Гравитационное взаимодействие присуще всем без исключения частицам, однако из-за малости масс элементарных частиц оно пренебрежимо мало и, по-видимому, в процессах микромира несущественно.
Идеальный газ. Экспериментальные газовые законы.
В молекулярно-кинетической теории пользуются идеализированной моделью идеального газа, согласно которой считают, что:
1) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
2) между молекулами газа отсутствуют силы взаимодействия;
3) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
Закон Бойля — Мариотта: для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
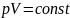
При
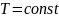 ,
,
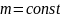 .
.
График
зависимости между параметрами состояния
газа при постоянной температуре
называется изотермой. Изотермы в
координатах
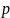 ,
,
 представляют собой гиперболы,
расположенные на графике тем выше, чем
выше температура, при которой происходит
процесс.
представляют собой гиперболы,
расположенные на графике тем выше, чем
выше температура, при которой происходит
процесс.
Законы Гей-Люссака:
1)
объем данной массы газа при постоянном
давлении изменяется линейно с
температурой:
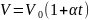
При
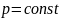 ,
.
,
.
2)
давление данной массы газа при постоянном
объеме изменяется линейно с температурой:
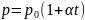
При
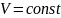 ,
.
,
.
В этих уравнениях — температура по шкале Цельсия,
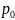 и
и
 — давление и объем при 0°С, коэффициент
— давление и объем при 0°С, коэффициент
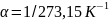 .
.Закон Авогадро: 1 моль любого газа при одинаковых температуре и давлении занимает одинаковый объем. При нормальных условиях этот объем равен
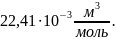
Закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений
 входящих в нее газов:
входящих в нее газов:
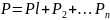
Уравнения Клапейрона-Менделеева. Основное уравнение мкт.
Уравнение Клапейрона-Менделеева:
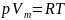
Уравнение Клапейрона—Менделеева для массы газа:

Основное уравнение молекулярно-кинетической теории идеальных газов: