- •«Аналитическая химия и физико-химические методы анализа»
- •Способы проведения аналитических реакций в растворе
- •Лабораторная работа №2. Реакции и анализ первой аналитической группы катионов
- •Реакции и анализ третьей аналитической группы катионов
- •1. Общая характеристика катионов третьей группы
- •3. Опыт 2 . Обнаружение иона
- •1. Предварительные испытания
- •2. Отделение катионов I аналитической группы от II:
- •6. Обнаружение ионов
- •7. Обнаружение иона стронция
- •3. Стандартизация раствора хлороводородной кислоты по тетраборату натрия.
- •4. Определение содержания щёлочи в растворе
- •Контрольные вопросы :
- •Задачи для самостоятельного решения
- •1. Приготовление раствора титранта кМnO4
- •2. Приготовление раствора первичного стандарта
- •3. Стандартизация раствора титранта кМnO4
- •4. Вычисления
- •5) Определение железа (II)
- •Определение концентрации ионов меди в растворе
- •4. Определение меди в исследуемом растворе
3. Опыт 2 . Обнаружение иона
Капельная реакция с бензидином.
Уксуснокислый раствор бензидина С12Н8(NН2)2 окисляется ионами СrO42¯.Г в соединение синего квела. Эта реакция выполняется капельным методом после окисления Сr3+ в СrО42¯ действием перекиси водорода в щелочной' среде.
Выполнение реакции:
К 2-3 каплям соли хрома (III) прибавить раствор концентрированной щёлочи Na0H до перехода выпавшего осадка Сг(ОН)з в раствор зелёного цвета, 3-4 капли перекиси водорода и нагреть, пока окраска из зелёной не станет жёлтой (если окраска не меняется, тогда добавить ещё перекиси водор
2 СrСl3 + 10 NаОН + ЗН202 2Na2Сr04 + 8Н20 +6NaCl
жёлтый
2 Сr3+ + 10ОН¯ + ЗН202 2СrO42¯ + 8Н20
Затем на полоску фильтровальной бумаги нанести каплю полученного раствора хромата и каплю бензидина. Пялно синеет. Рассматриваемую реакцию можно использовать для дробного открытия ионов Сr3+ в присутствии других катионов. Реакции мешают ионы Со3+ и Мn4+.
Контрольные вопросы :
1.Написать реакции взаимодействия избытка щёлочи и перекиси водорода с катионами Ш группы.
2. Написать реакции взаимодействия избытка раствора аммиака с катионами III группы
3. Отличается ли действие небольшого количества сильной щёлочи от действия раствора аммиака на ион цинка? Написать уравнения реакций.
4. Отличается ли действие избытка щёлочи от Действия раствора аммиака на раствор соли цинка? Написать уравнения реакций.
5. Почему при добавлении раствора соды к соли CrCl3 выпадает серо-зелёный осадок гидроксида хрома? Написать уравнение реакции
6. Почему при добавлении раствора соды к соли ZnSO4, выпадает осадок основного карбоната (ZnОН)2СОз? Написать уравнение реакции
Лабоаторная работа №5
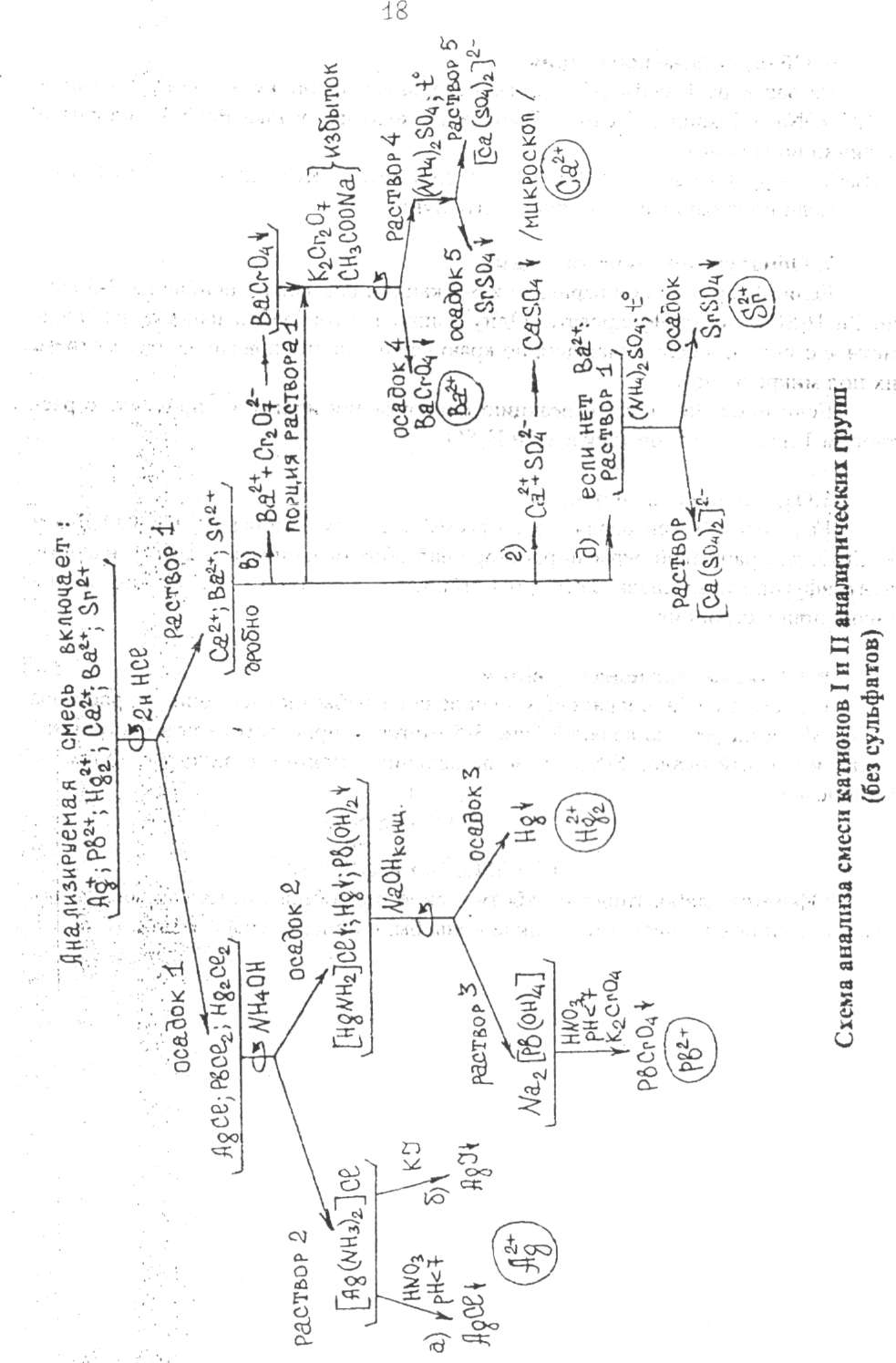
АНАЛИЗ СМЕСИ КАТИОНОВ I и II ГРУПП
Содержание работы
Целью работы является анализ раствора , содержащий смесь катионов первой и второй аналитических групп и проведение реакций обнаружения этих ионов. Совершенствование умений и навыков проведения аналитических реакци
Ход работы
1. Предварительные испытания
Прежде , чем приступить к открытию катионов в растворе прежде всего обращают внимание на окраску раствора и определяют рН раствора:
- если в результате определения pН исследуемой смеси среда кислая, то в растворе могут присутствовать ионы Hg22+, если среда почти нейтральная, то ионов Pb2+ и Hg22+ может не быть в смеси;
- если среда нейтральная или кислая, а полученная задача без осадка то, следовательно,в раствора нет хлоридов и сульфатов (см.схему).