
- •Лекция 16 углеводы
- •1. Моносахариды
- •1.1. Классификация, номенклатура, изомерия.
- •1.2. Строение моносахаридов. Строение моноз
- •Гликозидный гидроксил α-формы всегда находится в транс-положении к гидроксиметильной группе.
- •1.3. Получение моносахаридов.
- •1.4. Свойства моносахаридов.
- •2. Дисахариды
- •2.1. Классификация
- •2.2 Восстанавливающие дисахариды
- •2.3. Невосстанавливающие дисахариды
- •3. Полисахариды
- •3.1. Классификация
- •3.2. Крахмал
- •3.3. Целлюлоза
Гликозидный гидроксил α-формы всегда находится в транс-положении к гидроксиметильной группе.
1.3. Получение моносахаридов.
Моносахариды обычно получают из природного сырья.
1. Гидролизом ди- и полисахаридов под влиянием кислот или ферментов:
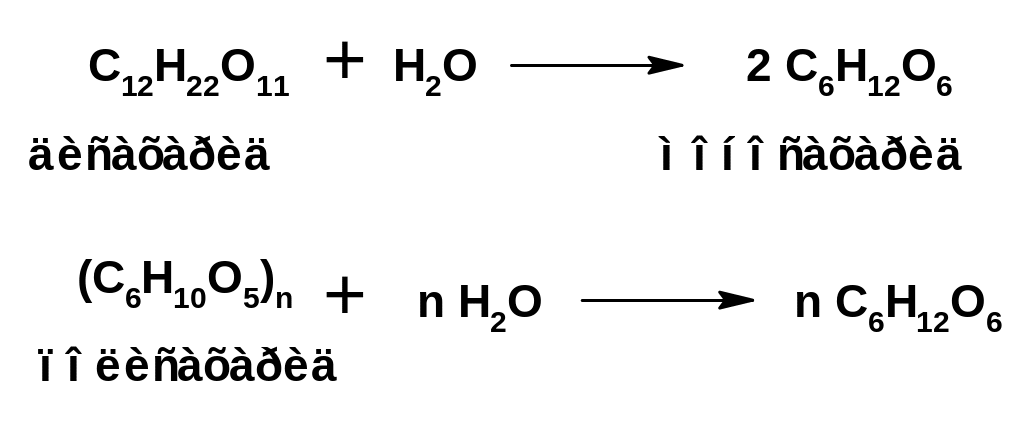
2. Окислением многоатомных спиртов обычными окислителями или под влиянием ферментов. При обычном окислении образуется смесь моноз:
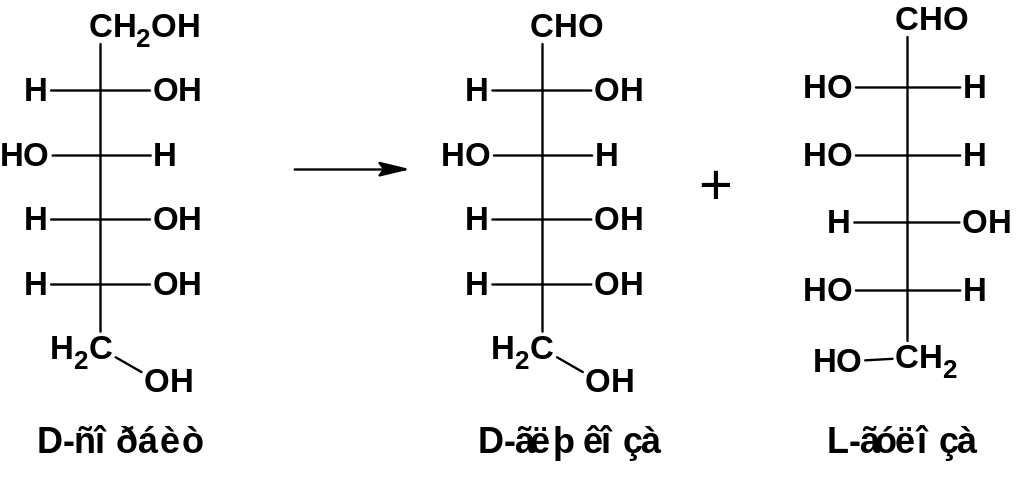
При энзиматическом окислении можно окислить определенную группу:
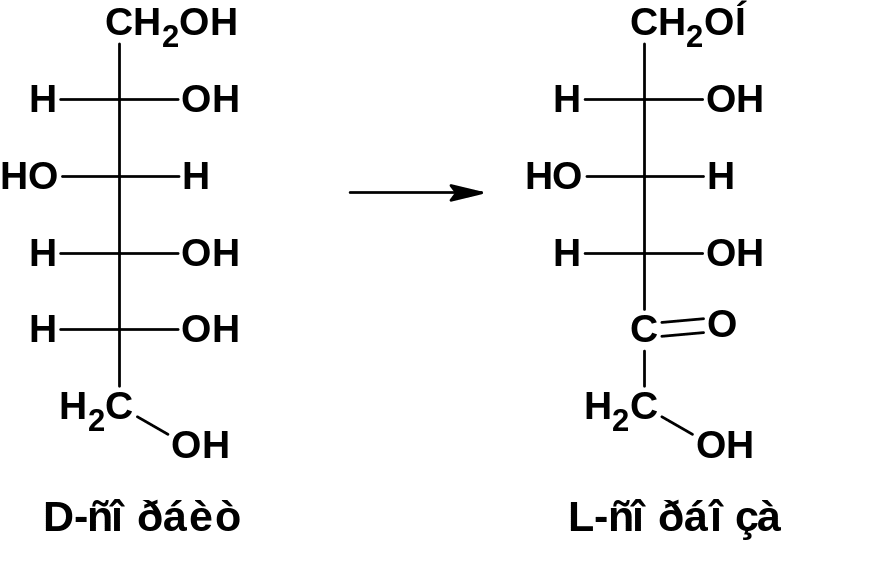
3. Оксинитрильный синтез.
1.4. Свойства моносахаридов.
Моносахариды – кристаллические вещества, хорошо растворимые в воде, больше частью сладкие на вкус. Как правило, оптически активны.
Моносахариды проявляют свойства спиртов, карбонильных соединений и полуацеталей.
Восстановление
При восстановлении сахаров образуются многоатомные спирты:
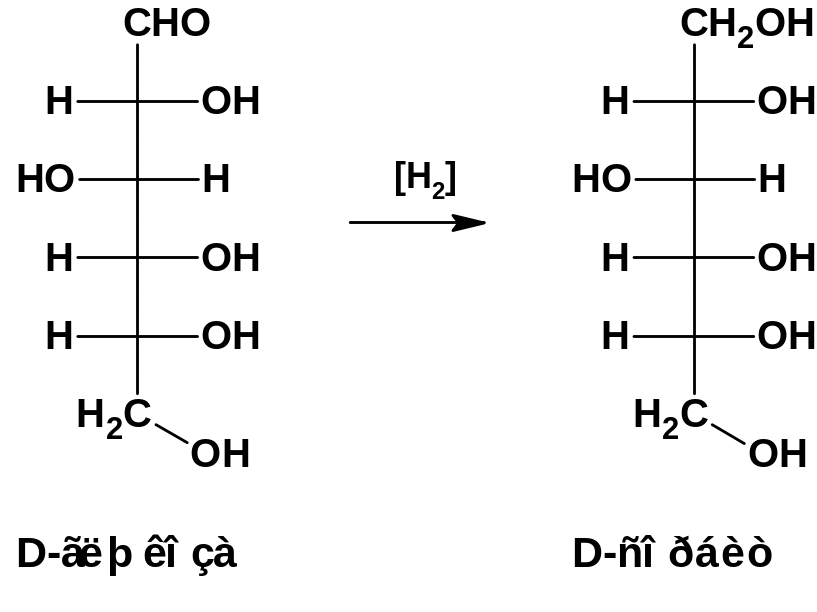
Окисление
При окислении сахаров мягко действующими реагентами. Например, бромной водой – образуются альдоновые кислоты:
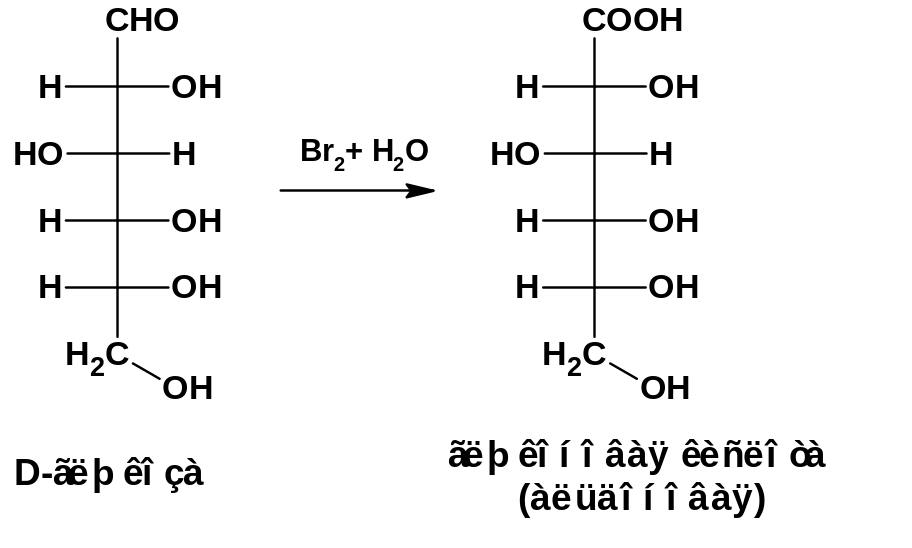
При окислении более жестким окислителем, например, азотной кислотой, образуются сахарные (альдаровая )кислоты:
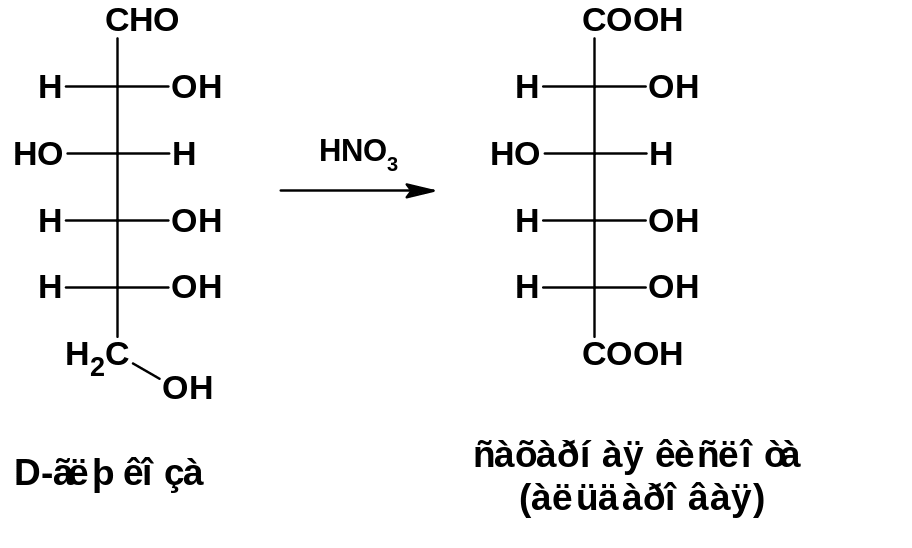
Оксинитрильный синтез
Оксинитрильный синтез является методом получения высших моноз из низших.
При присоединении синильной кислоты к альдегидной группе гексозы образуются два диастереомерные гидроксинитрилы, отличающиеся конфигурацией первого тетраэдра:
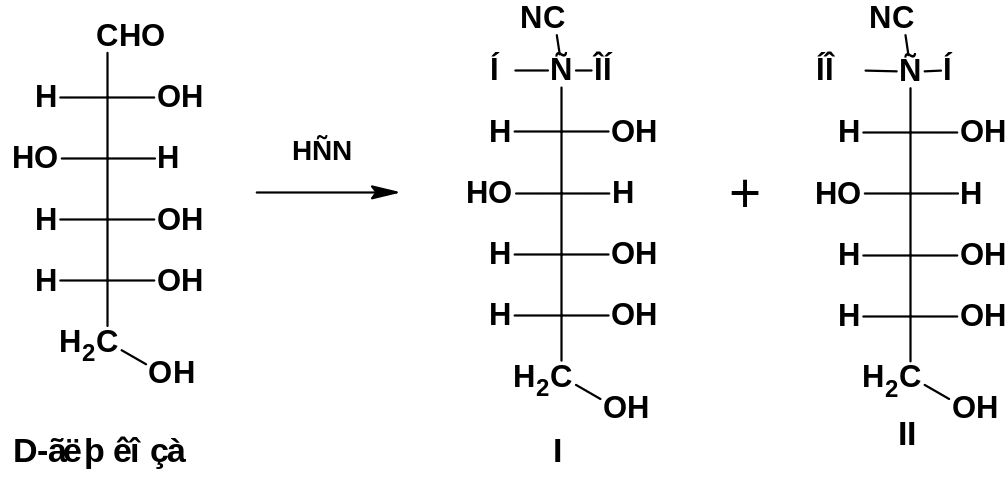
Гидроксинитрил (I) последующим омылением, образованием лактона и восстановлением последнего – превращается в альдогептозу:

Реакция с гидроксиламином
Реакцией с гидроксиламином переходят от более высших моноз - к низшим. Сахара легко образуют оксимы. Дегидратацией оксимов получают гидроксинитрилы, от которых отщепляют синильную кислоту влажной окисью серебра, при этом образуется гидроксиальдегид с числом углеродных атомов на один меньше, чем в исходном сахариде:
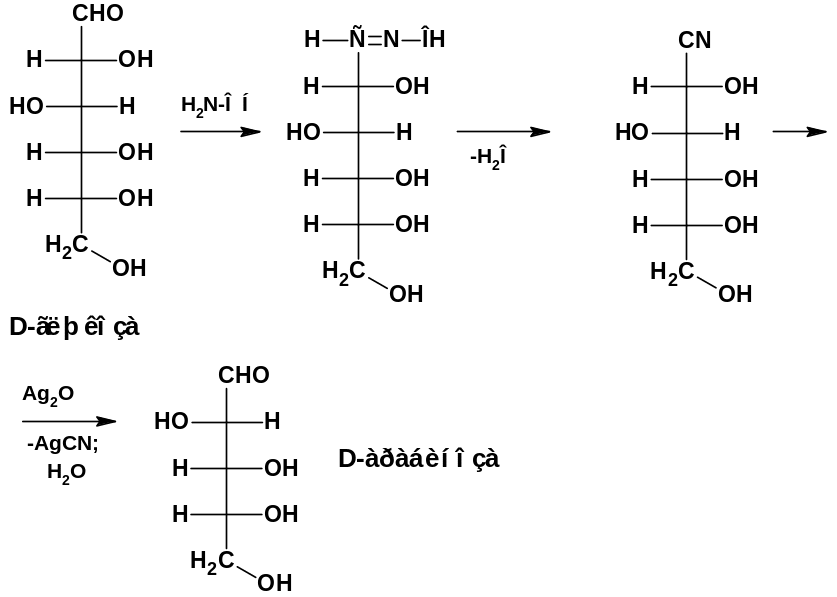
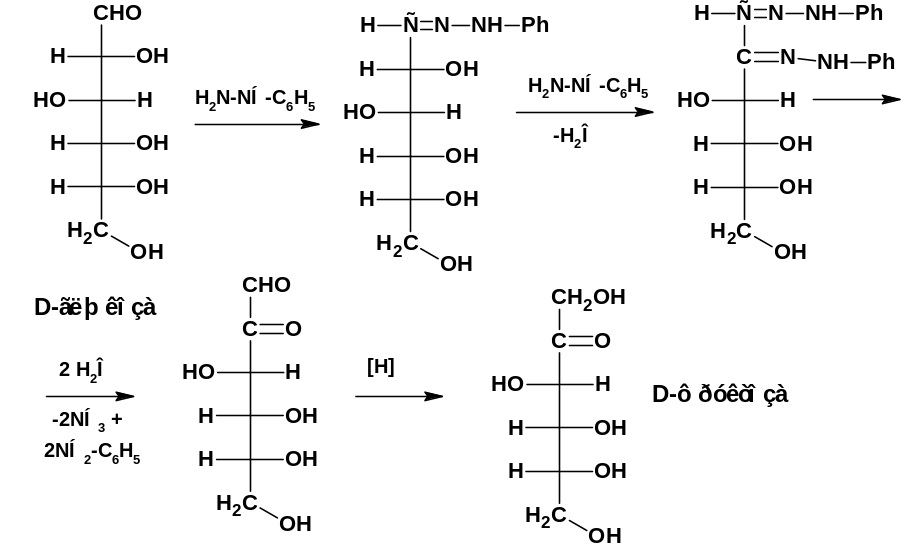
Реакция с фенилгидразином
По реакции с фенилгидразином можно перейти от альдозы к кетозе:
Действие щелочей
Под действием щелочей монозы претерпевают изомеризацию и образуется смесь сахаров, отличающихся строением и конфигурацией первого и второго тетраэдров. Так из глюкозы, маннозы и фруктозы образуется рановесная смесь трех сахаров:
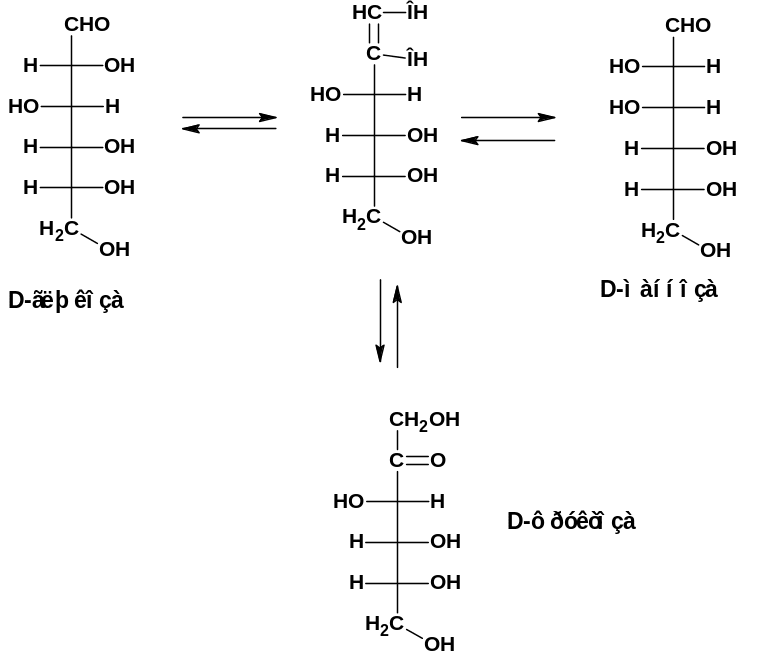
Причиной изомеризации является образование енола под действием щелочи. Строение енола одинаковое для всех трех моноз.
Реакция алкилирования
При алкилировании сахара реагируют в циклической полуацетальной форме.
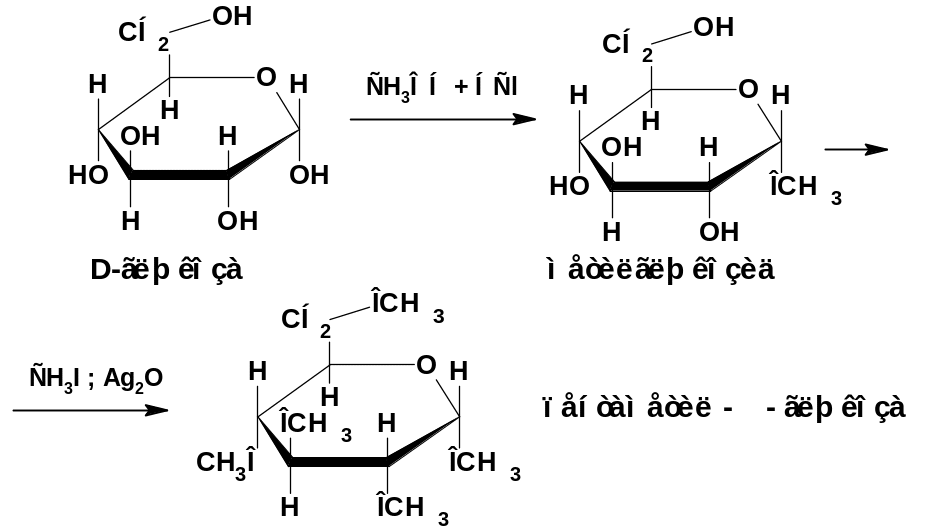
Реакция ацетилирования
При действии на глюкозу уксусного ангидрида получается пентаацетилглюкоза:
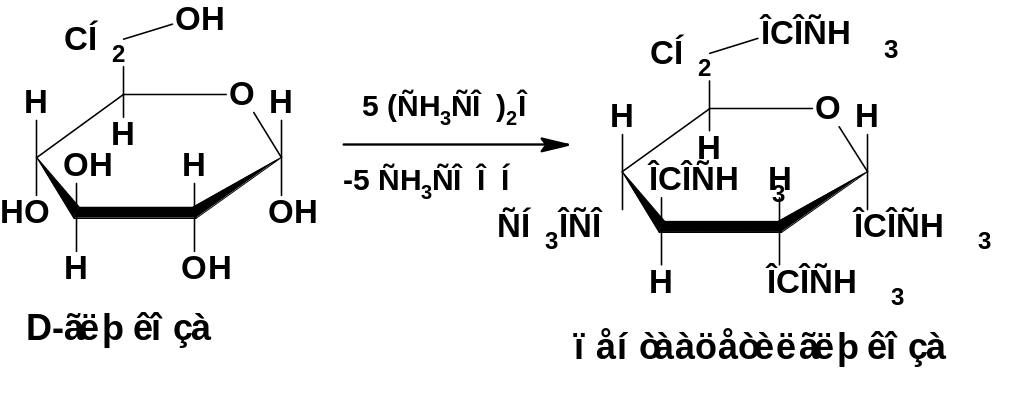
Дегидратация с циклизацией
При нагревании пентоз и гексоз с разбавленной серной кислотой - пентозы образуют фурфурол, а гексозы образуют α-гидроксиметилфурфурол:
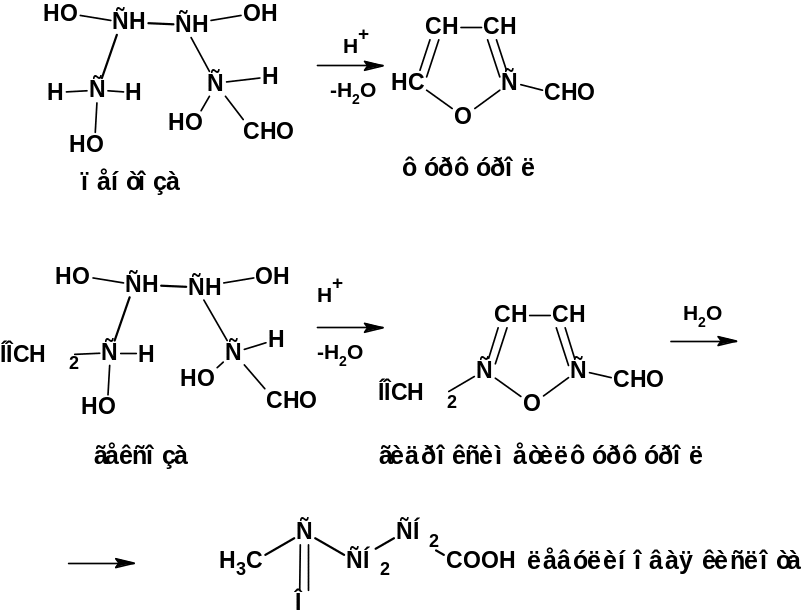
α-гидроксиметилфурфурол легко гидролизуется с образованием левулиновой кислоты. Таким путем можно различить пентозы и гексозы.
Брожение сахаров
Брожением называется расщепление молекул сахаров с выделением углекислого газа под влиянием ферментов (энзимов). Под влиянием фермента зимазы (дрожжи) происходит самое распространенное спиртовое брожение:
![]()
При ацетоно-бутаноловом брожении образуются ацетон и бутиловый спирт. Известны лимоннокислое брожение, маслянокислое и другие виды брожения.
