
- •Общие Методические указания
- •Варианты индивидуальных заданий
- •1.Эквивалент. Эквивалентная масса. Закон эквивалентов
- •2. Строение атома. Электронные конфигурации атомов элементов
- •1S2 2s2 2p6 3s2 3p3 сокращенно [Ne]3s23p3
- •3. Термохимия
- •4. Кинетика
- •5. Растворы
- •6. Жесткость воды
- •7. Гидролиз солей
- •8. Комплексные соединения
- •9. Окислительно-восстановительные реакции
- •10. Гальванические элементы
- •11. Электролиз
- •12. Коррозия металлов
- •13. Общие свойства металлов
- •14. Полимерные материалы (сэ, эа, кс выполнять не надо)
- •Приложение
8. Комплексные соединения
Типовая задача
Написать уравнение диссоциации комплексной соли и ее комплексного иона Na2[Zn(OH)4]. Укажите структурные элементы молекулы соли. Назовите соль согласно номенклатуре комплексных соединений и укажите численное значение координационного числа комплексообразователя. Напишите выражение для константы нестойкости данного комплексного иона.
Решение. 1. Записываем уравнение диссоциации комплексной соли:
Na2[Zn(OH)4] ↔ 2Na+ + [Zn(OH)4]2-
и уравнение диссоциации комплексного иона (аниона):
[Zn(OH)4] 2- ↔ Zn2+ + 4OH-
2. Указываем структурные элементы молекулы:
Na+ - внешняя координационная сфера
[Zn(OH)4]2- - внутренняя координационная сфера (комплексный ион)
Zn2+ - комплексообразователь
OH- - лиганды
3. Даем название соли.
В соответствии с номенклатурой комплексных соединений, сначала называют в именительном падеже анион соли, а затем – катион в родительном падеже (натрия). Название комплексного аниона начинают с указания числа (тетра-) и названия (гидроксо-) отрицательно заряженных лигандов; последним называют комплексообразователь.
тетрагидроксоцинкат натрия
Координационное число комплексообразователя (число лигандов) – 4.
Диссоциация комплексного иона характеризуется константой равновесия, называемой константой нестойкости комплексного иона:
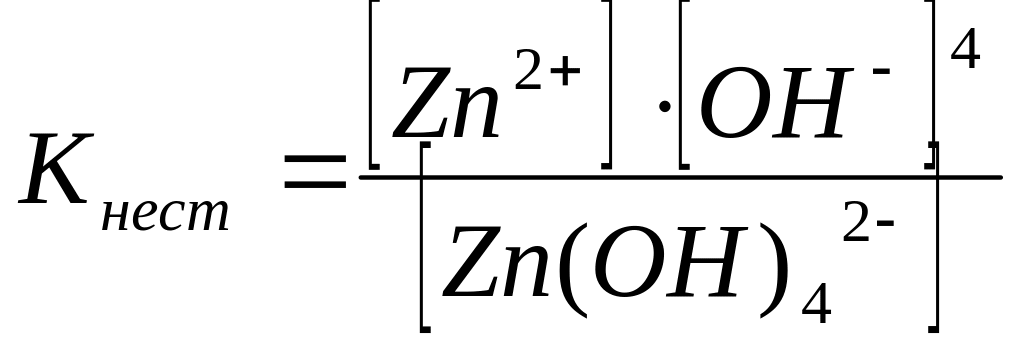
Варианты заданий
Таблица 8
№ п/п |
Комплексные соединения |
|
1 |
2 |
3 |
|
|
Na[AuCl4] |
[Cr(H2O) (NH3)5]Br3 |
|
|
[Zn(NH3)4](OH)2 |
K[FeCl6] |
|
|
[Al(H2O)6]Cl3 |
K4[Pt(CN)4Cl2] |
|
|
Na3[CoCl6] |
[Co(NH3)3(H2O)2Br]Cl2 |
|
|
[Ni(NH3)4]SO4 |
K[Ag(NO2)2] |
|
|
Na3[Al(OH)6] |
[Pt(NH3)5Cl]Cl3 |
|
|
[Cu(NH3)4] SO4 |
Na3[Co(CN)6] |
|
|
Na2[Sn(OH)4] |
[Cr(NH3)4(H2O)Cl]Br2 |
|
|
[Al(H2O)6]Cl3 |
K3[Fe(CN)6] |
|
|
[Ni(NH3)4](OH)2 |
K3[Co(CN)6] |
|
|
K[Pt(NH3)Cl5] |
[Co(H2O)2(NH3)3Cl]Br2 |
|
|
H2[PtCl6] |
[Pt(H2O)2(NH3)5Cl]Cl3 |
|
|
K3[Fe(CN)6] |
[Cr(NH3)5Cl]Br2 |
|
|
[Cr(NH3)4(H2O)2]Cl3 |
Na[Fe(CN)6] |
|
|
K[PtCl5(NH3)] |
[Co(H2O)4(NH3)2]Cl3 |
|
|
Na3[Ir(CN)6] |
[Pt(NH3)4Br2]Cl2 |
|
|
K2[SiF6] |
[Co(H2O)2(NH3)2Cl2]Br |
|
|
[Pt(NH3)4Br2]Br2 |
Na3[Co(CN)6] |
|
|
K3[Co(CN)6] |
[Cu(H2O)2(NH3)2]Cl2 |
|
|
[Ag(NH3)2]Cl |
K[PtCl5(NH3)] |
|
|
K3[Co(CN)6] |
[Zn(NH3)4] SO4 |
|
|
[Cu(NH3)4]Cl2 |
H2[SiF6] |
|
|
K[AuBr4] |
[Cr(H2O)4(NH3)Cl]Br2 |
|
|
Ba[Cu(SCN)(CN)3] |
[Cr(H2O)3(NH3)2Cl] SO4 |
|
|
K2[Cd(CN)4] |
[Cr(H2O)6]Br3 |
|
|
Na3[Co(CN)4Cl2] |
[Cd(NH3)4](OH)2 |
|
|
[Co(H2O)4(NH3)Cl]Cl2 |
K4[Co(CN)6] |
|
|
H2[PtCl6] |
[Cr(NH3)5Cl]Br2 |
|
|
K3[Co(CN)4Cl2] |
[Pt(NH3)5Cl]Cl3 |
|
|
H2[PtCl4] |
[Co(NH3)3(H2O)3]Cl3 |
