
2. Предмет физической химии
Физическая химия как самостоятельная наука занимается главным образом рассмотрением двух групп вопросов:
1) изучением свойств и строения различных веществ (а также частиц, их которых они состоят) в зависимости от их химического состава и условий существования;
2) изучением химических реакций и других форм взаимодействия между веществами (частицами, из которых они состоят) в зависимости от их химического состава и строения, условий протекания процессов и интенсивности внешних воздействий.
Курс физической химии включает ряд разделов, определяющих ее предмет.
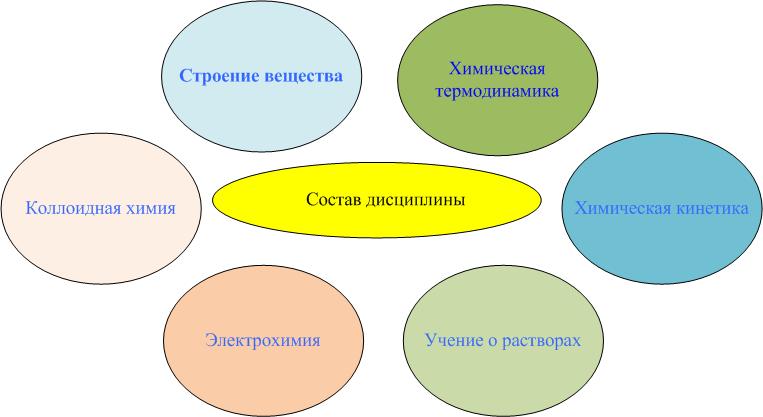
Важнейшими из них, а также перечень рассматриваемых в них вопросов, следующие.
Строение вещества: учение о строении атомов и молекул, учение об агрегатном строении вещества.
Химическая термодинамика базируется на двух основных законах термодинамики. На основе первого определяются тепловые балансы химических реакций, проводятся расчеты по количеству теплоты, поглощаемой или выделяемой при протекании химических реакций.
На основе второго закона определяется возможность самопроизвольного течения процесса в интересующем направлении; условия равновесия и его смещения под влиянием изменяющихся внешних факторов.
Учение о растворах рассматривает природу растворов, их внутреннюю структуру и свойства, зависимость свойств растворов от их концентрации и химической природы компонентов.
Электрохимия изучает некоторые особенности свойств растворов электролитов.
Химическая кинетика изучает скорость и молекулярный механизм химических реакций в гомо- и гетерогенных средах.
В отдельные самостоятельные группы вопросов физической химии выделяются изучение поверхностных явлений и свойств дисперсных и коллоидных систем.
3. Основы химической термодинамики
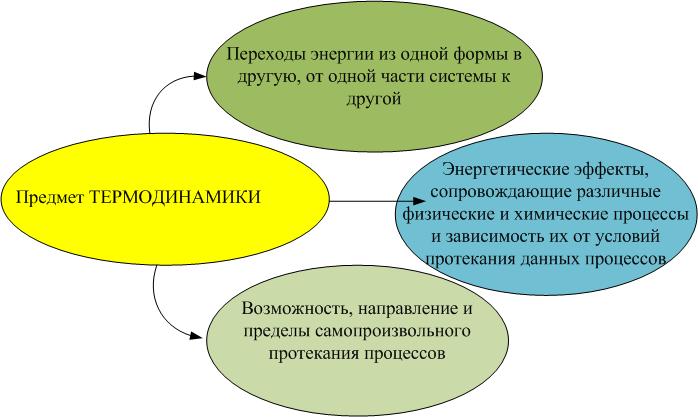
Термодинамика представляет собой научную дисциплину, которая изучает:
переходы энергии из одной формы в другую; от одной части системы к другой;
энергетические эффекты, сопровождающие различные фазовые и химические процессы, зависимость их от условий протекания;
возможность, направление и пределы самопроизвольного течения процессов в рассматриваемых условиях.
ОГРАНИЧЕНИЯ В ТЕРМОДИНАМИКЕ

4. Основные понятия термодинамики
СИСТЕМА – тело или группа тел, физически или мысленно обособленные от окружающей среды
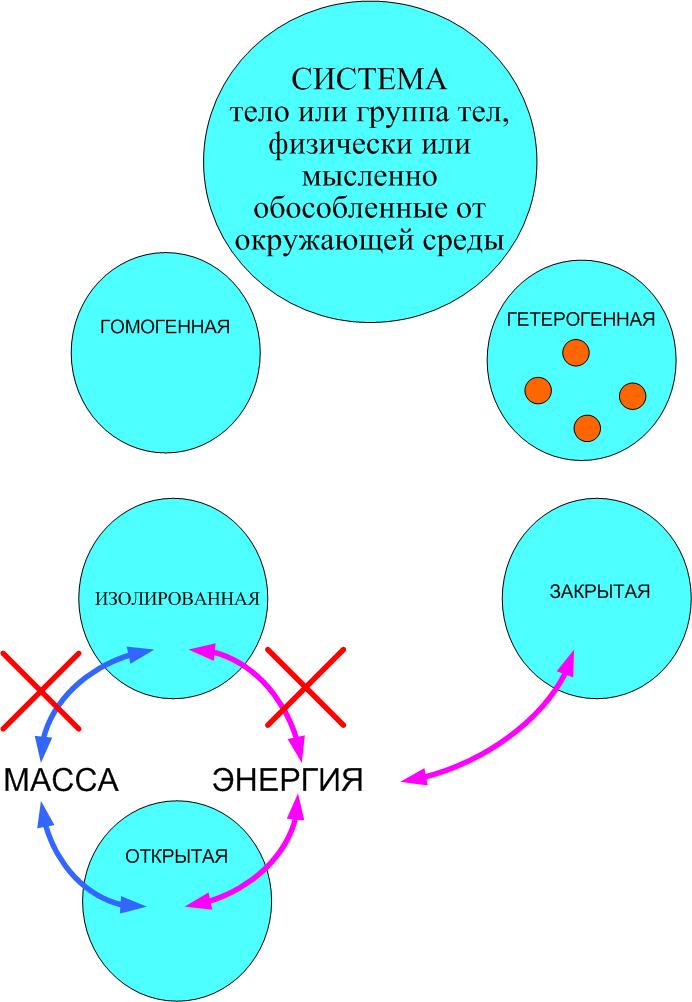
ГОМОГЕННАЯ СИСТЕМА – система, внутри которой нет поверхностей раздела фаз.
ГЕТЕРОГЕННАЯ СИСТЕМА – система, внутри которой существуют разделы фаз.
ИЗОЛИРОВАННАЯ СИСТЕМА – система, не обменивающаяся с окружающей средой веществом и энергией
ЗАКРЫТАЯ СИСТЕМА – система, которая может обмениваться с окружающей средой только энергией и не может сохранять постоянный объем
ОТКРЫТАЯ СИСТЕМА – cистема, которая может обмениваться с окружающей средой как энергией, так и веществом
ФАЗА – гомогенная часть системы, обладающая одинаковыми физико-химическими свойствами и ограниченная от других фаз системы поверхностью раздела
Характеристикой фазы является возможность ее механического выделения из системы.
Фазы бывают чистыми, то есть состоящими из одного вещества (например, кристалл поваренной соли NaCl), и смешанными-состоящими из смеси веществ (например, атмосферный воздух – смесь газов и водяного пара).
Совокупность всех физических и химических свойств системы характеризует ее состояние.
Изменение каких-либо из свойств обязательно приводит к изменению состояния.
ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ СОСТОЯНИЯ – любая из величин, определяющая состояние системы (температура системы, давление в системе, объем системы, внутренняя энергия системы, энтальпия системы, концентрация компонентов системы и др.)
ТЕРМОДИНАМИЧЕСКИЙ ПРОЦЕСС – всякое изменение, происходящее в системе и связанное хотя бы с изменением одного термодинамического параметра состояния.
ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ ПРОЦЕССА – любая из величин, служащая для характеристики процесса (изменение внутренней энергии, тепловой эффект реакции, теплота кристаллизации и т.п.)
Конечное
изменение параметра состояния [![]() ]
в процессе (например, изменение давления
газа при его расширении) будет обозначаться
в курсе лекций через
]
в процессе (например, изменение давления
газа при его расширении) будет обозначаться
в курсе лекций через
![]() ,
а конечное малое изменение – через
,
а конечное малое изменение – через
![]() или
или
![]() в частных производных.
в частных производных.
ТЕРМОДИНАМИЧЕСКАЯ ФУНКЦИЯ СОСТОЯНИЯ – функция, которая зависит только от состояния системы, а не от пути перехода из одного состояния в другое. Для термодинамической функции
![]()
где X2 и Х1 – значения параметров в начале и при окончании процесса.
