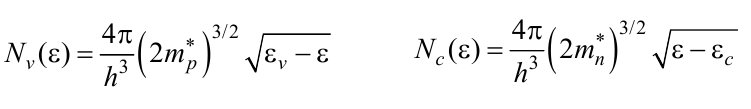Материалы, применяемые в электронике делятся на активные и пассивные.




По магнитным свойствам материалы делятся на диамагнетики (магнитная проницаемость µ < 1, но µ ≈ 1), парамагнитные (µ > 1, но µ ≈ 1), ферромагнитные (µ >> 1), ферримагнитные (µ >> 1).
По агрегатному состоянию материалы делят на твердые, жидкие, газообразные. По структуре на монокристаллические, поликристаллические, аморфные и смешанные.
Связь между атомами бывает ионной, ковалентной (атомной), металлической, молекулярной.
Согласно современным представлениям атомы имеют центральное ядро, состоящее из незаряженных нейтронов и положительно заряженных протонов, окруженное облаком отрицательно заряженных электронов. Атом электрически нейтрален, поскольку суммарный заряд электронов равен положительному заряду протонов.
Полная внутренняя энергия атома ε равна сумме кинетических энергий W всех электронов и потенциальных энергий U притяжения их ядром:

где r - расстояние электрона от ядра.
Если ε = W + U < 0, то движение электрона является связанным, оно ограничено в пространстве значением
r
=
 .
.
При ε > 0 движение электрона является свободным, и он может уйти на бесконечно большое расстояние от ядра.
Полная внутренняя энергия может принимать лишь одно из значений дискретного ряда: ε1, ε2, ε 3... (ε1 < ε2 < ε3...).
Энергия атома может изменяться только скачкообразно путем квантового перехода из одного стационарного состояния εi в другое состояние εj.
Согласно принципу Паули в каждом из возможных квантовых состояний может находиться не более одного электрона. Распределение электронов по энергетическим уровням в многоэлектронных атомах происходит в соответствии с двумя основными принципами:
1) атомная система устойчива, когда ее внутренняя энергия минимальна;
2) каждый электрон в атоме находится в своем квантовом состоянии, ха-
рактеризующимся четырьмя квантовыми числами n, l, m, s.
Главное квантовое число n определяет радиус круговой орбиты или большую полуось эллиптической. Оно может принимать значения n = 1, 2, 3 и т.д. Чем больше n, тем больше радиус орбиты и энергия электрона. Состояния электрона, определяемые главным квантовым числом, называют энергетическими уровнями.
Орбитальное квантовое число l определяет малую полуось эллиптической орбиты. Оно может принимать значения l = 0, 1, 2, …, (n–1). Значение l = 0 соответствует круговой орбите. Энергетические состояния, характеризующиеся различными значениями l, называют подуровнями.
Магнитное квантовое число m определяет пространственную ориентацию эллиптической орбиты. Оно может принимать значения m =0, ±1, ±2,..., ±l. Каждому квантовому числу l соответствует (2l+1) по-разному ориентированных орбит.
Спиновое квантовое число s определяет момент количества движения электрона вокруг собственной оси. Вектор момента количества движения может быть параллелен или антипараллелен вектору орбитального момента. Спин электрона равен половине постоянной Планка, поэтому он равен ± Ѕ.
Виды химической связи
Ионная связь или электровалентная связь
Ковалентная связь – гомеополярная связь
Металлическая связь – разновидность гомеополярной связи
Молекулярная связь
По характеру химических связей кристаллы делятся на четыре основные группы:
1) ионные кристаллы (например, NaCl);
2) ковалентные (например, алмаз, кремний);
3) металлические (металлы и полиметаллы);
4) молекулярные кристаллы (например, нафталин)
Точечные или нульмерные дефекты – это дефекты с размерами, сравнимыми с размерами атома. К точечным дефектам относятся примесные атомы внедрения и замещения, межузельные атомы и вакансии, а также центры окраски.
Все точечные дефекты являются центрами механических напряжений в кристаллах вследствие некоторых смещений ионов
К линейным или одномерным дефектам относятся цепочки точечных дефектов, дислокации и дисклинации. Дислокации – это дефекты кристаллической решетки, искажающие правильное расположение плоскостей атомов.
Поверхностными или двумерными дефектами являются дефекты упаковки атомов в кристаллической структуре, границы зерен, сама поверхность кристалла.
Динамика кристаллической решетки Частицы, составляющие кристалл (атомы, ионы, молекулы), под действием внешних сил или в результате теплового движения могут смещаться относительно своих равновесных положений в узлах кристаллической решетки.
В сложной кристаллической решетке, когда число атомов в элементарной ячейке больше 1, кроме акустических мод существует также (3N-3) колебательных мод, называемых оптическими колебаниями. Оптические моды характеризуются индивидуальным колебанием атомов, каждое из которых имеет независящую от других фазу колебаний. В отличие от акустических колебаний частоты оптических колебаний отличны от 0 даже при q = 0
При квантовом описании малых колебаний атомов кристалла, каждомунормальному колебанию с волновым вектором q можно сопоставить квазичастицу с квазиимпульсом P = hq и энергией ε = hω . Эти квазичастицы получили название фононов и являются элементарными возбуждения (квантами) поля упругих колебаний кристалла.
Энергетические зоны в кристаллах
В изолированном атоме электроны способны занимать лишь дискретные энергетические уровни, определяемые силами притяжения к ядру и силами от талкивания от других электронов. В твердом теле атомы расположены настолько близко друг к другу, что между ними возникают новые силы взаимодействия – это силы отталкивания между ядрами и между электронами соседних атомов и силы притяжения между всеми ядрами и всеми электронами. Под действием этих сил энергетические состояния в атомах изменяются: энергия одних электронов увеличивается, других – уменьшается. Разрешенные зоны отделены друг от друга запрещенными зонами, в которых отсутствуют разрешенные уровни. Ширина разрешенных зон по мере перемещения вверх по энергетической шкале возрастает, а ширина запрещенных зон соответственно уменьшается. Во многих случаях может иметь место перекрытие разрешенных энергетических зон
С точки зрения зонной теории все твердые тела можно подразделить на две основные группы: материалы, у которых валентная зона перекрывается зоной проводимости, и материалы, у которых валентная зона и зона проводимости разделены запрещенной зоной.
Металлами называются вещества, обладающие высокими электропроводностью, теплопроводностью, прочностью, а также характерным блеском
Металлы по сравнению с диэлектриками более мягкие (пластичные), потому что один слой кристалла легко скользит над другим. Скольжение слоев возникает не сразу, а последовательно от атома к атому. Свойства металлов обусловлены строением их кристаллической решетки.
Существуют три типа структурных твердых растворов:
растворы замещения, когда атомы растворенного металла замещают в узлах кристаллической решетки атомы металла-растворителя, распределяясь среди них по определенному закону;
растворы внедрения, когда атомы растворенного металла не замещают атомы металла растворителя, а располагаются в межатомных промежутках его кристаллической решетки;
твердые растворы вычитания, которые образуются при недостатке од-ного из компонентов сплава.
Два металла могут образовывать между собой не одно, а несколько соединений, например, NaSn3, NaSn2, NaSn, Na4Sn3, Na2Sn, Na4Sn и др.
Характеристика полупроводников
Полупроводники – наиболее распространенная в природе группа веществ.К ним относят химические элементы: бор (В), углерод (С), кремний (Si), фосфор (Р), сера (S), германий (Ge), мышьяк (As), селен (Se), олово (Sn), сурьма (Sb), теллур (Те), йод (I); химические соединения типа АI ВVII, АIII ВV, АIV ВIV, AI BVI, AII BVI (GaAs, GeSi, CuO, PbS, InSb и другие);
Зонная структура полупроводников
Вещества, в которых при температуре абсолютного нуля верхняя из заполняемых электронами энергетических зон (валентная зона) и нижняя из незаполняемых энергетических зон (зона проводимости) не перекрываются, составляют классы полупроводников и диэлектриков.
Примесные полупроводники
Полупроводники, кристаллическая решетка которых помимо четырехвалентных атомов содержит атомы с валентностью, отличающейся от валентности основных атомов, называют примесными.
В электронном полупроводнике из-за наличия пятивалентных примесных атомов в пределах запрещенной зоны вблизи дна зоны проводимости появляются примесные уровни Ed.
В дырочном полупроводнике за счет введения трехвалентных примесных атомов в пределах запрещенной зоны появляется примесный уровень Ea , который заполняется электронами, переходящими на него из валентной зоны. Примесные атомы называют акцепторами.
Концентрация носителей заряда в примесных полупроводниках.