

Курганская область, Петуховский район, МОУ «Новогеоргиевская СОШ»
Составила :
учитель биологии и химии первой квалификационной категории Яковлева Лариса Александровна
19 Июнь, 2019 |
Яковлева Л.А. |
1 |

|
|
Периодическая система химических элементов Д.И. Менделеева |
|
|
|
|||||||||||||||||||
Пери – |
|
|
|
|
|
|
Группы элементов |
|
|
|
|
|
||||||||||||
|
оды |
|
I |
II |
III |
IV |
V |
VI |
VII |
|
VIII |
|
|
|
||||||||||
1 |
Н |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Не |
|
2 |
|
1,00797 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4.0026 |
||||
Водород |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Гелий |
|||||
2 |
Li |
3 |
Ве |
4 |
В |
5 |
С |
6 |
N |
|
7 |
О |
|
8 |
F |
|
9 |
|
|
Nе |
|
10 |
||
6.939 |
9,0122 |
10,811 |
|
12,01115 |
|
14,0067 |
|
15,9994 |
|
18,9984 |
|
|
|
20,183 |
||||||||||
Литий |
Бериллий |
Бор |
|
Углерод |
Азот |
|
Кислород |
Фтор |
|
|
|
Неон |
|
|||||||||||
|
|
Na |
11 |
|
12 |
Al |
13 |
Si |
|
14 |
P |
|
15 |
S |
|
17 |
Cl |
|
17 |
|
|
Ar |
|
18 |
3 |
22,9898 |
Мg24,312 |
26,9815 |
|
28,086 |
|
30,9738 |
|
32,064 |
|
35,453 |
|
|
|
39,948 |
|||||||||
Натрий |
Магний |
Алюминий |
Кремний |
Фосфор |
Сера |
|
Хлор |
|
|
|
Аргон |
|||||||||||||
|
|
К |
19 |
Сa |
20 |
21 |
Sc |
22 |
|
Ti |
23 |
|
V |
24 |
|
Cr |
25 |
|
|
26 |
27 |
28 |
Ni |
|
|
|
39,102 |
40,08 |
44,956 |
47,90 |
|
50,942 |
|
51,996 |
|
44,956Мn |
55,847Fe |
58,933Со |
58,71 |
||||||||||
4 |
Калий |
Кальций |
Скандий |
Титан |
Ванадий |
Хром |
|
Марганец |
Железо |
2Кобальт |
Никель |
|||||||||||||
29 |
|
30 |
|
|
31 |
|
32 |
|
|
33 |
|
|
34 |
|
|
35 |
|
|
Кr |
|
36 |
|||
|
|
63,546Сu |
65,37 |
Zn |
Ga |
Ge |
As |
|
Se |
|
Br |
|
|
|
|
|||||||||
|
|
26,9815 |
72,59 |
|
74,9216 |
|
78,96 |
|
79,904 |
|
|
|
83,80 |
|||||||||||
|
|
Медь |
Цинк |
Галлий |
Германий |
Мышьяк |
Селен |
Бром |
|
|
|
Криптон |
||||||||||||
|
|
Rb |
85,4737 |
Sr |
87,6238 |
3988,905 |
Y |
91,2240 |
Zr |
92,90641 |
Nb |
95,9442 |
Мо |
[4399] |
Тс |
44101,07Ru |
102,9045 Rh |
106,446 |
Pd |
|||||
5 |
Рубидий |
Стронций |
Иттрий |
Цирконий |
Ниобий |
Молибден |
Технеций |
Рутений |
5Родий |
Палладий |
||||||||||||||
47 |
|
48 |
|
In114,8249 |
Sn |
50 |
Sb |
|
51 |
Тe |
|
52 |
I |
|
53 |
|
|
Xe |
|
54 |
||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
107,86Ag |
112,40Сd |
118,69 |
|
121,75 |
|
78,96 |
|
126,9044 |
|
|
|
131,30 |
||||||||||
|
|
8Серебро |
Кадмий |
Индий |
Олово |
Сурьма |
Теллур |
Йод |
|
|
|
|
Ксенон |
|||||||||||
|
|
Cs |
55 |
Ва |
56 |
57 * |
La |
72 |
|
|
73 |
|
|
74 |
|
|
75 |
Re |
76 |
77 |
78 |
|
|
|
|
|
132,905 |
137.34 |
138,81 |
178.49Hf |
180,94Та |
183.85W |
186,2 |
190,2 Оs |
192,2 Ir |
195,09Рt |
|||||||||||||
6 |
Цезий |
Барий |
Лантан |
Гафний |
8Тантал |
Вольфрам |
Рений |
Осмий |
Иридий |
Платина |
||||||||||||||
79 |
|
80 |
|
ТI204,3781 |
Pb |
82 |
Вi |
|
83 |
Ро |
|
84 |
At |
|
85 |
|
|
Rn |
|
86 |
||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
196,96Аu |
200,59Hg |
207,19 |
|
208,980 |
|
[210] |
|
210 |
|
|
|
[222] |
||||||||||
|
|
7Золото |
Ртуть |
Таллий |
Свинец |
Висмут |
Полоний |
Астат |
|
|
Радон |
|||||||||||||
7 |
Fr[223] 87 |
Rа[226] 88 |
89138,81**Ас |
[261]104Rf |
[105262] |
Db |
[106263] |
Sg |
[107262] |
Bh |
[108265] Hs |
[109266] Мt |
|
|
|
|||||||||
Франций |
Радий |
Актиний |
РезерфордийДубний |
Сиборгий |
Борий |
Хассий |
Мейтнерий |
|
|
|
||||||||||||||
|
|
|
|
|
||||||||||||||||||||
|
Высшиеоксиды |
R2О |
RO |
R2O3 |
RO2 |
R2O5 |
RO3 |
R2O7 |
|
RO4 |
|
|
|
|||||||||||
|
ЛВС |
|
|
|
|
|
|
RH4 |
RH3 |
RH2 |
RH |
|
|
|
|
|
||||||||

Строение и свойства атомов
•Щелочные металлы – это элементы главной подгруппы I группы Периодической системы химических элементов Д.И. Менделеева: литий, натрий, калий, рубидий, цезий, франций.
•На внешнем энергетическом уровне атомы этих элементов содержат по одному электрону, находящемся на сравнительно большом удалении от ядра. Они легко отдают этот электрон, поэтому являются сильными восстановителями. Во всех соединениях щелочные металлы проявляют степень окисления +1.
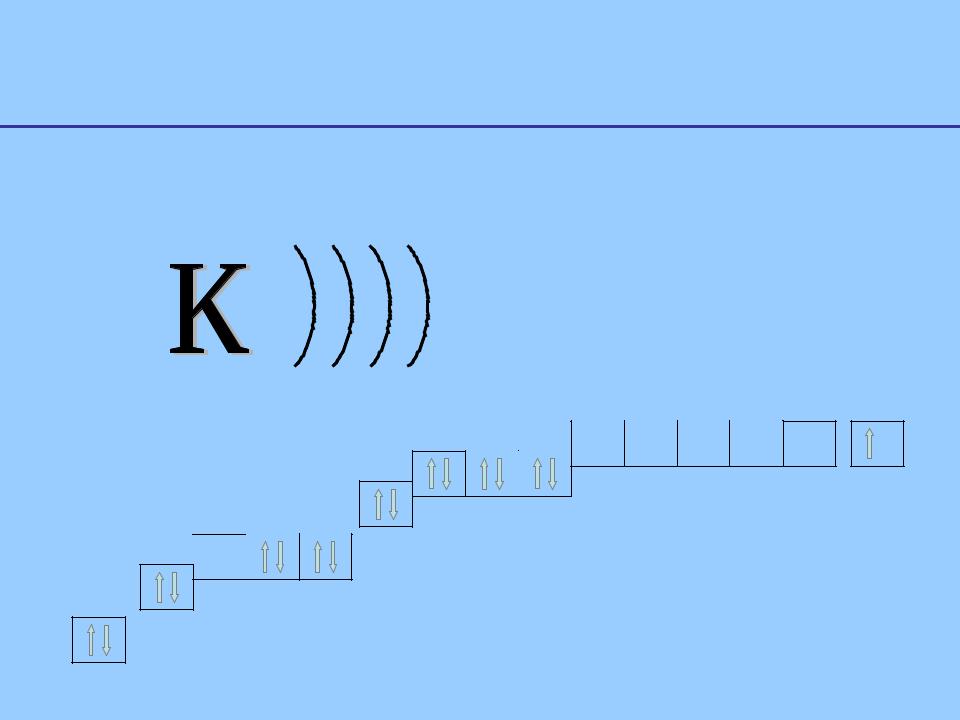
Калий
39 0
e = 19P = 19 N = 20
+19
2 8 |
8 |
1 |
3d0 |
4s1 |
|
3s2 |
3p6 |
|
|
|
|
|
||
2p6 |
|
|
|
|
2s2 



1s2
Краткая электронная запись - |
____ |

Щелочные металлы – простые вещества
Натрий
Литий

Щелочные металлы
Калий |
Рубидий |
|

Цезий

Физические свойства
•Серебристо – белые мягкие вещества (режутся ножом), с характерным блеском на свежесрезанной поверхности. Все они лёгкие и легкоплавкие, причём, как правило, плотность их возрастает от лития к цезию.

Химические свойства
• А) с простыми веществами
2Li + Н2 = 2LiН – гидрид лития; 2К + Сl2 = 2КСl – хлорид калия; 2Nа + S = Nа2S – сульфид натрия; 4 Li + О2 = 2Li2О – оксид лития.
б) со сложными веществами 2Nа + 2НОН = 2NаОН + Н2

