
- •Номенклатура
- •Алкены – ациклические
- •Строение
- •1. Выбор главной цепиСН3 .СН СН СН СН3
- •Агрегатное состояние:
- •Химические
- •главная
- •Применение Ацетальдегид
- •ТипАлкенгибридизациимассой 4,2 г Проверка АлкенамКакой тинепхарактерныизомерии Общаяособенатомприсоединитьф врмууглеродаалкенов8 г брома. знаний


Номенклатура |
Физические |
Получение |
|
свойства |
|||
|
|
Строение |
CnH2n |
Проверка |
молекулы |
знаний |
Изомерия |
Химические |
Применение |
|
свойства |
|||
|
|
19.06.19 |
2 |

Алкены – ациклические |
CnH2n |
углеводороды, в молекуле |
|
которых кроме одинарных |
|
связей содержится одна |
|
двойная связь между |
|
атомами углерода. |
|
Общая формула: СnH2n |
|
19.06.19 |
3 |
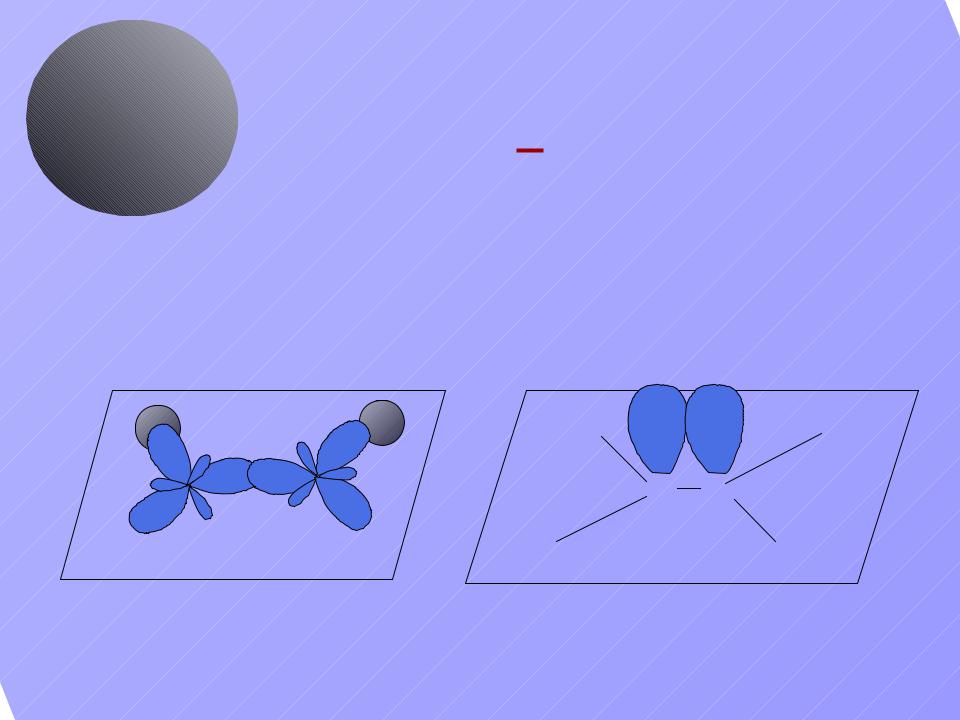
Строение |
sp2-гибридизация |
||
молекулы |
Cπ |
|
δC |
|
|||
|
Угол связи – 1200 |
||
Форма молекулы – плоский треугольник
н |
н |
с |
с |
 н н
н н 
н |
н |
с |
с |
н н
н
19.06.19 |
4 |

1. Выбор главной цепиСН3 .СН СН СН СН3
СН
2. Нумерация3 атомов
главной5 4 цепи3 2. 1 СН3 СН СН СН СН3
СН СН3
|
СН |
3. Формирование |
|
|
3 |
названия. |
|
СН3 |
СН СН СН СН3 |
|
СН |
Номенклатура
4 - пент - метил ен 2
19.06.19 |
3 |
5 |

|
|
|
|
|
|
|
|
|
1. Структурная |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Изомерия |
|
|
|
изомерия. |
|
|
|
|
бутен - 1 |
|||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||||||
|
|
СН3 |
СН32 СН СН2 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
метилпропен СН3 |
С |
|
|
|
СН2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
2. Изомерия положения |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
двойной |
|
|
связ |
и. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
СН3 СН |
|
|
СН |
СН |
|
СН3 |
СН |
|
СН СН |
|||||||||||||||||||||
|
|
|
|
|||||||||||||||||||||||||||
|
бутен - |
2 |
|
|
|
|
|
бутен - |
||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
3 |
|
||||||||
3. Геометрическая изомерия. |
|
|
|
|
|
|
|
|||||||||||||||||||||||
СН3 |
1 |
|
|
|
СН3 |
|
СН3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Н |
|
С |
|
|
С Н |
|
|
|
Н |
С |
|
|
С |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
цис-бутен |
|
|
|
транс- |
|
|
|
|
|
|
|
|||||||||||||||||||
4. Межклассовая- 2 |
изомериябутен. |
- 2 |
|
|
|
|
|
|
||||||||||||||||||||||
СН |
|
|
СН |
|
СН |
проп |
|
|
|
|
|
|
|
|
|
|
|
циклопро |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
ен |
|
|
|
|
|
|
|
|
|
|
|
|
пан |
|||||||
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
19.06.19 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
||||||||||

Агрегатное состояние: |
Физические |
||||||
свойства |
|||||||
С Н – |
|
|
газообразные |
|
|||
|
|
|
|||||
С2Н4 |
|
|
вещества; |
|
|||
С54Н108 – |
|
|
|
жидкост |
|
||
|
|
|
|
||||
С18Н36 |
|
|
|
|
|
и; |
|
|
твердые |
|
|||||
с С19Н38 |
|
||||||
вещества С увеличением молекулярной массы соединений
температуры кипения и плавления закономерно
Этилен |
повышаются. |
|
||
Г, |
З нефтяной, |
Плохо в |
||
С2НT4 = - |
Ц |
Tкип = - 103,70С |
||
Н2О |
||||
пл |
|
|
|
|
169,20С |
|
|
|
|
19.06.19 |
|
|
7 |
|
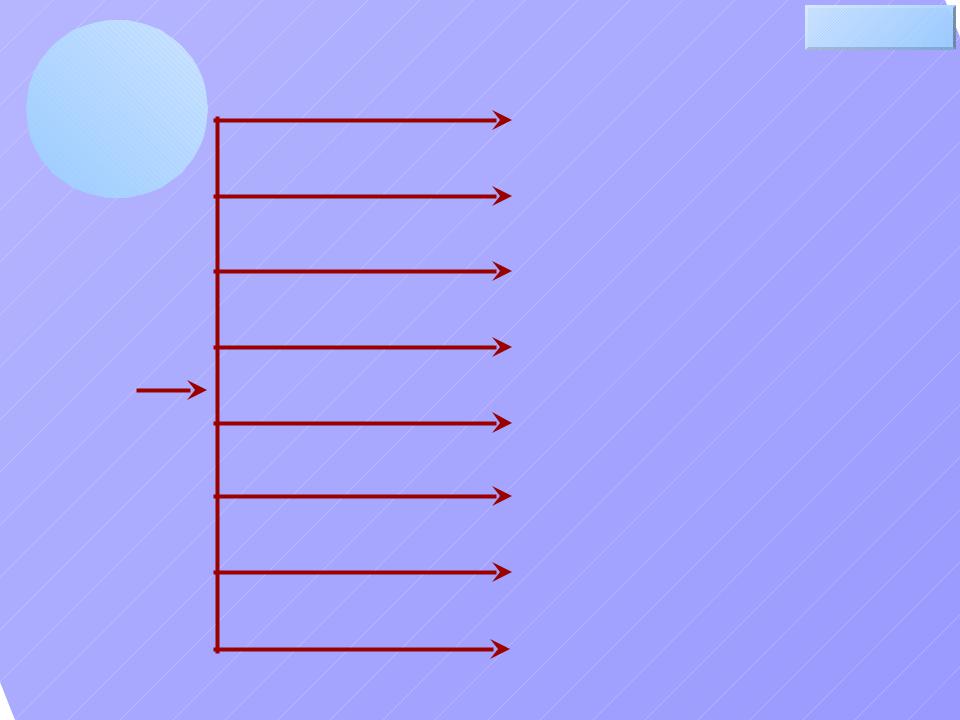
Химические
свойства
СnH2n
19.06.19
+ Н2, t0, Ni
+ Hal2
+ HHal
+ H2O, t0, H+
+ H2O + [O]
+ O2, t0
(горение)
- H2, t0, Ni
+ nCnH2n
этилен
CnH2n+2
дигалогеналканы,
СnH2nHal2
галогеналканы,
СnH2n+1Hal
CHnH2n+1O
CnH2n(OH)2
CO2 + H2O
CnH2n-2
полимер
8


 главная
главная 

1. |
|
|
СН2 |
|
|
|
СН2 + Н2 |
|
|
Pt, t |
СН3 |
|
|
|
|
|
СН3 |
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
Гидрировани |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2. |
Галогенирование: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
СН2 + Br2 |
СН2Вr СН2Вr |
||||||||||||||||||||||||||||||||||||||||||||||
е: |
|
|
|
|
СН2 |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
3. Гидрогалогенировани |
е: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
СН2 + НСl |
|
|
|
CН3 |
|
СН2Сl |
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
СН2 |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
4. |
Гидратация: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
t, Н3РО4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
СН2 |
|
+ Н2О |
|
|
|
|
|
|
|
|
|
|
|
CН3 СН2ОН |
||||||||||||||||||||||||||||||||||||
|
СН2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
5. Мягкое |
|
|
|
|
СН2 |
|
|
|
СН2 + [О] +Н2О |
|
СН2 |
|
|
|
СН2 |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
окисление: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2Н2О ОН |
|
|
ОН |
|||||||||||||||||||||
6. |
СН2 |
|
СН2 + 3О2 |
|
|
2СО2 |
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
Горение: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7. |
|
|
|
СН2 |
|
|
|
СН2 |
|
t, Ni |
|
СН |
|
|
|
|
СН + Н2 |
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
Дегидрировани |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
8. |
|
|
nСН |
|
|
СН |
|
|
|
cat |
( |
|
|
|
|
|
|
|
|
|
СН |
2 |
|
|
|
СН |
2 |
|
|
…)n |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
е: |
|
|
|
|
2 |
|
|
|
|
2 |
|
|
|
|
|
|
… |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
Полимеризация |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
: 19.06.19 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
9 |
|||

1. |
Крекинг нефтепродуктов: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Получение |
||||||||||||||||||||||||||||||
С16Н34 |
|
|
|
|
С8Н18 + С8Н16 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
2. |
Дегидрирование предельных |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
углеводородов: |
СН2 |
|
|
|
СН |
|
|
|
|
СН2 |
|
|
|
|
СН3 + Н2 |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
СН3 |
|
|
|
СН2 |
|
СН2 |
СН3 |
СН |
3 |
|
|
|
|
|
СН |
|
|
|
|
|
СН |
|
|
|
СН |
+ Н |
2 |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
3. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
||
Дегидратация спиртов (отщепление |
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
воды): |
|
|
|
|
|
|
|
|
|
Н2SО4 , 140 – |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
СН3 |
|
|
|
СН2 |
ОН |
|
1500С |
|
|
|
|
|
|
|
|
СН2 |
|
|
|
|
|
СН2 |
+ |
|
|
|
|
||||||||||||||||||||||
4. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Н2О |
|
|
||||
Дегидрогалогенирование (отщепление |
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
галогеноводорода): спирт, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
СН |
|
|
СН СН |
|
СН + |
t |
|
|
|
|
|
СН3 |
|
|
СН |
|
|
СН СН3+Na +Н2 |
|||||||||||||||||||||||||||||||
|
3 |
|
|
|
|
|
|
|
|
|
2 |
|
|
3NaОН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Br |
О |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
5. |
|
|
|
|
B |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
r |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Дегалогенировани |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
СН |
|
|
СН СН СН +ZnB |
|
|||||||||||||||||||||||||||||||||||||||||||
СН |
|
|
СН СН СН +Z |
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
е: |
3 |
|
|
|
|
|
|
|
|
|
|
|
3n |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3r2 |
|
|
|
|||||
|
|
|
|
B |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
B |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
19.06r.19 |
|
r |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
||||||||
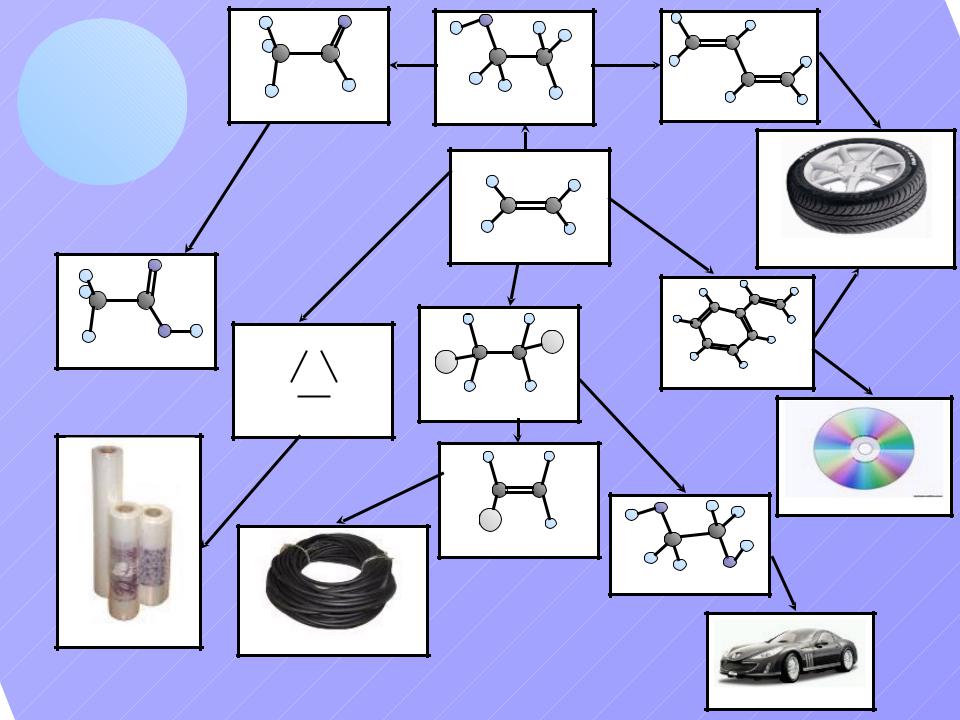
Применение Ацетальдегид |
Этанол |
Уксусная кислота |
О |
Н2С |
СН2 |
Оксид этилена |
|
Этилен
1,2-дихлорэтан |
Хлорвинил
Полиэтилен Поливинилхлорид 19.06.19
Бутадиен-1,3 |
Синтетический
каучук
Стирол |
Полистирол
Этиленгликоль
11
Антифриз
