
11)Зависимость теплоемкости от различных факторов. Вывод уравнения Майера.Показатель Пуассона
Удельная теплоемкость зависит не только от свойств вещества, но и от того, при каком процессе осуществляется теплопередача. Если нагревать газ при постоянном давлении, то он будет расширяться и совершать работу. Для нагревания газа на 1 °С при постоянном давлении ему нужно передать большее количество теплоты, чем для нагревания его при постоянном объеме
вывод уравнения майера
Теплоемкостью тела
С называется отношение бесконечно ма
юго количества тепла бQ, полученного
телом, к соответствующему приращению
dT его температуры:
![]() Если
учесть по первому закону термодинамике:
Если
учесть по первому закону термодинамике:![]() можно написать
можно написать
![]() Надо
учеть:
Надо
учеть:![]() Легко
выводиться
Легко
выводиться
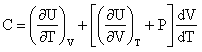 Особое
значение имеют теплоемкости при
постоянном объеме и постоянном давлении,
обозначаемые символами Cv и Ср. Если
объем остается постоянным, то dV = 0, и
следовательно,
Особое
значение имеют теплоемкости при
постоянном объеме и постоянном давлении,
обозначаемые символами Cv и Ср. Если
объем остается постоянным, то dV = 0, и
следовательно,
![]() Если
же постоянно давление, то отношение
Если
же постоянно давление, то отношение
![]() переходит
в частную производную
переходит
в частную производную
![]() В
этом случае
В
этом случае
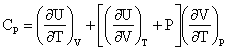 Для
разности теплоемностей Сp—Cv получаем
Для
разности теплоемностей Сp—Cv получаем
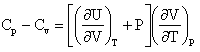 По
закону Джоуля
По
закону Джоуля
![]() .
Из уравнения Клапейрона следует
.
Из уравнения Клапейрона следует
![]() .
Поэтому указанная формула дает
.
Поэтому указанная формула дает
![]() Это
важное соотношение называется уравнением
Роберта Майера.
Это
важное соотношение называется уравнением
Роберта Майера.
![]() Подставляя
это соотношение в формулы теплоёмкости
получаем для изохорной.
Подставляя
это соотношение в формулы теплоёмкости
получаем для изохорной.
![]() Для
изобарной:
Для
изобарной:
![]() Измерив
теплоемкости Сp и Cv газа, можно вычислить
механический эквивалент теплоты. Для
этого можно воспользоваться уравнением
Роберта Майера. Измеряя количество
тепла в калориях, можно на опыте найти
разность Сp—Cv в тепловых единицах. С
другой стороны, газовую постоянную R
можно измерить в механических единицах.
Измерив
теплоемкости Сp и Cv газа, можно вычислить
механический эквивалент теплоты. Для
этого можно воспользоваться уравнением
Роберта Майера. Измеряя количество
тепла в калориях, можно на опыте найти
разность Сp—Cv в тепловых единицах. С
другой стороны, газовую постоянную R
можно измерить в механических единицах.
Адиабата Пуассона
Для идеальных газов, чью теплоёмкость можно считать постоянной, в случае квазистатического процесса адиабата имеет простейший вид и определяется уравнением
![]()
где
![]() —
его объём,
—
его объём,
![]() —
показатель адиабаты,
—
показатель адиабаты,
![]() и
и
![]() —
теплоёмкости газа соответственно при
постоянном давлении и постоянном объёме.
—
теплоёмкости газа соответственно при
постоянном давлении и постоянном объёме.
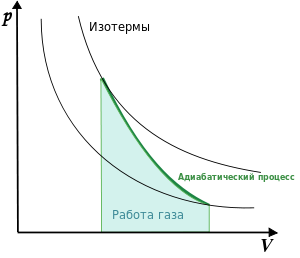
График
адиабаты (жирная линия) на
![]() диаграмме
для газа.
p — давление газа;
V —
объём.
диаграмме
для газа.
p — давление газа;
V —
объём.
С учётом уравнения состояния идеального газа уравнение адиабаты может быть преобразовано к виду
![]()
где T — абсолютная температура газа. Или к виду
![]()
Поскольку
![]() всегда
больше 1, из последнего уравнения следует,
что при адиабатическом сжатии (то есть
при уменьшении V) газ нагревается
(T возрастает), а при расширении —
охлаждается, что всегда верно и для
реальных газов. Нагревание при сжатии
больше для того газа, у которого больше
коэффициент
.
всегда
больше 1, из последнего уравнения следует,
что при адиабатическом сжатии (то есть
при уменьшении V) газ нагревается
(T возрастает), а при расширении —
охлаждается, что всегда верно и для
реальных газов. Нагревание при сжатии
больше для того газа, у которого больше
коэффициент
.
Согласно закону Менделеева — Клапейрона справедливо соотношение
![]()
где R — универсальная газовая постоянная. Продифференцировав обе части, получаем
|
Если в (3) подставить dT из (2), а затем dU из (1), получим
![]()
или, введя коэффициент :
![]() .
.
Это уравнение можно переписать в виде
![]()
что после интегрирования даёт уравнение
![]() .
.
Окончательно получаем
![]()
что и требовалось доказать.
